【识林心得】几个可以长期收藏的页面
识林基于长期跟踪和系统整理,制作了多个专题索引页面,旨在将分散的信息集中呈现,降低检索成本。以下四个索引较为典型,分别覆盖ICH指南国内官方版本、CDE专家文献、各省变更管理细则以及PIC/S GMP资源。每个索引按专业领域分类,标注关键信息点(如适用阶段、文件状态、发布时间等),并保持动态更新,供研发、注册、合规及质量人员参考。
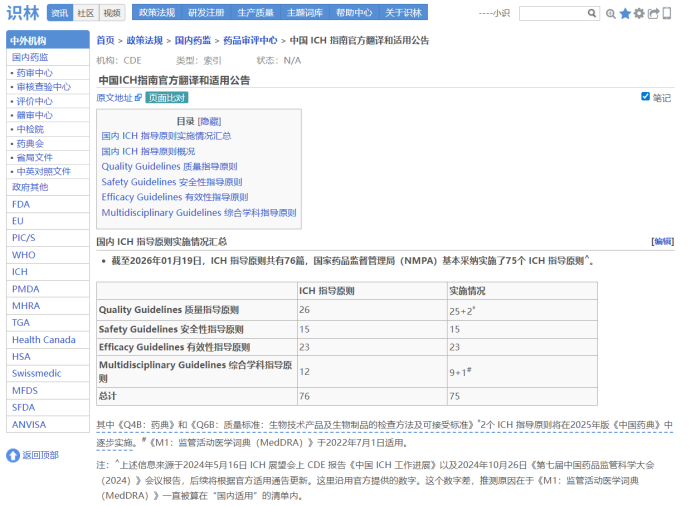
除了专门为ICH制作索引之外,识林考虑到国内会员需要,梳理了CDE官方发布的ICH指南中文翻译及适用公告:目前共有征求意见翻译100个、定稿翻译108个、适用公告87个,覆盖质量(Q系列)、安全性(S系列)、有效性(E系列)及综合学科(M系列)四大领域。本索引页实时跟踪官方动态,汇总每项指南的Step阶段、翻译稿和适用时间点,帮助快速定位最权威的中文版ICH技术文件,高效指导药品研发与注册申报。
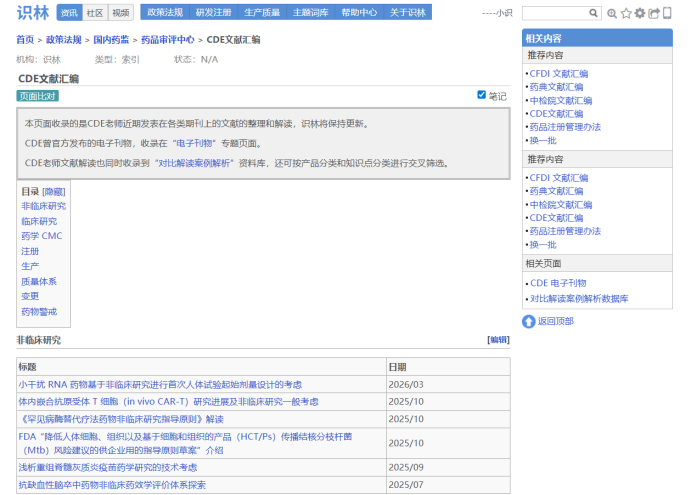
本页面系统梳理了CDE老师近年来发表于核心期刊的学术文献,并持续更新。内容覆盖非临床研究、临床研究、药学CMC、注册、生产、质量体系、变更管理及药物警戒八个领域,汇聚审评专家对新技术、新方法、典型案例的深度解读。无论是小干扰RNA、CAR-T、mRNA疫苗等前沿品种,还是ICH指南落地、变更管理、中药监管等热点议题,都能快速找到官方审评视角下的关键考量。此外,资深研发注册人也许都记得,CDE曾将早期文献收录于官网“电子刊物”板块,识林也保留了一套完整的索引,供会员参阅。
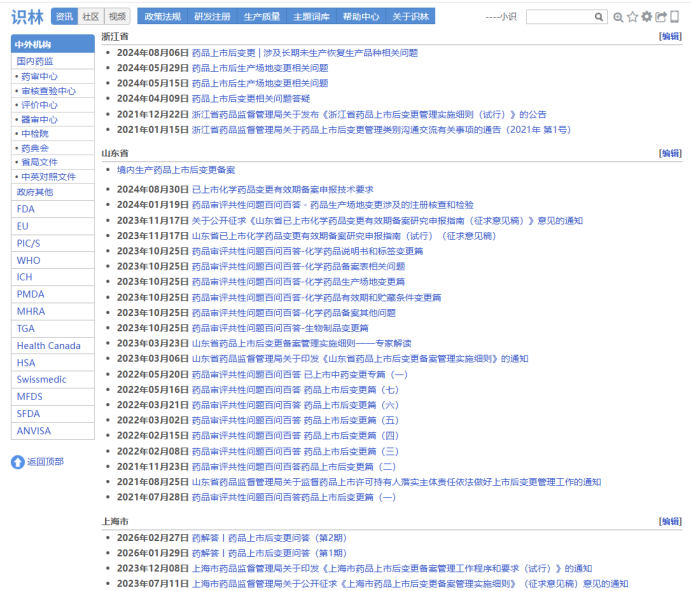
药品上市后变更是企业日常合规中的高频事项,但各省局实施程序和要求不尽相同,补充申请试点以来更需特别关注。识林系统梳理全国各省(区、市)药监局发布的药品上市后变更管理相关文件,涵盖北京、上海、江苏、浙江、山东、广东等省市的实施细则、备案指南、共性问题解答、沟通交流程序及申报资料撰写指导。无论是生产场地变更、包材变更、有效期变更还是供应商变更,均可快速定位属地管理要求,规避合规风险。对于公司产品横跨多个省市的会员更具价值。
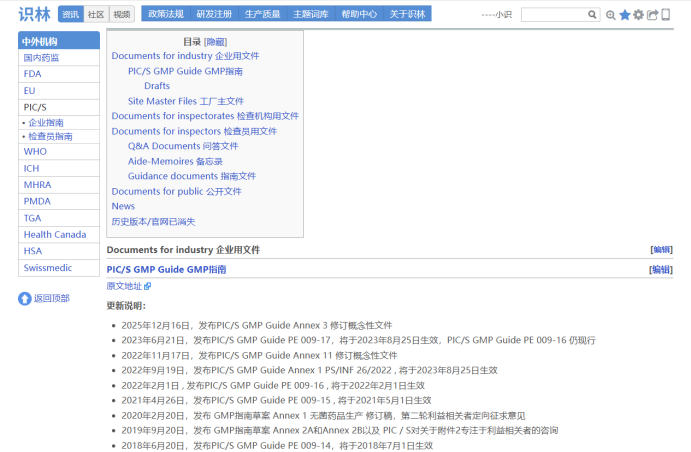
PIC/S(药品检查合作计划)是全球药品检查机构互认的核心组织(我国正在加入进程中),其GMP指南是国际通行标准。识林系统梳理PIC/S官方发布的全量资源,涵盖GMP指南(PE 009-17及全部附录)、修订概念文件、工厂主文件(SMF)、检查备忘录、数据可靠性、远程评估、交叉污染控制等关键指南,并为重要文件提供中英双语版本。
|责任编辑:识林-木姜子
|编辑:识林-雪见
识林®版权所有,未经许可不得转载

【关于识林-常见问题与解答】

