周末文摘 | 关于创新医疗器械经济学评价的思考


引用本文
卢忠,李丹荣,姜明欢,郝丽静,赵明月,周思奇,彭晋,方宇*.关于创新医疗器械经济学评价的思考[J].中国食品药品监管,2026(3):4-13.
关于创新医疗器械经济学评价的思考
Reflections on the Economic Evaluation of Innovative Medical Devices
卢忠
中国药品监督管理研究会医疗器械监管研究专业委员会
新型生物材料与高端医疗器械广东研究院
LU Zhong
Special Commitee for Medical Device Regulation, China Society for Drug Regulation
Guangdong Institute of Advanced Biomaterials and Medical Devices
李丹荣
国家药品监督管理局南方医药经济研究所
LI Dan-rong
National Medical Products Administration Institute of Medical Economics
姜明欢
西安交通大学药学院
西安交通大学药品安全与政策研究中心
国际药物经济学与结果研究学会(ISPOR)中国西北分中心
JIANG Ming-huan
School of Pharmacy, Xi'an Jiaotong University
Center for Drug Safety and Policy Research, Xi'an Jiaotong University
ISPOR Northwest China Chapter
郝丽静
新型生物材料与高端医疗器械广东研究院
国家药品监督管理局监管科学创新研究基地
HAO Li-jing
Guangdong Institute of Advanced Biomaterials and Medical Devices
NMPA Center for Innovation and Research in Regulatory Science
赵明月
西安交通大学药学院
西安交通大学药品安全与政策研究中心
国际药物经济学与结果研究学会(ISPOR)中国西北分中心
ZHAO Ming-yue
School of Pharmacy, Xi'an Jiaotong University
Center for Drug Safety and Policy Research, Xi'an Jiaotong University
ISPOR Northwest China Chapter
周思奇
西安交通大学药学院
西安交通大学药品安全与政策研究中心
国际药物经济学与结果研究学会(ISPOR)中国西北分中心
ZHOU Si-qi
School of Pharmacy, Xi'an Jiaotong University
Center for Drug Safety and Policy Research, Xi'an Jiaotong University
ISPOR Northwest China Chapter
彭晋
西安交通大学药学院
西安交通大学药品安全与政策研究中心
国际药物经济学与结果研究学会(ISPOR)中国西北分中心
PENG Jin
School of Pharmacy, Xi'an Jiaotong University
Center for Drug Safety and Policy Research, Xi'an Jiaotong University
ISPOR Northwest China Chapter
方宇*
西安交通大学药学院
西安交通大学药品安全与政策研究中心
国际药物经济学与结果研究学会(ISPOR)中国西北分中心
FANG Yu*
School of Pharmacy, Xi'an Jiaotong University
Center for Drug Safety and Policy Research, Xi'an Jiaotong University
ISPOR Northwest China Chapter
摘 要 / Abstract
医疗器械产业作为国家战略性新兴产业,其发展直接关乎民生健康与国家竞争力。我国通过《创新医疗器械特别审查程序》等政策构建了针对创新医疗器械的审评审批体系,但在其临床应用价值评估、医保支付标准建立等方面仍面临挑战。卫生经济学评价可为量化创新医疗器械成本效益、形成医保准入决策依据提供有效的分析工具。本文通过国际案例比较与政策分析,剖析当前国内创新医疗器械评价体系中存在的深层矛盾,提出构建“价值量化、动态调整、多方协同”的“三医”协同体系,旨在探讨适配我国国情的创新医疗器械价值评估框架,为我国构建科学、高效的创新医疗器械价值评估与决策体系提供关键参照。
As a national strategic emerging industry, the medical device sector has profound implications for public health and industrial competitiveness. China has established a review and approval framework for innovative medical devices through policies such as the Special Review Procedure for Innovative Medical Devices. Nevertheless, the current system faces challenges in accurately assessing clinical value and establishing standardized reimbursement criteria. Health economic evaluation, as a pivotal analytical tool in health policy research, offers a methodological approach to quantify the cost-effectiveness of innovative medical devices and provide evidence-based support for reimbursement decision-making. Through international case comparisons and policy analysis, this paper identifies underlying challenges in China's domestic evaluation system for innovative medical devices and proposes a "tripartite coordination system" featuring "value quantification, dynamic adjustment, and multi-stakeholder collaboration." It aims to explore a value evaluation framework tailored to China’s context and provide key references for establishing a scientific and efficient evaluation and decision-making system for innovative medical devices in China.
关 键 词 / Key words
创新医疗器械;卫生经济学评价;临床价值评估;医保准入;卫生政策研究
innovative medical devices; health economic evaluation; clinical value assessment; medical insurance reimbursement; health policy research
基金项目
国家科技重大专项研究课题(2025ZD0548004);2023 年中国药品监督管理研究会课题(2023-Y-Q-012);广东省重点领域研发计划项目(2025B1111090001)

医疗器械产业是关系国计民生和国家安全的战略性新兴产业,发展创新医疗器械是发展新质生产力的重要组成部分,也是推动经济高质量发展的重要领域,对于提升产业竞争力、满足公众健康需求具有关键作用。为深入推进审评审批制度改革,鼓励医疗器械创新,深化供给侧结构性改革和“放管服”改革要求,激励产业创新高质量发展,国家药品监督管理局逐步构建了一套创新医疗器械审评审批体系。2014 年,原国家食品药品监督管理总局印发了《创新医疗器械特别审批程序(试行)》;2018 年,国家药品监督管理局修订发布了《创新医疗器械特别审查程序》及《创新医疗器械特别审查申报资料编写指南》等一系列配套文件,有力推动了国产创新医疗器械发展,更好地满足了人民群众对高端医疗器械的需求。我国医疗器械市场持续高速增长,成为目前全球最具潜力的医疗器械市场之一。医疗器械作为受法规严格监管的特殊商品,实行上市准入管理制度。《创新医疗器械特别审查程序》要求申请人已完成产品的前期研究并具有基本定型产品,且具有显著的临床应用价值。目前,对“显著临床应用价值”的界定尚不明确,市场准入环节也缺乏量化维度评价。此外,在产品上市后的医保支付环节,对其经济性与综合价值的考量仍缺乏标准化的数据采集路径与证据衔接机制。有鉴于此,高价值创新医疗器械在市场准入与使用环节仍面临诸多挑战。
如何科学评估医疗器械的综合价值,并将评估证据应用于市场准入、医保支付等决策场景,已成为全球许多国家和地区卫生系统面临的共同挑战。在此背景下,卫生经济学评价逐渐成为连接“产品-价值- 决策”的关键工具。通过成本-效用分析(cost-utility analysis,CUA)、成本-效果分析(cost-effectiveness analysis,CEA)和成本-效益分析(cost-benefit analysis,CBA)等方法,卫生经济学评价能够系统量化创新器械与现有方案在成本与健康收益方面的差异。评价方法体系是否适配器械特性、评价结果能否支撑多方决策、政策机制能否保障评价落地,已成为平衡“创新激励、患者可及、医保可持续”三者关系的关键议题。评价结果不仅能够为价格谈判、医保准入与医院采购提供科学依据,促进高价值医疗技术和创新医疗器械的有序引入和合理使用,提升整体医疗服务效率和患者健康获益,也有助于优化支付优先级和准入流程,提升决策的规范性、科学性与透明度,推动形成以价值为导向的创新医疗器械准入与支付体系。
本文通过梳理部分国家相关卫生经济学评价指南、医保政策文件、配套法规及学术文献,开展对典型国家的案例比较分析,剖析国际上主流应用模式在评价主体、评估对象、决策流程、应用场景、证据要求等方面的具体运行机制及制度逻辑。同时,结合国内卫生经济学评价的应用现状和政策环境以及创新医疗器械的特点,为我国构建科学、高效且适配国情的创新医疗器械价值评估与决策体系提供切实可行的参考依据。

01
部分国家医疗器械经济学评价的应用模式
本文梳理了部分国家在医疗器械经济学评价中的实践差异,遴选了英国、澳大利亚、加拿大、瑞典、韩国、日本、德国、法国等典型国家,对其医疗器械经济学评价机制进行比较(表1)。分析涵盖评价组织方、证据使用方、具体应用场景等维度,旨在揭示不同体系下医疗器械价值评估模式的核心特征与政策导向差异。
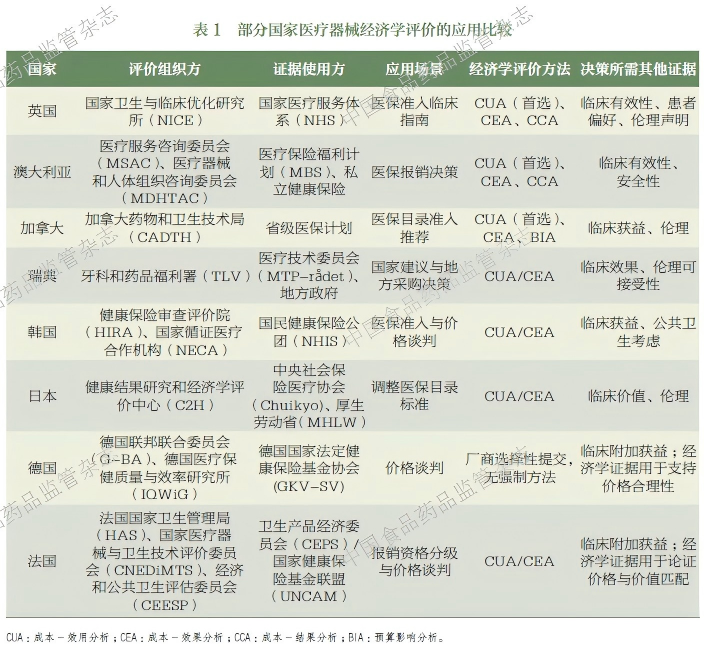
本研究在表1 列出的8 个国家中,选取英国、德国、日本进行详细介绍,主要基于以下考量:这3 个国家分别代表卫生经济学评价在医疗器械领域的3 种典型应用模式——英国的前置性评估与固定增量成本-效果比(incremental cost-effectiveness ratio,ICER)阈值决策、德国的临床附加获益先导与价格谈判、日本的上市后动态调价与真实世界数据驱动。这3 种范式与本文关于医保支付体系中的经济学评价核心议题直接对应,有一定的启示。
1.1 英国:“分层评价+ 快速通道”,兼顾严谨性与创新效率
英国国家卫生与临床优化研究所(National Institute for Health and Care Excellence,NICE)通过评估新技术的临床效果和成本效益,判断其是否值得国家医疗服务体系(National Health Service,NHS) 的公共资金投入[1]。NICE 内部设有多个医疗器械评估路径。例如,医疗技术评估计划(medical technologies evaluation programme,MTEP)[2] 专门评估具有临床优势且能为NHS 节省系统成本的治疗类器械, 通常采用成本- 结果分析(cost-consequence analysis,CCA)[3] ;而诊断评估计划(diagnostics assessment programme,DAP)[4] 则聚焦于诊断类器械,严格采用CUA,并将计算得出的ICER 值与官方设定的20 000~30 000 英镑/ 质量调整生命年(quality-adjusted life year,QALY)的阈值范围进行比较,以此作为是否推荐的核心依据。在实际决策中,除经济学证据外,临床有效性、患者偏好和伦理声明等因素也会被纳入综合考量。
1.2 德国:“临床分级+ 价格谈判”,锚定创新的临床价值核心
德国依据《德国社会法典》(German Social Code)第五部第35a 条规定,确立以“临床附加获益”为核心的法定医疗保险支付决策机制,强调实行“先临床准入、后经济协商”的法定程序[5]。医疗器械在取得CE 认证后,须由德国联邦联合委员会(The Federal Joint Committee,G-BA)主导开展临床附加获益评估,G-BA 通常委托医疗保健质量与效率研究所(Institute for Quality and Efficiency in Health Care,IQWiG) 提供科学支持。未能证明具有临床附加获益的产品,不得纳入国家法定健康保险基金协会(GKV-Spitzenverband,GKV-SV)支付范围。根据应用场景及风险等级,德国对医疗器械的具体医保支付路径作出区分:其中,住院使用的医疗器械原则上通过疾病诊断相关分组(diagnosis related groups,DRG)进行打包支付。若为创新医疗器械且成本超出现行DRG 覆盖范围,医疗机构可向医院支付研究所(Institute for the Hospital Remuneration System,InEK)申请新诊疗方法,以获得临时附加支付。若涉及高风险医疗器械,则需依据《德国社会法典》第137h 条款接受单独评估[6]。而对于门诊使用的医疗器械,则须先通过G-BA 评估,并纳入《统一评估量表》(Einheitlicher Bewertungsmaßstab,EBM)后,方可获得医保支付资格[7]。在完成临床评估并取得支付资格后,相关企业方可与GKV-SV 开展价格谈判,其提交的卫生经济学评价报告仅作为论证定价合理性及其与临床价值匹配度的参考依据。
1.3 日本:“全生命周期动态调价+ 真实世界数据库支撑”,破解证据滞后难题
日本对医疗器械经济学评价(特别是成本效益分析)的应用重心已从市场准入前转移至上市后,其核心功能被定位为对已上市技术进行价值再评估和价格动态调整的治理工具。这种模式旨在应对创新医疗器械在上市初期证据不足的挑战,允许其先进入市场,在真实世界中积累证据后,再对其价值和价格进行校准。具体而言,一项新技术在接受正式的成本效益评估前,已根据其适用的定价规则获得了医保支付资格及初始医保支付价格。医疗器械的初始医保定价主要采用类似功效比较法或成本计算法[8]。对于已被纳入医保目录且具备创新性高、费用高昂或对医保基金影响巨大特征的产品,厚生劳动省(Ministry of Health, Labour and Welfare,MHLW)可将其提名至中央社会保险医疗协会(Central Social Insurance Medical Council,Chuikyo)以启动经济学评价。Chuikyo 负责审核企业提交的卫生经济学报告,并依据评估所得的ICER 区间确定相应的支付标准调整比例。例如,若ICER 值低于500 万日元/QALY,则判定为具有成本效益,支付标准维持不变;若ICER 值在500 万~750 万日元/QALY之间,则被判定为成本效益较差,相关支付标准将依据评估结果按比例下调。
1.4 其他国家应用模式
除上述3 种典型模式外,其他部分国家也结合各国国情,形成了具有自身特点的经济学评价应用路径。例如,在法国,实际临床获益和附加临床获益是卫生产品经济委员会(Comité Économiquedes Produits de Santé,CEPS) 定价决策的首要依据[9],而经济学评价仅对年销售额超过2000 万欧元的医疗器械强制要求提交,其结论仅起辅助验证作用,无权调整附加临床获益所确定的基础定价权限[10]。在加拿大,联邦层面对于医疗器械的经济学评价结果仅提供参考建议,医保准入和报销决策最终由各省独立制定,各省在进行地方决策时可自行补充开展经济学评价以辅助决策。在瑞典,通过采用社会视角统计总成本(含生产力损失),在特定情况下对QALY 进行差异化加权,并将人类尊严、需求、团结以及成本效益等原则置于优先地位,以确保医疗资源分配的公平性[11]。在韩国,健康保险审查评价院(Health Insurance Review and Assessment Service,HIRA)对创新医疗器械进行经济学评估,以确定其是否符合国民健康保险(National Health Insurance,NHI)制度的报销资格,并协商确定支付标准[12]。
总体来看,上述国家在保障医疗器械临床安全有效性的前提下,普遍将经济学评价作为相关产品纳入医保支付体系的重要决策工具,并结合自身的支付能力和价值理念,形成了多元化且因地制宜的实践格局。值得注意的是,部分发达国家已将医疗器械经济学评价深度融入卫生决策的各个环节,并形成了各具特色的实际应用模式,呈现出更灵活、更细分、更依赖真实世界数据的趋势。无论是英国、澳大利亚等将经济学评价作为医保准入的前置性评估工具,还是德国、法国等以临床附加获益为先导,将经济学评价主要用于支持价格谈判,抑或是日本将其作为上市后医保支付标准动态调整的依据,各国模式均体现了在平衡创新激励、患者可及性与医保基金可持续性等多重目标时所作出的制度选择。具体而言,英国模式将效率置于首位,标准明确但可能延缓创新产品准入;德国模式以临床附加获益为前提,强调科学验证与价格协商,但可能面临为边际附加效益支付较高价格的风险;日本模式则力求在可及性与可持续性之间寻求平衡,但对上市后价值再评估所需的监管能力提出了较高要求。

02
我国创新医疗器械经济学评价的实践场景与现实挑战
我国正逐步将经济学评价融入创新医疗器械全流程管理,但在创新医疗器械审批、地方医保支付实践、支付政策衔接、医疗机构应用等场景中,相关证据链条仍存在短板。随着产业创新加速,相关挑战日益凸显。
2.1 显著临床应用价值缺乏量化评价效能
(1)方法学与医疗器械特性不匹配:现有评价多沿用药品的“CUA+ 固定ICER 阈值” 框架,但创新医疗器械差异显著。例如,人工智能(artificial intelligence,AI)医疗器械的算法迭代成本、植入类医疗器械的长期安全性监测成本、诊断医疗器械的漏诊/ 误诊引发的后续成本等均难以通过传统方法测算。
(2)证据链衔接不紧密:创新医疗器械特别审查和产品注册申报在研发阶段生成的临床数据(如临床试验报告),与后续医保准入所需的经济学证据(如成本测算、预算影响)之间存在脱节。医疗器械临床试验主要记录有效率、并发症发生率等临床指标,但可能会忽略同步收集患者住院时间、治疗费用等经济指标,医保准入时常需重新开展回顾性研究,证据生成周期延长1~2 年。
(3)数据共享机制不完善:开展创新医疗器械的经济学评价,需要从多个相关方获取不同数据,如企业的生产研发数据、医疗机构的临床使用数据、医保部门的支付数据等。然而,目前部分数据处于碎片化离散状态,有效的管理工具和共享机制有待建立。同时,由于相关部门的职责边界不清,存在一定的监管协同障碍,进一步增加了数据获取和整合治理难度,使得创新医疗器械经济学评价缺乏精准数据支撑。
2.2 地方实践中的“经济性门槛”标准碎片化
近年来,各地对新增医疗服务价格项目的申报和审批日益规范,逐步形成以临床价值与经济性为导向的科学决策机制。在多个地区的政策实践中,卫生经济学评价已成为立项评审与价格核定的关键依据。例如,广东省明确规定,拟申报价格在5000 元以上的项目(含可单独收费耗材)必须提交卫生经济学评价报告或已开展项目的临床效价比较报告,否则不予受理[13]。湖南省在政策中明确提出,若申报项目不符合卫生经济学要求,将不被纳入该省公立医疗机构新增医疗服务价格项目范围内[14]。在各地出台的医疗服务价格项目管理办法中,普遍要求对拟新增项目的技术创新性、与现有可比项目的横向对比差异以及完整的经济性证据进行系统论证。天津市要求,对资源消耗大、价格预期高的新增项目,必须提供关于创新性与经济性的评价报告,不符合卫生经济学的要求、性价比不合理的项目不予立项,且评审过程中必须有卫生经济学等领域专家参与[15]。
同时, 在按DRG 和按病种分值付费(diagnosis-intervention packet,DIP)医保支付方式改革持续推进的背景下,各地积极探索在“医保控费”与“激励创新”之间取得平衡。2022 年7 月,北京市医疗保障局发布《关于印发CHSDRG付费新药新技术除外支付管理办法的通知(试行)》,明确对满足三年内获批上市、临床效果较传统方案有较大提升,且对DRG 病组支付标准有较大影响等条件的新药新技术(含医疗器械),经企业申报、形式审查、专家论证及数据验证后,纳入“除外支付”范围,在未来3 年内有效,年终统一据实结算,以保障创新技术合理应用与医保基金可持续的平衡[16]。
此外,在当前医疗成本控制和质量管理并重的环境下,医疗机构管理者在保障医疗质量的前提下,愈发注重提升运营水平和资源使用效率。引入具有成本效果的创新医疗器械,已成为优化诊疗流程、提高服务质量的重要手段。通过缩短平均住院日、减少术后并发症及重复治疗,能在有效提升患者健康获益的同时,助力医疗机构控制总体运营成本[17]。在实际准入和临床使用决策中,医疗机构管理者和临床专家愈发倾向于参考卫生经济学评价结果,并结合本院疾病谱、患者特征和预算状况,从众多同类产品中做出更具科学性和针对性的选择。系统的经济性证据不仅有助于识别出具有临床优势与经济价值的产品,还可推动医疗机构从“低价中标”向“优质优价”的价值导向转变。
2.3 关于完善我国创新医疗器械经济学评价的思考
在医疗器械领域应用卫生经济学评价的基础上,针对创新医疗器械特别审查程序要求,创新医疗器械经济学评价需跳出医保“单一控费”思维,致力于构建“价值量化、动态调整、多方协同”的医疗、医保、医药“三医”协同与联动体系。具体思考主要包括以下方面。
2.3.1 搭建以显著临床应用价值为核心的经济学评价支持体系
建议充分发挥卫生经济学评价在贯通“产品-价值- 决策”方面的关键工具作用,针对创新医疗器械上市早期临床证据可能有限的特点,可重点围绕经济学评价结果,结合风险共担、按疗效付费等多样化支付方式,建立专项准入和动态管理机制。通过实时更新评价数据和动态调整支付标准,既能激励技术创新,又能保障医保基金可持续,还能促进医疗器械市场健康发展。
2.3.2 建立针对不同类别医疗器械的差异化卫生经济学评价框架
针对当前创新医疗器械与集采中选医疗器械缺乏差异化的经济学评价体系、评价针对性不足等问题,可参考国际经验,如英国医保准入评估模式,设立以经济学评价为基础的准入评价路径,旨在为准入决策提供支撑。根据创新医疗器械的技术特性与临床应用场景,可制定差异化评价方法,避免“一刀切”。例如,对于应用AI 的医疗器械,可考虑采用CEA 并辅以长期价值跟踪,核心指标可包括诊断/ 治疗时间缩短率、人工替代率、算法迭代成本,同时引入真实世界数据动态补充。对于植入类医疗器械,宜采用CUA 并辅以安全性成本核算,除传统QALY 指标外,需额外测算长期并发症处理成本(如假体松动后的翻修费用)、患者生活质量改善带来的社会收益(如重返工作岗位的收入贡献)。对于可吸收性心脏支架,可跟踪5 年数据,核算避免二次手术的成本节约与材料吸收过程中的监测费用。对于诊断类医疗器械,可采用CEA 并辅以误诊成本测算,效果指标可聚焦漏诊率、误诊率降低幅度,成本端需包含因误诊或延误治疗导致的后续治疗费用增加。例如,对于某款新型肿瘤早筛设备,评价时需计算“每减少1 例漏诊所避免的晚期治疗费用(平均30 万元/ 例)”,以此衡量其成本效益。
2.3.3 构建覆盖创新医疗器械全生命周期的分阶段评价方法
针对创新医疗器械“研发- 上市- 迭代- 退市”的不同阶段特性,分阶段进行评价,实现经济价值持续校准。企业在研发阶段可基于疾病发病人数、现有疗法成本等数据,评价创新医疗器械的潜在市场规模和显著临床应用价值。在产品上市初期,可评价短期临床效果与直接成本。上市后1~3 年内,可开展调价评价,医保相关部门可基于真实世界数据(如使用量、并发症发生率、医保支出)测算ICER 值,若ICER 值低于某一设定阈值,可维持或适度上调价格;反之,可协商降价或调整支付比例。在产品迭代或淘汰阶段(如上市3 年以上),可对迭代产品开展增量评价,仅测算升级部分的成本效益,如AI 医疗器械的算法升级、植入类医疗器械的材料改进等。对于临床应用价值下降的产品,应开展退出评价,评估其退出市场对医保支出、患者治疗的影响,制定有序退出方案。
2.3.4 强化创新医疗器械经济学评价的数据、标准与人才支撑
高质量的经济学评价依赖于完善的数据支持。目前,我国医疗器械相关数据存在分散和不完整的问题,影响评价的科学性和准确性。建议加强数据基础设施建设,保障评价数据质量和可用性。可依托国家药品监督管理局、国家医疗保障局等信息平台,整合产品注册、临床使用和医保支付等多源数据,建设覆盖产品全生命周期的真实世界数据库。同时,可制定统一的证据提交标准,明确生产企业在产品注册及医保申报时提交临床及经济学证据的必要性和具体规范,并推动第三方专业机构参与数据和证据整合、审核与管理,确保评价过程的透明和公正。此外,锻造专业化人才队伍,可提供技术支持与智库服务。目前,我国经济学评价相关领域复合型人才缺口较大,特别是在经济学模型、医疗器械技术及临床应用交叉领域人才储备不足。建议监管部门联合高校、研究机构和企业等多方力量,打造一支具备跨学科知识和实践经验的专业人才队伍,聚集多学科专家力量,从而为监管决策提供持续、科学、权威的技术支持和政策建言。

第一作者简介
卢忠,硕士,中国药品监督管理研究会医疗器械监管研究专业委员会副主任委员/ 研究员。专业方向:医疗器械监管科学
通讯作者简介
方宇,博士,西安交通大学药学院,西安交通大学药品安全与政策研究中心,国际药物经济学与结果研究学会(ISPOR)中国西北分中心,副院长/ 教授。专业方向:卫生经济学评价

【参考文献】略




编辑:向丽
审核:赵燕宜

