半年实现临床突破与商业落地,麦科奥特冲刺18A多肽第一股

1
临床管线全线提速:四大核心产品里程碑密集落地,全球首创差异化价值持续验证
临床进展始终是创新药企的核心生命线,也是药渡衡量创新药企成长潜力的核心指标。药渡盘点发现,聚焦心脑血管与代谢类重大疾病领域,麦科奥特在两次递表的半年间隔期内,四大核心临床管线均实现里程碑式突破,无论是患者入组进度还是临床数据表现,均充分彰显了其全球首创产品的差异化竞争优势。
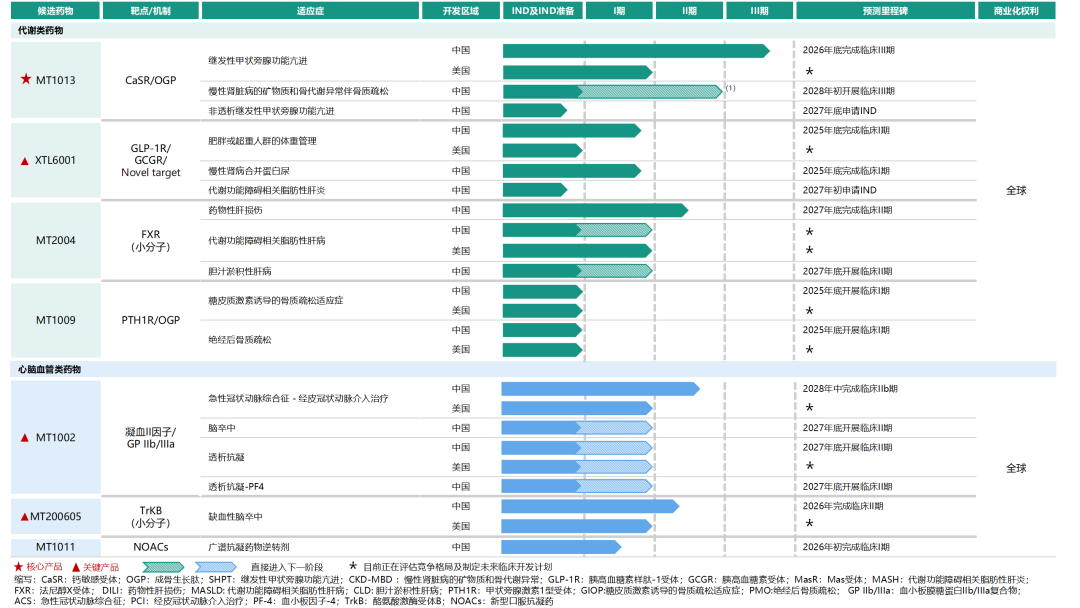
图1. 麦科奥特产品管线,来源:公司官网
核心产品MT1013(继发性甲状旁腺功能亢进症,SHPT)迎来注册临床关键节点
作为全球首创的CaSR/OGP双靶点受体激动剂多肽药物,MT1013 在麦科奥特首次递表时(2025年9月底),注册III期临床完成首例患者入组;截至 2026 年 3 月底,该产品中国关键注册 III 期临床试验已完成方案设定的全部 424 例患者入组,临床推进速度超预期,为 2026 年底完成 III 期研究、后续 NDA 申报奠定了核心基础。
继MT1013美国肾脏病学会(ASN)“Late-Breaking” 最新突破成果后不久,在2026年3月31日,日本横滨召开的世界肾脏病大会(WCN)上,MT1013与依特卡肽头对头II期关键研究(MT1013-II-C03)完整数据以壁报形式向全球肾脏病学界正式公布(壁报编号:WCN26-AB-7392)。研究结果显示,MT1013在综合达标率(血钙、血磷、iPTH)及心血管风险关键指标FGF-23的改善方面均显著优于已上市最优拟钙剂依特卡肽,同时展现出良好的安全性与耐受性。
图1. MT1013与依特卡肽头对头II期关键研究壁报数据
本次发布的MT1013-II-C03研究结果提示,相较于依特卡肽,MT1013实现了更优的:
综合达标率显著提升:钙、磷、iPTH三项综合达标率(39.29%与34.48%)是依特卡肽组(15.63%)的约2.2至2.5倍。
潜在心血管保护获益:MT1013两组FGF-23降幅(−33.5%与−39.9%)均优于依特卡肽组(−22.8%)。已有研究表明,FGF-23降幅>30%与心血管死亡风险降低34%、猝死风险降低43%直接相关(Moe et al., Circulation, 2015)。
良好的安全性与耐受性:MT1013症状性低钙血症发生率(7.69%)低于依特卡肽组(12.125%)。依特卡肽主要解决“抑制 PTH“的单点问题,而 MT1013 通过“调控代谢 + 促骨生成”双通路,从源头修复 CKD-MBD 的代谢紊乱,实现了从“控制病情”到“主动修复”的治疗理念升级。
缺血性脑卒中领域核心产品MT200605完成关键临床入组
该产品为具备激活 TrkB 受体与高效清除氧自由基双重协同机制的创新神经保护剂,截至 2026 年 3 月 20 日,其 II 期临床研究已完成全部 360 例患者入组,预计 2026 年 6 月底获得完整临床数据,计划于 2026 年 12 月完成 III 期临床首例患者入组,有望为国内缺血性脑卒中患者带来全新的神经保护治疗方案。
抗凝抗栓管线MT1002临床边界持续拓展
作为全球首个凝血因子 II 和 GP IIb/IIIa 双靶点肽拮抗剂,MT1002 的 ACS-PCI 适应症国内 II 期临床试验顺利推进,III 期临床方案已启动与监管机构的前置沟通;同时,脑卒中与透析抗凝两大扩展适应症明确了临床推进节奏,预计于 2026 年 6-7 月完成 II 期临床首例患者入组,将全面覆盖国内 PCI 手术的广阔市场需求。
全球首创三靶点代谢管线XTL6001完成I期临床收官
作为全球首个在中美双双获批 IND 的 GLP-1R/GCGR/MasR 三靶点激动剂,XTL6001 肥胖及慢性肾病合并蛋白尿适应症中国 I 期研究已于 2026 年 3 月全面完成,即将启动 II 期临床,有望在千亿级肥胖与代谢病市场中实现差异化突围。
2
商业化布局里程碑突破:12.4亿BD合作落地,树立多肽领域商业化新标杆
药渡观察到,两次递表期间,麦科奥特实现了商业化布局从0到1的里程碑式跨越,成为2025-2026年多肽创新药赛道商业化落地的标杆案例。2026 年 2 月 4 日,公司基于 MT1013 的全球首创临床价值,与云顶新耀达成重磅商业化合作,成为本年度中国多肽创新药领域标志性 BD 交易。
根据合作协议,云顶新耀获得 MT1013 在中国及亚太区(日本除外)的独家商业化授权,麦科奥特持续持有国内 MAH 权益;本次合作首付款及近期里程碑金额高达 12.4 亿元,其中 2 亿元首付款已于 2026 年 2 月全额到账。药渡认为,此次合作不仅充分印证了 MT1013 的临床价值与商业化潜力,更借助云顶新耀在肾病领域成熟的商业化体系与渠道布局,为产品 2028 年初的上市商业化铺平了道路,同时为公司补充了充足的现金流,进一步夯实了其港股上市的估值基础。
3
资本加持与财务结构优化:充足现金流筑牢长期发展护城河
在 2025 年生物医药一级市场仍处于复苏周期的行业背景下,麦科奥特在首次递表前逆势完成 D 轮 2.355 亿元融资,成为 2025 年多肽创新药赛道的融资标杆。药渡数据统计显示,该轮融资规模达同期生物医药创新药行业平均单笔融资金额的 2 倍,占据 2025 年国内多肽新药领域全年融资总额的 25%,充分彰显了资本市场对公司核心管线价值与长期发展前景的高度认可。
截至 2025 年 12 月 31 日,公司账面货币资金与低风险理财产品合计在手资金达 2.7 亿元;叠加 2026 年 2 月 BD 合作到账的 2 亿元首付款,公司现金流储备充足,可完全覆盖后续核心管线临床 III 期推进、CMC 工艺开发、IPO 筹备等全环节资金需求。同时,公司持续加大核心研发投入,2025 年全年研发开支达 1.301 亿元,其中核心产品 MT1013 研发投入占比达 64.9%,为管线持续推进与技术创新提供了坚实保障。
4
全链条技术能力持续升级:CMC工艺迭代与平台突破,构建创新核心壁垒
药渡盘点发现,两次递表期间,麦科奥特在 CMC 工艺开发与核心技术平台升级方面持续突破,进一步完善了从药物发现、临床开发到商业化生产的全链条创新能力,构建起多肽创新药领域的核心技术护城河。
CMC工艺层面,公司完成核心产品 MT1013 规模化生产工艺迭代,实现产品收率大幅提升、生产成本显著下降,同时进一步优化了产品稳定性,为后续商业化生产与供应链保障奠定了坚实基础;同步完成 MT1002 工艺优化,确认最终工艺参数,可全面满足 III 期临床与商业化生产需求;XTL6001 上下游工艺与参数优化持续推进,充分适配后续临床阶段需求。
技术平台层面,公司依托双 / 多特异性肽技术平台、计算机辅助肽设计平台、口服肽递送平台、成药性评价平台四大核心技术体系持续深化创新能力:
计算机辅助肽设计平台完成多款新一代双 / 多特异性肽候选化合物的分子模拟与筛选,新增超 10 个高潜力候选靶点;
口服肽递送平台取得关键技术突破,完成 1 款候选药的成药性评价并获取 PCC 分子,为多肽药物口服化突破奠定了技术基础。
截至最新招股书披露日期,公司已拥有全球范围内35项已授权专利、17项在审专利申请,构建了完善的知识产权保护体系。
5
行业影响力持续跃升:学术与产业双重认可,巩固赛道龙头地位
凭借在多肽创新药领域的技术突破与行业贡献,麦科奥特在两次递表期间斩获多项重磅奖项与荣誉,行业龙头地位持续巩固。除 MT1013 斩获的 ASN 国际顶级学术认可外,公司先后获评 2025 中国生物医药创新企业 50 强、多肽药物领域标杆企业、2025 未来医疗 100 强、生命科技 VENTURE50、2025 中国医药健康明日之星等多项行业重磅荣誉,品牌影响力与行业认可度实现跨越式提升。
*声明:本文仅是介绍医药疾病领域研究进展或简述研究概况或分享医药相关讯息,并非也不会进行治疗或诊断方案推荐,也不对相关投资构成任何建议。内容如有疏漏,欢迎沟通指出!


中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市

*声明:本文仅是介绍医药疾病领域研究进展或简述研究概况或分享医药相关讯息,并非也不会进行治疗或诊断方案推荐,也不对相关投资构成任何建议。内容如有疏漏,欢迎沟通指出!


中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市



中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市



中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市



中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市


中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市


中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市

中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市
中国首个!这款1类创新核药正式获批上市
国内首个!这款国产长效HIV预防药物首次获批临床
信达生物这款ROS1抑制剂在澳门获批上市

