百济神州重磅新药,在国内获批上市!

4月10日,中国国家药品监督管理局(NMPA)最新公示,百济神州与安进公司联合开发的注射用塔拉妥单抗(Tarlatamab)已正式获批上市,用于治疗既往接受过至少2线治疗(含含铂化疗)失败的广泛期小细胞肺癌成人患者。这是国内首款获批的DLL3/CD3双特异性T细胞衔接器(BiTE®),标志着我国小细胞肺癌治疗正式迈入双抗免疫治疗新阶段。

截图来源:NMPA官网
01
全球上市不足两年,塔拉妥单抗国内获批提速
塔拉妥单抗是安进公司研发的一款靶向DLL3与CD3的双特异性抗体,属于BiTE®(双特异性T细胞衔接器)平台的重要成果。其通过同时结合肿瘤细胞表面的DLL3蛋白与T细胞表面的CD3蛋白,激活患者自身T细胞,特异性杀伤表达DLL3的肿瘤细胞,从而发挥抗肿瘤作用。
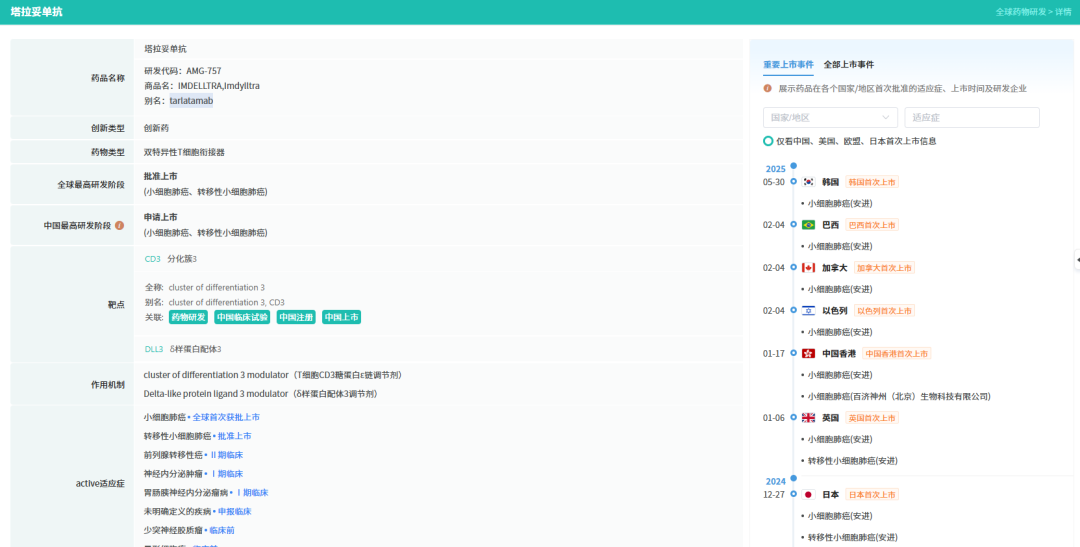
截图来源:全球药物研发数据库(更多点击小程序查看)
摩熵数据库显示,该药最早于2024年5月在美国获批上市,用于治疗含铂化疗失败的ES-SCLC成人患者;同年12月,该药在日本获批,而后于2025年度陆续在英国、加拿大等国家和地区获批上市。在国内,塔拉妥单抗的首个上市申请于2025年7月提交,并被纳入优先审评,今日终于正式获批。
从首次全球获批到国内上市,历时不足两年,体现了我国药品审评审批体系对重大临床需求创新药的支持力度,也凸显了该疗法在全球范围内公认的临床价值。
02
关键临床数据亮眼:ORR达40%,为中国患者带来明确获益
此次塔拉妥单抗国内获批,主要基于两项关键注册临床研究——全球多中心II期研究DeLLphi-301和中国桥接/IIa期研究DeLLphi-307的积极结果。
塔拉妥单抗研发现状
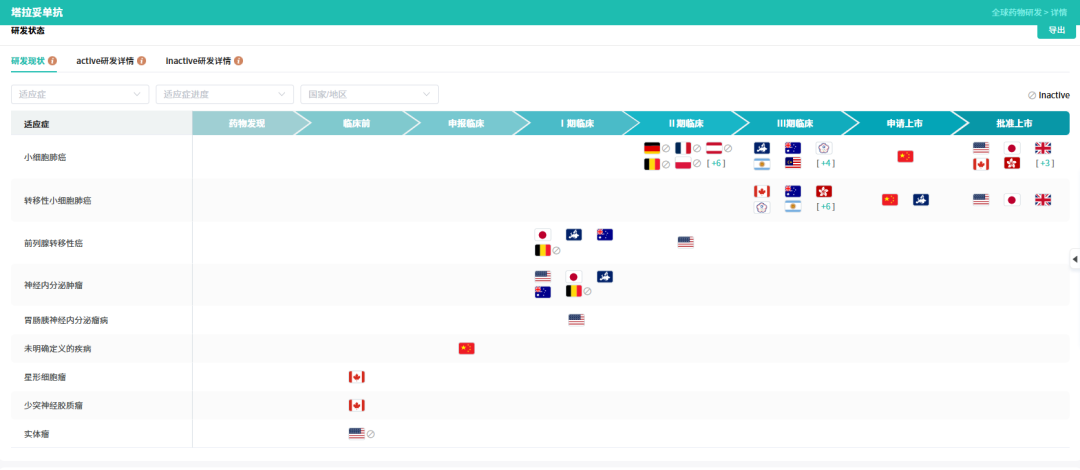
截图来源:全球药物研发数据库(更多点击小程序查看)
DeLLphi-301研究是一项开放性、全球多中心II期试验,旨在评估塔拉妥单抗治疗复发性/难治性小细胞肺癌的疗效与安全性。研究结果显示:客观缓解率(ORR)达40%(95% CI: 31, 51),意味着近半数既往多线治疗失败的患者可实现肿瘤显著缩小;中位缓解持续时间(DoR)达9.7个月(95% CI: 2.7, 20.7+),展现出持久的疗效。DeLLphi-307研究则专门针对中国患者开展,其疗效趋势与全球研究一致,证实了该疗法在中国人群中的有效性和适用性。
在安全性方面,塔拉妥单抗整体耐受性良好。最常见的不良反应为细胞因子释放综合征(CRS),多为1-2级,且多发生于首次给药后,可通过标准支持治疗进行管理。因不良反应导致永久停药的比例较低。
03
竞争格局:全球领跑,国产加速追赶
虽然塔拉妥单抗目前仍是全球唯一获批的DLL3/CD3双抗药物,但该赛道的热度正急剧升温。据摩熵数据库统计,全球已有10款针对该靶点的抗体药进入临床阶段(含获批临床及以上),其中5款为双抗。

截图来源:全球药物研发数据库(查数据.找摩熵)
除安进的塔拉妥单抗外,另有两款处于III期临床的重磅竞品紧随其后:一是勃林格殷格翰与中国生物制药合作的Obrixtamig,具备潜在Best‑in‑class潜力;二是泽璟制药与艾伯维共同开发的Alveltamig,正依托前者深厚的双抗技术积累快速推进。 SCLC后线治疗市场正从“独家垄断”迅速转向“群雄逐鹿”。
塔拉妥单抗的获批,对我国广泛期小细胞肺癌治疗具有里程碑意义。它不仅填补了SCLC后线靶向治疗的长期空白,更验证了BiTE®平台在实体瘤领域的巨大潜力。
随着更多DLL3靶点药物的推进,小细胞肺癌这一“难治”癌种,正迎来前所未有的精准治疗曙光。
END
本文为原创文章,转载请留言获取授权
近期更多摩熵咨询热门报告
识别下方二维码领取

联系我们,体验摩熵医药更多专业服务 | ||||
会议 合作 | 报告 定制 | 数据库 咨询 | 数据 定制 | 媒体 合作 |