海思科两款1类新药,国内斩获关键进展!

4月8日,CDE官网最新公示,海思科医药集团两款1类新药迎关键进展:其子公司沈阳海思科制药申报的1类创新药HSK46256片IND申请正式获受理,该产品为首次在国内申报临床。
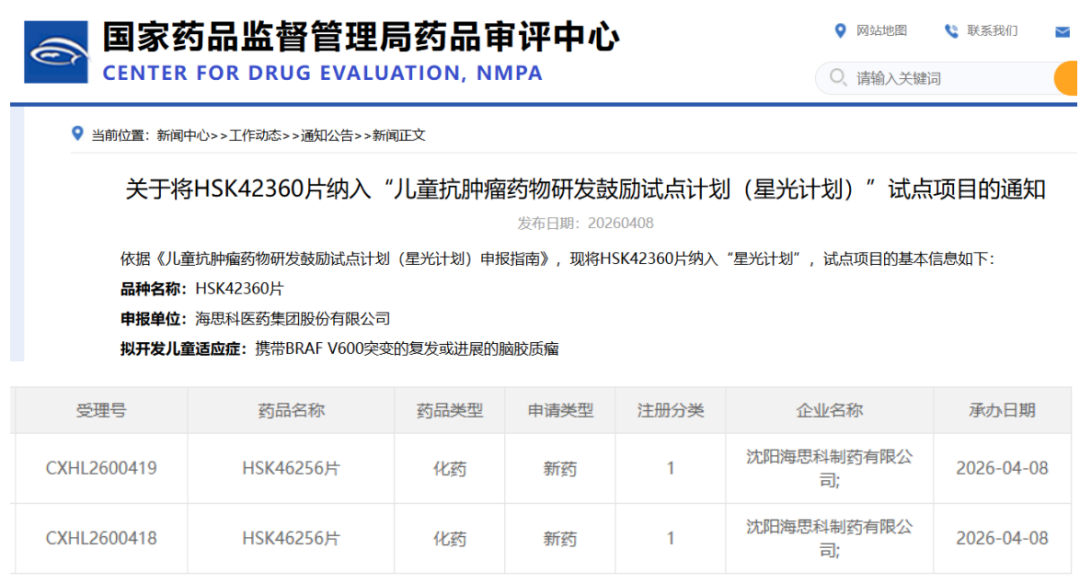
截图来源:CDE官网
同日,另一款1类新药HSK42360片被CDE纳入“星光计划”,旨在加速儿童抗肿瘤药物的研发进程。这一连串动作标志着海思科在创新药研发,尤其是肿瘤与儿童用药领域的布局正加速落地。
01
加速创新转型,HSK46256片首次冲击临床
HSK46256片是海思科自主研发的一款化学药品1类创新药,本次为首次在国内提交IND申请并获CDE受理,标志着该产品正式迈入临床开发阶段。
今年以来,海思科的创新药管线推进节奏明显加快。摩熵医药数据显示,2026年至今,海思科已有HSK46256片、HSK44459两款1类新药首次申报临床;此外,HSK-39297片为首次申请上市,而HSK-46575片、HSK-47388片两款1类新药则先后获批临床。这一系列进展显示出海思科正处于从“仿转创”向“创新驱动”跨越的关键窗口期。
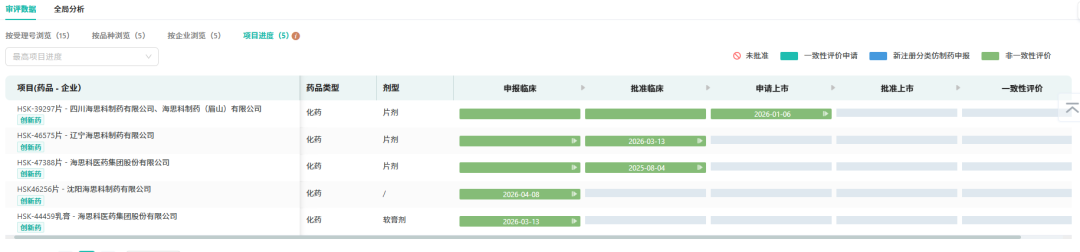
截图来源:中国药品审评数据库(更多点击小程序查看)
截至目前,海思科已有安瑞克芬注射液、考格列汀片、苯磺酸克利加巴林胶囊、环泊酚乳状注射液4款1类新药在国内成功获批上市,覆盖神经系统、消化系统及代谢两大治疗领域,为公司构建了稳定的创新药商业化梯队。
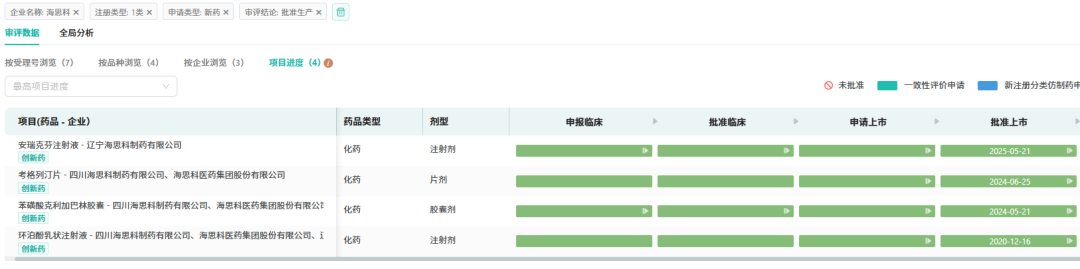
截图来源:中国药品审评数据库(更多点击小程序查看)
02
聚焦儿童肿瘤,HSK42360入选CDE“星光计划”
海思科另一款在研新药HSK42360片成功入选CDE“星光计划”。该计划旨在针对抗肿瘤药物儿童适应症研发过程中的技术难点提供前瞻性、针对性指导,从而显著提高儿童抗肿瘤药物的研发效率。HSK42360此次纳入计划的儿童适应症为:携带BRAF V600突变的复发或进展的脑胶质瘤。
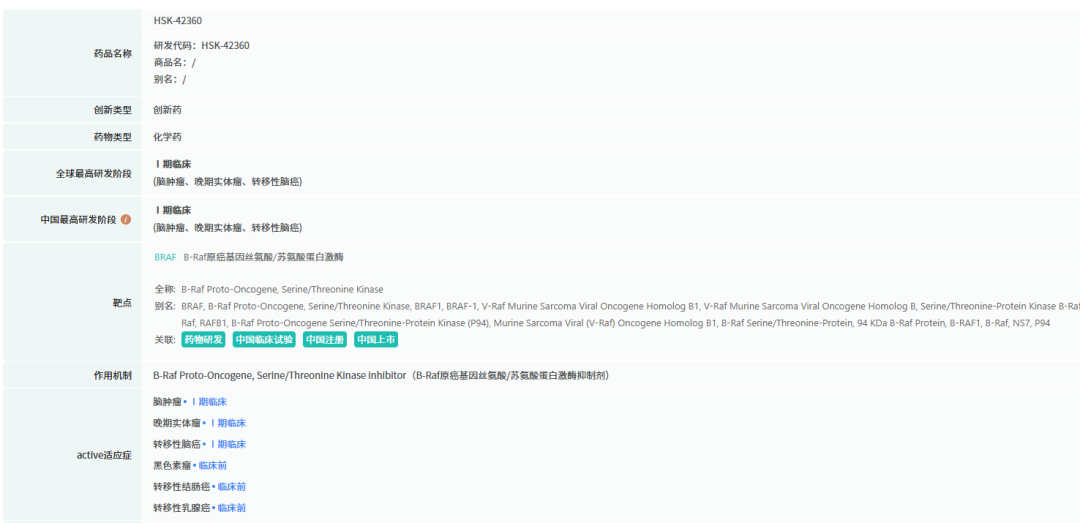
截图来源:全球药物研发数据库(更多点击小程序查看)
HSK42360是海思科自主研发的一款靶向BRAF V600突变且具有脑渗透性的小分子抑制剂,拟开发用于治疗BRAF V600突变晚期实体瘤。临床前研究显示,该药在多个BRAF V600突变的实体瘤药效模型中展现出极佳的抗肿瘤活性,同时表现出了良好的耐受性和较大的安全窗。2024年3月,HSK42360正式提交临床申请;6月11日,顺利获得首次临床批准;仅仅6天后,即6月17日,便迅速推进至晚期实体瘤Ⅰ期临床试验阶段,研发进程高效有序。
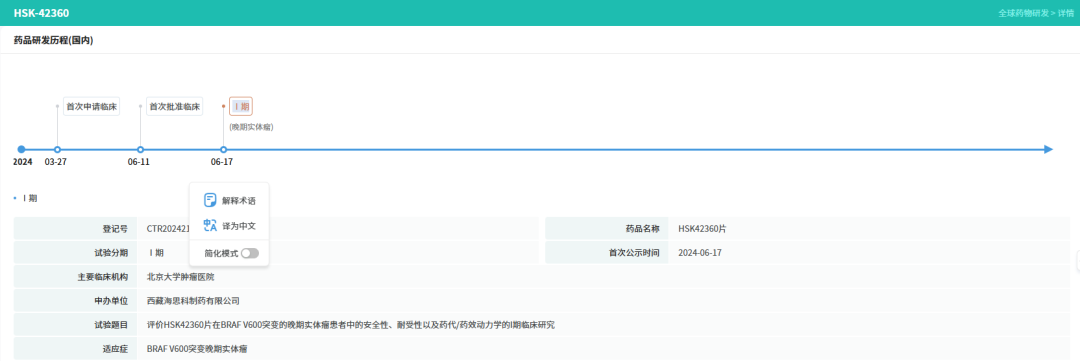
目前,HSK42360片正在同步开展两项Ⅰ期临床研究:一项针对成人实体瘤患者;一项专门针对6岁至18岁的儿童恶性脑肿瘤患者。
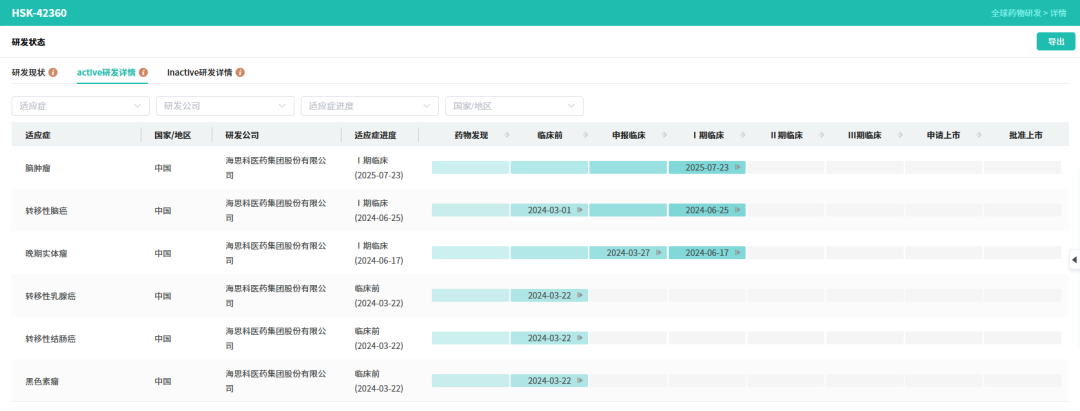 截图来源:全球药物研发数据库(更多点击小程序查看)
截图来源:全球药物研发数据库(更多点击小程序查看)
该药的成功入选,不仅体现了监管机构对其研发策略与临床潜力的认可,也为后续加速开发、解决儿童肿瘤患者的临床急需奠定了政策基础。
此次HSK46256片IND获受理、HSK42360片入选“星光计划”,不仅是海思科在肿瘤精准治疗与儿童罕见/难治性疾病领域的重要突破,也体现了其在小分子创新药研发与复杂临床设计能力上的持续进阶。随着多款1类新药陆续进入临床中后期及申报上市阶段,海思科有望在未来2–3年内迎来创新药管线的密集兑现期,进一步夯实其在国内创新型药企中的竞争地位。
END
本文为原创文章,转载请留言获取授权
近期更多摩熵咨询热门报告
识别下方二维码领取

联系我们,体验摩熵医药更多专业服务 | ||||
会议 合作 | 报告 定制 | 数据库 咨询 | 数据 定制 | 媒体 合作 |