约 500 项临床及超万篇研究,EVs/外泌体治疗 6 大疾病探索

2026 年 4 月 12 日
医麦客新闻 eMedClub News
据资料显示,截至目前,已有约 500 项临床试验登记,评估 EVs 相关策略的临床潜力,彰显其在生物医学领域的广阔前景。与此同时,有关 EVs/外泌体的发表文献数量快速增长,根据 PubMed 数据库统计,相关发表文献数量 2024 年已达到 9812 篇,截至 2025 年,已有近 10099 项相关研究被收录,呈现出近乎指数级的快速扩张趋势。
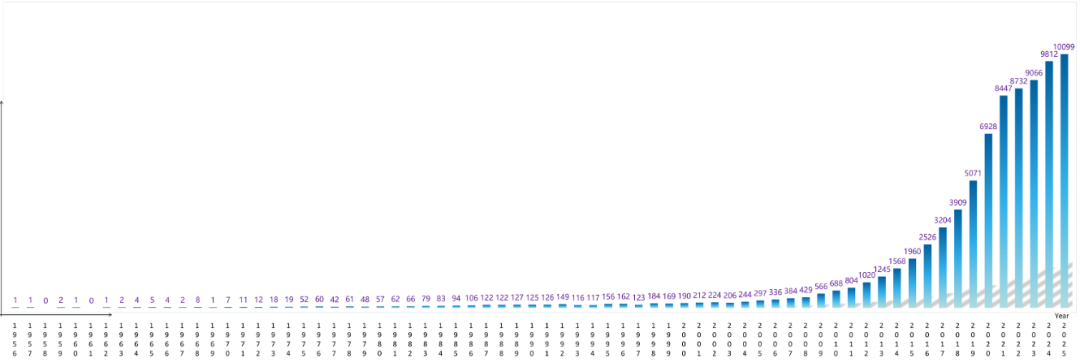
这一趋势表明,该领域研究已成为生物医学的重要研究热点。EVs/外泌体富含多种功能性生物活性物质,在诊断和治疗方面均具有显著潜力,当下随着科研与临床的深入发展,其已经被应用于多种疾病的治疗中。
肿瘤
肿瘤治疗的手段多样,EVs/外泌体在肿瘤治疗中主要发挥了其出色的递送功能。在化疗中,载阿霉素外泌体(Exo-Dox)可显著提升细胞摄取效率与抗肿瘤效果,并降低心脏毒性。Li 等人利用透明质酸(CD44 特异性配体)修饰牛乳外泌体,将阿霉素特异性递送至 CD44 高表达的肿瘤细胞,同时也尝试了泛癌抑癌分子 miR-204-5p,可高效诱导 CD44 阳性肿瘤细胞死亡。另外,EVs/外泌体还展现出独特的血脑屏障穿透能力和逆转化疗耐药潜力。
在靶向治疗中,Kim 等人首次报道肿瘤来源细胞外囊泡可作为 CRISPR-Cas9 的递送平台用于肿瘤基因编辑。多项临床前研究显示,EVs/外泌体可作为反义寡核苷酸(ASO)、siRNA、miRNA、mRNA、circRNA、lncRNA 等核酸药物的递送工具。值得一提的是,CAR-T 来源外泌体在抗肿瘤治疗中同样展现出潜力。
心血管疾病
在动脉粥样硬化疾病中,内皮祖细胞(EPC)来源的 EVs/外泌体已被证明能够调控动脉粥样硬化的进展,如抗炎 M2 型巨噬细胞来源 EVs/外泌体可减轻斑块内炎症与改善造血异常,血小板膜融合的 M2 巨噬细胞来源 EVs/外泌体靶向性更强,可有效缓解动脉粥样硬化进展。

心肌缺血、损伤和梗死是由于心肌血液供应与氧气需求失衡引起的不同类型的心肌组织损伤。研究显示,心肌梗死(MI)患者体内血小板、内皮细胞与白细胞来源 EVs/外泌体水平升高,其可以保护心肌免受缺血再灌注损伤,如缺氧诱导的间充质干细胞来源 EVs/外泌体通过 miR-125b 抑制心肌细胞凋亡,促进缺血性心脏修复。
EVs/外泌体在心肌肥厚与心力衰竭中介导心肌细胞与成纤维细胞之间的交互作用。在病理状态下,成纤维细胞来源 EVs/外泌体可将 miR-21 与 miR-27a 转运至心肌细胞,促进心肌肥厚。相反,携带 miR-185-5p、miR-143/145 簇等 miRNA 的干细胞来源 EVs/外泌体可下调心肌肥厚相关基因表达,发挥保护作用。
目前该领域研究多集中于将循环 EVs/外泌体 miRNA 表达谱的变化作为心肌肥厚与心衰的潜在标志物。探索 EVs/外泌体及其 miRNA 在治疗中的应用仍处于早期阶段,是未来重要研究方向。
代谢性疾病
有研究表明,EVs/外泌体在脂质代谢调控中至关重要,具备肥胖治疗潜力。经脂肪干细胞衍生的 EVs/外泌体处理的 M2 巨噬细胞高表达酪氨酸羟化酶,进而促进脂肪干细胞增殖与乳酸生成,推动白色脂肪组织褐变并改善代谢稳态。与肥胖相关的 EV miRNA,如 miR-122、miR-192 和 miR-27a-3p 等可以作为肥胖治疗的靶点。
在糖尿病中,EVs/外泌体可作为糖尿病早期检测与病情监测的可靠无创生物标志物。除诊断应用外,EVs/外泌体还可主动调控代谢通路。囊泡内包裹的部分 miRNA、蛋白质与脂质可影响葡萄糖稳态相关关键信号通路,改善胰岛 β 细胞功能与外周组织胰岛素敏感性。间充质干细胞衍生的 EVs/外泌体可减轻全身炎症、降低氧化应激并促进胰岛再生,具备治疗潜力。
衰老与神经退行性疾病
来自年轻血浆或细胞的 EVs/外泌体可通过改善线粒体功能、减轻氧化应激、逆转细胞衰老实现衰老组织年轻化。间充质干细胞来源的 EVs/外泌体在减轻氧化损伤、促进组织修复、延长早衰小鼠健康寿命方面潜力突出。未来研究可聚焦优化年轻或工程化细胞来源的治疗性 EVs/外泌体。
神经退行性疾病是一类以中枢神经系统内异常蛋白聚集和进行性神经元丢失为特征的疾病,其治疗药物受到血脑屏障的阻碍,而 EVs/外泌体可跨越血脑屏障,是治疗分子的理想载体。
多项研究已经证实了 EVs/外泌体在阿尔茨海默病(AD)中的治疗潜力,如骨髓间充质干细胞来源的 EVs/外泌体可通过改善 BDNF 相关神经病理缓解 AD 模型小鼠认知衰退。Yu 等人构建狂犬病病毒糖蛋白(RVG)肽修饰的工程化外泌体(RVG-EXO),装载脑啡肽酶变体靶向脑海马区α7-nAChR,可降低脑部促炎标志物(IL-1α、TNF-α)并提高抗炎因子 IL-10,为 AD 提供新型治疗策略。
在帕金森病(PD)中,EVs/外泌体既可以作为生物标志物,也可以作为治疗工具。Liu 等人开发以未成熟树突状细胞来源 RVG 修饰外泌体包裹的核-壳杂化纳米系统(REXO-C/ANP/S),递送靶向 α-突触核蛋白的 siRNA,可高效清除 α-突触核蛋白聚集并降低 PD 神经元毒性。另外,将生物相容性较低的治疗药物包裹于 EVs/外泌体已成为 PD 治疗的重要研究方向。例如,载多巴胺的血液来源 EVs/外泌体可显著提升纹状体与黑质多巴胺分布,相较于游离多巴胺在 PD 模型中疗效更强、全身毒性更低。
创伤医学
EVs/外泌体在再生医学中备受关注,可促进伤口、骨、软骨、半月板、脊髓、肌腱与肌纤维修复。
伤口愈合是复杂临床难题,涵盖感染性、糖尿病性、烧伤等多种创面。该过程需要细胞、生长因子、细胞外基质、神经纤维与血管协同作用。间充质干细胞在皮肤再生修复中发挥关键作用,参与伤口愈合从炎症到组织重建的全部阶段,间充质干细胞来源的 EVs/外泌体可发挥类似作用。此外,M2 巨噬细胞衍生的 EVs/外泌体可诱导 M1 向 M2 表型转化,通过促进血管生成、再上皮化与胶原沉积加速愈合。其他干细胞类型(如脂肪干细胞)来源的 EVs/外泌体同样在伤口愈合中展现潜力。
在骨再生过程中,骨髓间充质干细胞来源的 EVs/外泌体的水凝胶被用于颅骨缺损修复;在半月板损伤修复中,EVs/外泌体可通过促进半月板细胞迁移、细胞外基质合成与抑制炎症反应,促进半月板再生;在脊髓损伤修复中,神经干细胞与间充质干细胞来源 EVs/外泌体可携带神经保护分子(miRNA、生长因子、抗凋亡蛋白)促进轴突生长并防止神经元死亡,自体血浆来源的 EVs/外泌体被用于靶向递送促生长肽,促进脊髓损伤后恢复。
感染性疾病
EVs/外泌体与病毒感染及机体免疫密切相关。多项基于 EVs/外泌体的策略被用于抵抗 HIV、新冠病毒(SARS-CoV-2)、乙肝病毒(HBV)等感染,如装载 Cas9/gRNA 并经水疱性口炎病毒糖蛋白(VSV-G)修饰的 EVs/外泌体可显著增强 Cas9 蛋白内体逃逸并提升受体细胞基因编辑活性,有效降低 HBV 复制与感染细胞中的病毒抗原及共价闭合环状 DNA(cccDNA)水平。
在细菌感染中,研究人员开发了可同时靶向结核肉芽肿与胞内结核分枝杆菌的工程化囊泡纳米颗粒,在结核小鼠模型中,疗效优于一线抗生素。在真菌感染中,真菌来源外泌体一方面可以促进感染和传播,另一方面也可以调控真菌生长、刺激宿主适应性免疫发挥保护作用,在临床诊疗与疾病预防中具有前景。
责任编辑丨浔
校对丨浔
参考资料:
1.Li Q, Ding Y, Shi Y, Qiu C, Lei L, Li S, Zhu Z, Zheng J, Qin C, Wang K, Jiang C, Han Z, Yang L, Zhang L, Li P, Tong L, Wang D, Xu H, Dai B, Du Y, Wang K, Fan Z, Wang W, Guo K, Huang Y, Wang X, Sui B, Wen L, Chen F, Feng D, Qin X, Mao W, Liu H, Liu C, Li Z, Wang Y, Huang R, Lu R, Zhang Y, Tian Y, Miao X, Yin Y, Zhang J, Wang Z, Ma T, Dong H, Wei D, Yang Z, Yang X, Cheng X, Chrzanowski W, Chang Z, Zhang X, Cho WC, Luo Y, Xia W, Huang Z. 80 years of extracellular vesicles: from discovery to clinical translation. Extracell Vesicles Circ Nucleic Acids. 2026;7:165-233.
精彩活动
长按识别二维码立即参与↓
推荐 1
4 月 16 日 19:00-20:30
2026 核酸药物爆发启示,开发、药效机制研究与爆发的底层逻辑


点点“分享”、“点赞”和“在看”
给我充点儿电吧~