破局“先天不足”:阿斯利康奥拉帕尼的制剂升维之战
发布时间:2026-04-12来源:药事纵横
本文旨在深入剖析全球首个上市的PARP抑制剂——奥拉帕尼(Olaparib)的制剂改良历程。奥拉帕尼作为一种典型的生物药剂学分类系统(BCS)IV类药物,其低溶解度和低渗透性的固有特性为口服制剂的开发带来了巨大挑战。本文将从药物的分子特征、理化性质、生物药剂学性质及DMPK特点出发,系统阐述其最初上市的胶囊剂型所面临的临床局限性,特别是严重的“药丸负担”(pill burden)问题。在此基础上,本文将详细解析阿斯利康公司(AstraZeneca)如何通过制剂创新,开发出新一代片剂,并深入探讨这一剂型变更背后的科学逻辑、所采用的关键技术(如无定形固体分散体技术)以及最终实现的临床获益,包括降低服药剂量、显著减少每日服药数量、提升患者依从性并维持等效的药物暴露。本文将以代表性上市产品Lynparza®的演进为例,全面呈现奥拉帕尼从“难成药”分子到优化给药方案的成功转化之路,为现代药物制剂开发提供一个经典的案例研究。第一部分:奥拉帕尼的理化与生物药剂学特性:制剂挑战的根源
为了理解奥拉帕尼制剂改良的必要性和逻辑,首先必须深入了解其作为活性药物成分(API)的内在属性。这些属性直接决定了其在体内的吸收过程,并构成了制剂开发的根本挑战。1.1分子结构与基本特征
奥拉帕尼的化学名称为4-[(3-{[4-(环丙烷羰基)哌嗪-1-基]羰基}-4-氟苯基)甲基]酞嗪-1(2H)-酮。其分子式为C24H23FN4O3,分子量约为434.46 g/mol。奥拉帕尼是一种白色至类白色的结晶性粉末,并且存在多种晶型,至少两种无水多晶型(Form A 和 Form L)和一种单水合物多晶型(Form H),这为制剂的稳定性和溶出一致性带来了额外的挑战。1.2关键理化性质:低溶解度的核心难题
奥拉帕尼的理化性质是其制剂开发困难的直接原因,其中最突出的便是其极低的水溶性。溶解度(Solubility):奥拉帕尼是一种难溶性药物。其在生理pH范围(pH 1.2至6.8)的水性介质中,溶解度表现出pH不依赖性,数值极低,约为0.1 mg/mL。具体实验数据显示,其在pH 1.2盐酸介质中溶解度为0.10-0.12 mg/mL,在pH 4.5醋酸缓冲液中为0.13 mg/mL,在pH 6.8磷酸缓冲液中为0.11 mg/mL。尽管在生物相关模拟肠液(FeSSIF)中,其溶解度可略微提升至0.2 mg/mL,但这仍远低于高剂量给药所需的要求。相比之下,它在有机溶剂如DMSO(可达33 mg/mL)和乙醇(1.7 mg/mL)中溶解性更好。表1在37˚C下,奥拉帕尼在生理pH范围内的水溶性(参考1)酸碱性:奥拉帕尼被定性为弱酸性化合物。其在胃肠道环境中,奥拉帕尼分子几乎完全以非解离的中性形式存在,其溶解度基本不随pH变化而改变。亲脂性(Lipophilicity):奥拉帕尼具有中等亲脂性。实验测定的其在pH 7.4下的辛醇/水分配系数(Log D)为1.49。这一特性虽然有助于药物分子穿透细胞膜,但与其极低的水溶性相结合,使得药物难以从制剂中溶出并到达肠壁表面以供吸收。熔点:奥拉帕尼为结晶性粉末,属于难溶性药物。通过差示扫描量热法测定,其熔点(定义为起始温度)为199-206°C。奥拉帕尼为非手性分子。1.3生物药剂学分类(BCS):确认为IV类药物
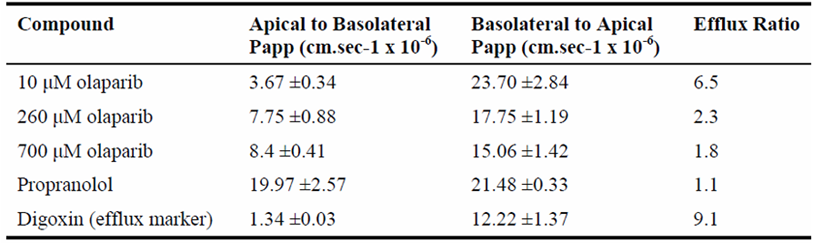
基于上述的低溶解度特性,结合其渗透性数据,奥拉帕尼被广泛归类为生物药剂学分类系统(BCS)IV类药物,即低溶解度、低渗透性。低渗透性方面,虽然有资料称其渗透性可能为“中等”,但多数监管文件和研究文献的共识是其渗透性较差。P-糖蛋白(P-gp)介导的主动外排作用可能也是其低渗透性的原因之一。表2奥拉帕利在Caco-2细胞模型中的渗透性;n=3(参考1)BCS IV类药物是口服制剂开发中最具挑战性的类型。它们的吸收同时受限于溶出速率和跨膜转运速率,导致口服生物利用度通常很低且个体差异大。这为奥拉帕尼的制剂开发定下了一个基调:必须采用先进的增溶技术来克服其“先天不足”。1.4药物代谢动力学(DMPK)概览
奥拉帕尼在人体内的DMPK特征进一步揭示了其成药性面临的挑战和制剂优化的方向。吸收(Absorption):口服后吸收迅速,达峰时间(Tmax)中位数约为1.5小时。高脂饮食会延迟Tmax,但对总吸收程度(AUC)影响不大。其绝对口服生物利用度数据有限,有报道称在35%至46%之间。分布(Distribution):奥拉帕尼具有较大的表观分布容积(Vd),约为158-167 L表明其在组织中有广泛分布。血浆蛋白结合率中等,约为82%。代谢(Metabolism):主要通过肝脏的细胞色素P450 3A4/5(CYP3A4/5)酶系进行代谢因此与强CYP3A抑制剂或诱导剂合用时存在显著的药物相互作用风险。排泄(Excretion):代谢产物及少量原形药物通过尿液(约44%)和粪便(约42%)排泄。其表观血浆清除率(CL)约为7.4 L/h 终末消除半衰期(t1/2)约为15小时。综上所述,奥拉帕尼的BCS IV类特性是其制剂开发的核心障碍。为了在每日高达数百毫克的治疗剂量下实现有效且稳定的血药浓度,必须通过先进的制剂技术来显著提高其溶出度和/或溶解速率,从而改善其口服生物利用度。第二部分:奥拉帕尼的制剂改良之路:从胶囊到片剂
奥拉帕尼的上市历程完美展示了如何通过制剂科学的进步来解决药物分子的内在缺陷,实现产品生命周期的优化。其演进主要经历了从初代胶囊到二代片剂的重大转变。2.1最初上市产品:Lynparza®胶囊剂
2014年12月,奥拉帕尼首次在美国获批上市,其商品名为Lynparza®,剂型为硬胶囊。该胶囊剂的规格为50mg。其批准的治疗剂量为每次400mg,每日两次(BID)。这意味着,患者每次服药需要吞服8粒胶囊,每日总共需要服用16粒胶囊。为了应对奥拉帕尼极低的溶解度,最初的胶囊配方采用了一种基于脂质的增溶策略。文献显示,该胶囊使用了脂质辅料Gelucire™ 44/14(月桂酰聚氧乙二醇甘油酯)作为载体,将微粉化的奥拉帕尼制成固体分散体,以改善药物在胃肠道中的润湿和溶解。这是一种相对传统的增溶手段。尽管该胶囊剂成功将奥拉帕尼推向市场,但其临床应用中很快暴露了严重缺陷,核心问题就是 “药丸负担”(Pill Burden)。要求癌症患者每日吞服多达16粒胶囊,这极大地影响了患者的用药依从性、生活质量和长期治疗的意愿。对于正在接受化疗、可能伴有恶心、呕吐或吞咽困难的患者而言,这一负担尤为沉重。因此,开发一种更便捷的给药方式成为迫在眉睫的需求。2.2制剂迭代:Lynparza®片剂
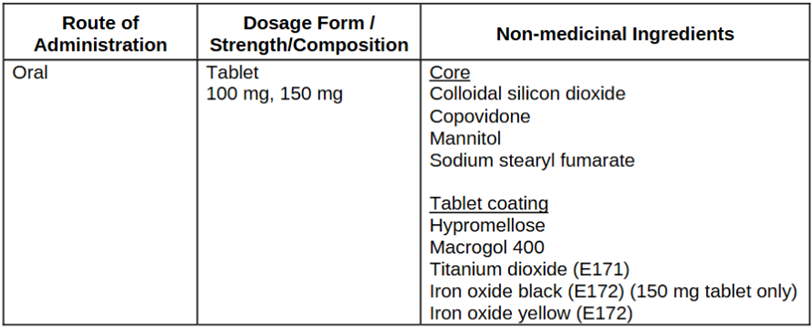
为解决胶囊剂的“药丸负担”问题并进一步优化药物的药代动力学特性,阿斯利康开发了新一代的Lynparza®片剂。该片剂于2017年获得FDA批准。变更的驱动因素与逻辑: 制剂变更的目标非常明确:显著降低药丸负担:这是最核心的驱动力。通过提高单片药物的载药量和生物利用度,减少每日服药的总片数。提高生物利用度并降低变异性:采用更先进的增溶技术,旨在比初代胶囊更有效地提高药物的溶出度和吸收,从而可能在更低的剂量下达到同等的治疗暴露,同时减少患者间的药代动力学差异。简化给药方案: 提升患者便利性,例如减少与食物同服的限制等。新制剂的特点与优势,片剂提供了100mg和150mg两种规格。新的推荐剂量调整为每次300mg(2片150mg),每日两次(BID)。这一变更使得患者的每日服药量从16粒胶囊锐减至4片药片,极大地改善了患者的用药体验和依从性。2.3两种剂型的药代动力学比较
从胶囊到片剂的转变不仅仅是物理形态的改变,更是一次基于药代动力学优化的精准升级。生物利用度差异: 由于采用了更优的增溶技术,片剂的口服生物利用度高于胶囊剂。一项研究显示,片剂的相对暴露量(AUC)比胶囊高出约13%。剂量调整与暴露匹配:正因为生物利用度的不同,片剂和胶囊在同等毫克数下不可互换。开发团队通过严谨的临床桥接研究,确定了300mg的片剂剂量。群体药代动力学模型分析证实,每日两次300mg片剂的稳态药物暴露水平(AUC)与原先每日两次400mg胶囊的暴露水平基本相当。这意味着,通过制剂技术的革新,在达到同样疗效的同时,每日总给药剂量从800mg降低到了600mg。表3在癌症患者中观察到的典型稳态PK参数对比(参考4)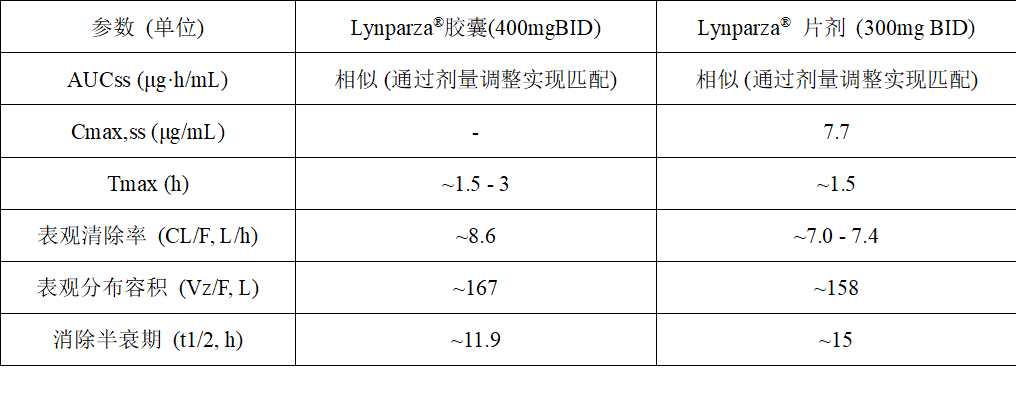 注意:由于生物利用度(F)不同,表观清除率(CL/F)和表观分布容积(Vz/F)在两种剂型间不具直接可比性。但总体趋势表明,片剂实现了更高效的吸收。最终,由于片剂的巨大优势,阿斯利康已于2018年8月在美国市场停止销售Lynparza®胶囊剂,完成了产品的全面升级换代。在中国市场,奥拉帕尼获批上市的剂型直接就是片剂,胶囊剂从未在中国上市。
注意:由于生物利用度(F)不同,表观清除率(CL/F)和表观分布容积(Vz/F)在两种剂型间不具直接可比性。但总体趋势表明,片剂实现了更高效的吸收。最终,由于片剂的巨大优势,阿斯利康已于2018年8月在美国市场停止销售Lynparza®胶囊剂,完成了产品的全面升级换代。在中国市场,奥拉帕尼获批上市的剂型直接就是片剂,胶囊剂从未在中国上市。第三部分:代表性上市产品与未来展望
3.1代表性上市产品
奥拉帕尼的代表性上市产品就是由阿斯利康(AstraZeneca)和默沙东(Merck & Co.)联合开发的Lynparza®。该产品经历了以下演进:Lynparza®胶囊 (Capsules): 规格50mg,为第一代上市产品,现已在主要市场(如美国)退市。Lynparza®片剂 (Tablets): 规格100mg和150mg,为目前全球市场的主流产品,也是在中国获批上市的唯一剂型。它代表了奥拉帕尼制剂改良的成功硕果。3.2后续制剂研发方向
尽管Lynparza®片剂已经取得了巨大成功,但针对奥拉帕尼这种BCS IV类药物的制剂研究并未停止。这主要由两方面驱动:仿制药开发和寻求进一步优化的可能性。这些研究主要集中在:新型固体分散体:探索使用不同类型、不同比例的新型聚合物载体和添加剂,以获得稳定性更好、溶出度更高、或具有自主知识产权的ASD配方。这是仿制药企试图规避原研专利的主要路径。脂质基系统(Lipid-based Systems):虽然初代胶囊已应用了简单的脂质辅料,但更复杂的自乳化/微乳化给药系统(SEDDS/SMEDDS)等仍在探索中,旨在进一步提高药物在肠道中的溶解度和吸收。纳米技术(Nanotechnology):如将药物制成纳米晶(Nanocrystals)或载入纳米粒通过大幅增加药物的比表面积来提高溶出速率。尽管这方面的商业化应用尚不明确,但它仍是提高BCS IV类药物口服生物利用度的前沿策略之一。目前,这些后续研发尚未产生新的、超越现有Lynparza®片剂的上市产品。它们更多地体现了制剂科学领域的持续创新和激烈的市场竞争。结论
奥拉帕尼的演进,是一部针对分子“先天缺陷”的精准改良史。从首代胶囊的“妥协”到二代片剂的“优化”,其核心驱动力是对其BCS IV类属性(低溶解、低渗透)的深刻认知与技术创新。这场变革的胜利,并非源于药粉形式的简单改变,而是依托于无定形固体分散体等先进技术对生物利用度的根本性提升。此举实现了“一箭双雕”:在将患者日服药量从16粒锐减至4片、极大改善依从性的同时,竟奇迹般地降低了每日给药总量(800mg → 600mg),并确保了疗效的等效。奥拉帕尼的成功向我们揭示:对于现代药物开发而言,一个分子的终点并非其获批上市之时。制剂科学,正是将一个有潜力的“候选者”锤炼为一款患者友好、价值最大化的“卓越产品”的关键锻造术。它的故事,为所有面对难溶性药物的研发者,点亮了一盏明灯。参考资料
1.https://www.accessdata.fda.gov/drugsatfda_docs/nda/2014/206162Orig1s000ClinPharmR.pdf2.https://data.epo.org/publication-server/rest/v1.0/publicationdates/20231011/patents/EP4257119NWA1/document.pdf3.https://pdf.hres.ca/dpd_pm/00045160.PDF4.https://ec.europa.eu/health/documents/community-register/2018/20180508140545/anx_140545_en.pdf
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。