Science:重新认识实体瘤靶点——CD70
发布时间:2026-03-31来源:bioart
嵌合抗原受体
(
CAR
)
是能够重新定向免疫效应细胞的特异性并增强其功能的人工合成受体。目前,靶向
CD
19
的
CAR
-
T
细胞已经革新了
B
细胞恶性肿瘤的治疗,在某些情况下甚至能使其他难治性疾病获得持久的完全缓解。然而,
CAR
-
T
细胞在实体瘤中尚未取得类似的疗效,这主要是受限于实体瘤中尚未发现具有类似特性的、在正常组织中表达受限的泛癌细胞表面靶点。因此,实体瘤的有效靶向受到两方面因素的制约:一是肿瘤抗原的异质性表达,这限制了
CAR
-
T
的疗效;二是靶点在正常组织中的表达,这就导致不能使用强效
T
细胞,为了避免不可接受的毒性。目前,实体瘤中普遍缺乏有效、通用的
CAR
靶点。
CD70
是肿瘤坏死因子超家族的成员,也是
CD27
的配体,因其在多种实体瘤中异常上调,而在生理条件下仅表达于部分活化的免疫细胞,因此成为一个有吸引力的
CAR
靶点。
CD70
在
70%
至
80%
的肾透明细胞癌和卵巢癌以及
25%
的胰腺癌中高表达,使其成为针对多种癌症的极具价值的靶点。
然而,
CD70
在肿瘤中的表达通常是异质性的,一些肿瘤细胞高表达,而另一些
(通常占肿瘤细胞的大多数)
则表现为低表达或不表达。
因此
,使用靶向
CD70
的
CAR T
细胞治疗晚期肾透明细胞癌患者所获得的临床反应一直很有限。
近
日
,
来自
哥伦比亚
大学
的
Michel Sadelain
团队
在
Science
杂
志上发表文章
Sensitive CAR T cells redefine
targetable CD70 expression in
solid tumors
,
发现肿瘤中
CD
70
的异质性表达受到表观遗传调控,表达水平在单个细胞中从高到极低不等,因此通过常规检测方法可能显示为阴性。利用一种高灵敏度的
CD
70
受体——即共表达共刺激分子
CD
80
和
4
-1
BBL
的
HLA
非依赖性
T
细胞受体,可有效清除能够逃逸常规
CAR
-
T
细胞攻击的
CD
70
异质性肿瘤
。
这项研究为治疗多种实体瘤提供了一种潜在策略。

研究人员
首先利用两名多重治疗耐药的患者建立了两种肾透明细胞癌患者来源的异种移植模型,通过将肿瘤原位植入肾被膜下建立肾癌模型,通过静脉注射建立肺癌模型。这两种异种移植物均在培养中表达
CD
70
,并被表达
CD
70
特异性
CAR
的
T
细胞裂解。但在动物模型中,即使是非常高的
CAR
T
细胞剂量
也未能根除肿瘤。
当联合肺和肾模型,使小鼠在两个部位都长有肿瘤时,
CD70-CAR T
细胞在肺部引发快速的肿瘤清除,但在肾部位未能如此。用高斯荧光素酶标记的
CD70-CAR T
细胞在肺部和荷瘤肾脏中均可检测到,这表明
CD70-CAR T
细胞并非无法到达肾肿瘤。与肾部位相比,肺部的肿瘤细胞表现出强烈的
CD70
表达,提示
CAR-T
细胞失败的原因是
CD70
的表达水平,而非其无法迁移到肾部位。
对治疗后的肾肿瘤进行
CD
70
抗原谱分析显示,
CD
70
阳性的肿瘤被清除,但低表达或阴性的部分仍然存在。但进一步提高
CD
70
检测能力显示,表观
CD
70
阴性的肿瘤细胞仍然存在极低水平的
CD
70
。那么,如果使用更灵敏的
CAR
设计,例如
HLA
非依赖性
T
细胞受体,是否可以检测并清除具有低水平
CD
70
的肿瘤细胞?体内治疗显示,与
CD
70-
CAR
T
细胞相比,
CD
70-
HIT
T
细胞能够显著改善肿瘤清除能力。当在
CD
70-
HIT
中共表达
CD
80
和
4
-1
BBL
时,其能够实现完全且持久的肿瘤清除
,而在
CD
70-
CAR
中表达
CD
80
和
4
-1
BBL
或仅表达
4
-1
BBL
都不能增强肿瘤清除效果。
将
CD70
野生型
PDX
肿瘤与
25%
的
CD70
敲除肿瘤混合,
CD70-HIT+CD80/4-1BBL T
细胞并未能根除肿瘤,这表明其体内疗效并非由于对
CD70
阴性肿瘤细胞的旁观者杀伤,而是需要肿瘤细胞表达
CD70
。
随后,研究人员对
CD
70
的表达如何被沉默至极低水平进行分析,
发现
EZH2
介导的
CD70 H3K27me3
表观遗传沉默与肾透明细胞癌中极低但可被
HIT
靶向的
CD70
表达水平相关。
同时在
异质性肾透明细胞癌
原发患者样本中也观察到,
表观
CD70
阴
性的肿瘤细胞中存在由染色质可及性预测的低水平
CD70
表达
,这表示其可能对
HIT
疗法敏感。为了预测
HIT
疗法可能出现的毒副作用,
使用
CD
70
染色质可及性对正常组织的
CD
70
表达水平进行评估。结果发现,
除活化的免疫细胞
(在激活后获得
CD70
表达)
外,
CD70
在大多数成人正常组织中基本不表达。与此一致的是,在细胞毒性试验和人源化小鼠模型中,
CD70-HIT T
细胞的毒性并未超过
CD70-CAR
或
CD19-CAR T
细胞,这进一步验证了染色质可及性预测的可靠性以及
CD70-HIT T
细胞的安全性。
CD
70
的异质性表达在包括卵巢癌和胰腺癌在内的其他实体瘤中,是否也存在保留低水平
CD
70
表达的现象?研究人员在卵巢癌和胰腺癌模型中测试了
CD
70-
HIT
T
细胞的疗效,能够实现完全的肿瘤清除。同时也存在
EZH2
介导的
H3K27me3
对
CD70
表达的抑制
,这支持
CD70-HIT+CD80/4-1BBL T
细胞可能对一系列广泛的、通过常规染色技术显示部分
CD70
阳性的实体瘤有效。
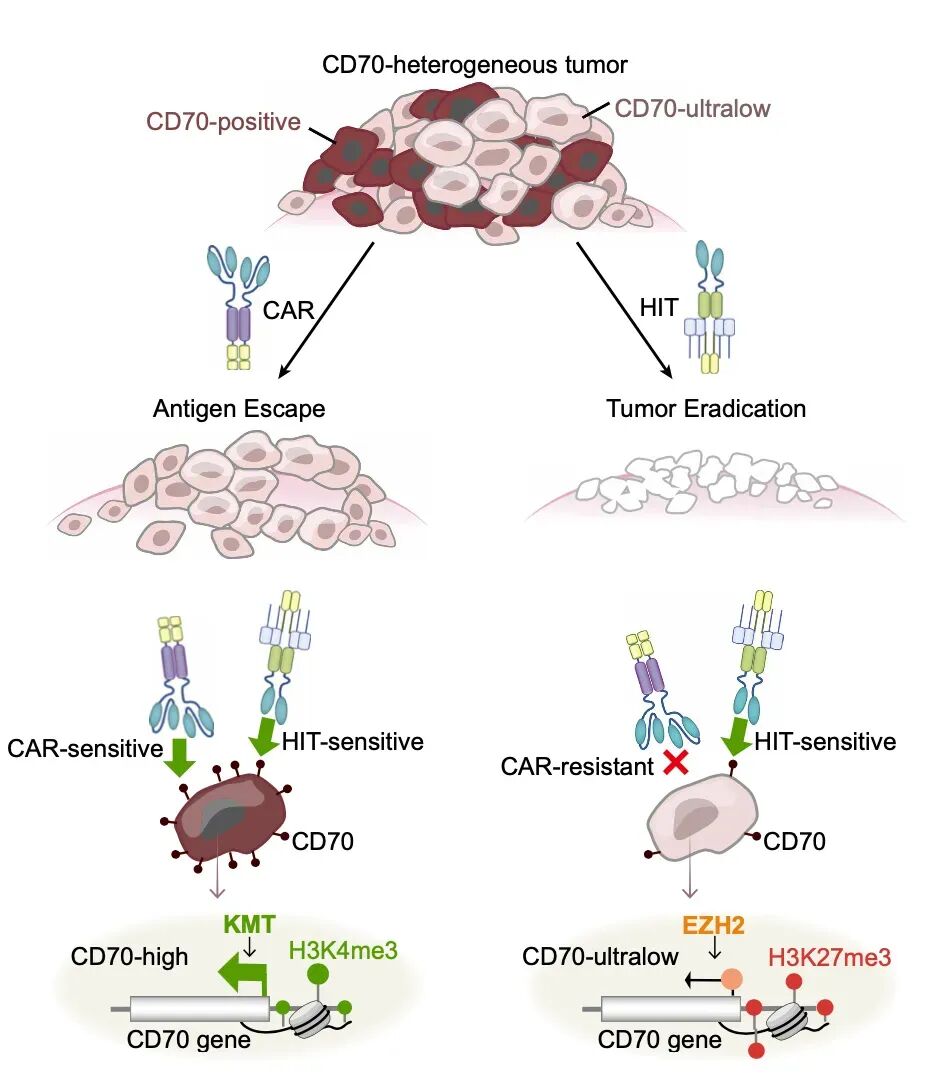
总的来说,
这项研究
揭示了
在
多种
CD70
异质性实体肿瘤中,
CD70
的表达是泛细胞性的——尽管部分细胞通过标准检测方法可能呈现为阴性。
使用高灵敏度的靶向受体
CD
70-
HIT
(同时共表达)可实现肿瘤的完全清除,为治疗多种实体瘤提供了一种潜在策略。
原文链接:
10.1126/science.adv7378
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。
