540亿美元开局!2026创新药出海Q1狂飙,“国际化”硬仗已开始
2025年,无疑是中国创新药BD出海授权交易的爆发元年,全年市场交易总额强势突破千亿美元,国产创新药正式走出国门、跻身全球医药创新舞台。
基于此,对2026年中国创新药BD出海授权交易的整体走势,多数业内人员早已给出乐观预判:认为行业增长势能将持续释放,出海交易有望从“数量爆发”转向“质量突围”,成为国产药企全球化布局的核心抓手。
立足当下,国内创新药出海模式逐步成熟,趋于完善,全球医药市场未被满足的临床需求缺口持续扩大,叠加国内药企研发技术不断实现突破性进展;更关键的是,海外药企对中国高性价比、高潜力创新药的需求,已经从以往的“可选补充”彻底转变为“战略刚需”。
多重利好因素共振之下,2026年中国创新药BD出海授权交易或迎来跨越式发展,2026年首个季度便交出远超市场预期的亮眼答卷,用硬核数据印证了行业高增长趋势。
Q1数据超越2024年全年水平
而针对上述利好预期,数据往往是最好的证明。
据药智数据显示,2026年第一季度(统计截至2026.3.24)中国创新药BD授权出海再次实现量价齐升:交易事件数、交易总额、首付款等核心指标均再次突破历史记录,创下行业新高。
具体而言,一季度国产创新药达成出海BD项目42项,同比增长10.53%;披露交易总金额达540.07亿美元,同比增长61.75%;披露交易首付款金额达6.79亿美元,同比增长321.85%。各项核心数据增速迅猛,直观展现出国产创新药出海的强劲爆发力。
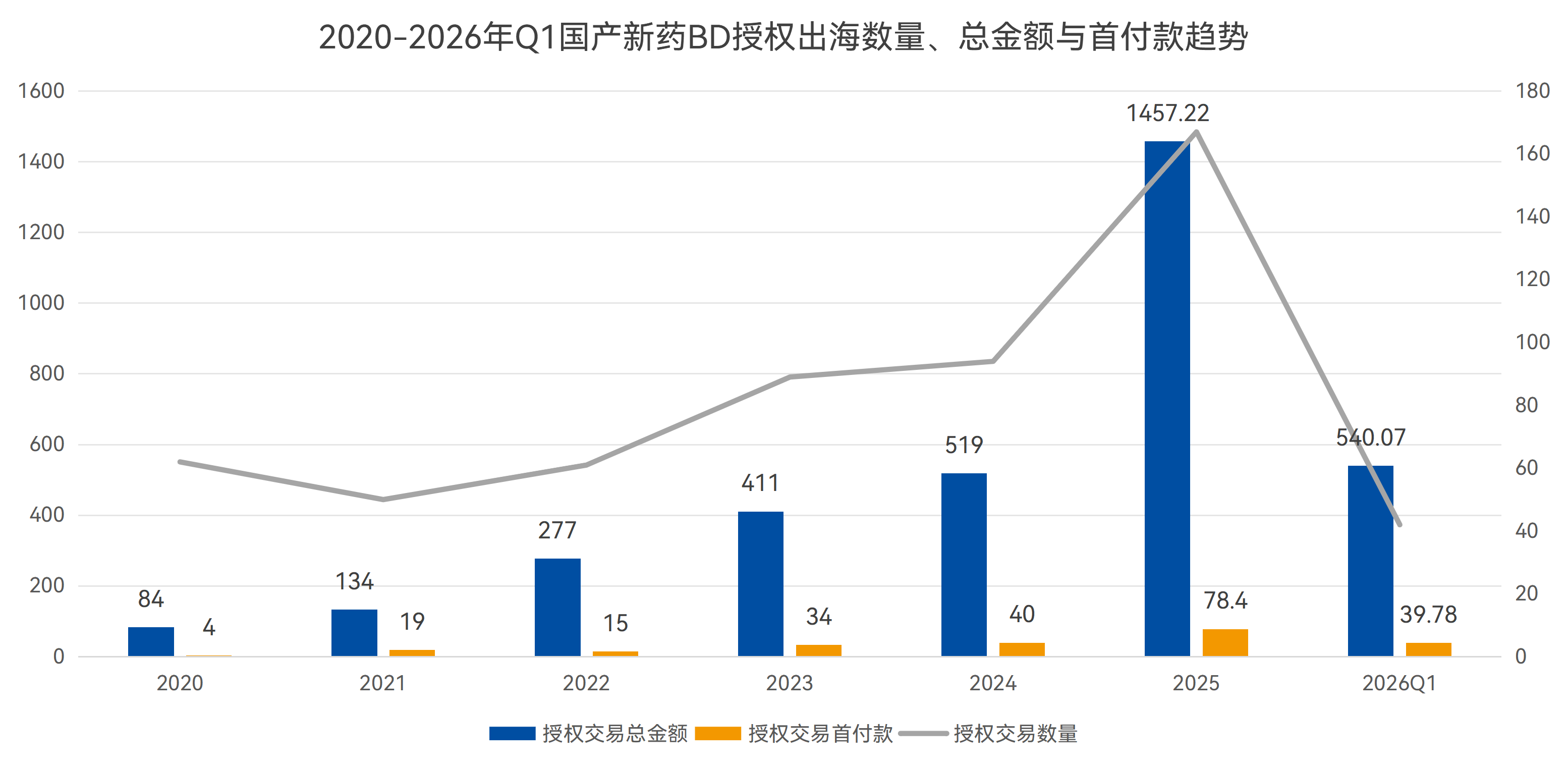
数据来源:药智数据(统计截至2026.3.24)
且更关键的是,Q1期间BD授权交易总金额与首付款金额规模,已与2024全年整体水平持平(上图所示),且已超越2025全年交易水平的六成。据目前的高速增长趋势推算,2026全年BD出海授权规模或将再创新高,全年交易总金额有望冲刺2000亿美元大关,突破国产创新药出海增长空间。
同时,2026年BD出海授权总金额与首付款规模再创新高的情况,却也并非依靠暴涨的出海项目数量堆砌而来。相反,2026年Q1的行业平均交易规模、最高交易规模均实现大幅提升(下图所示),单笔交易含金量持续走高,凸显了阶段出海项目整体质量的全面提升,告别了以往粗放式的数量增长。
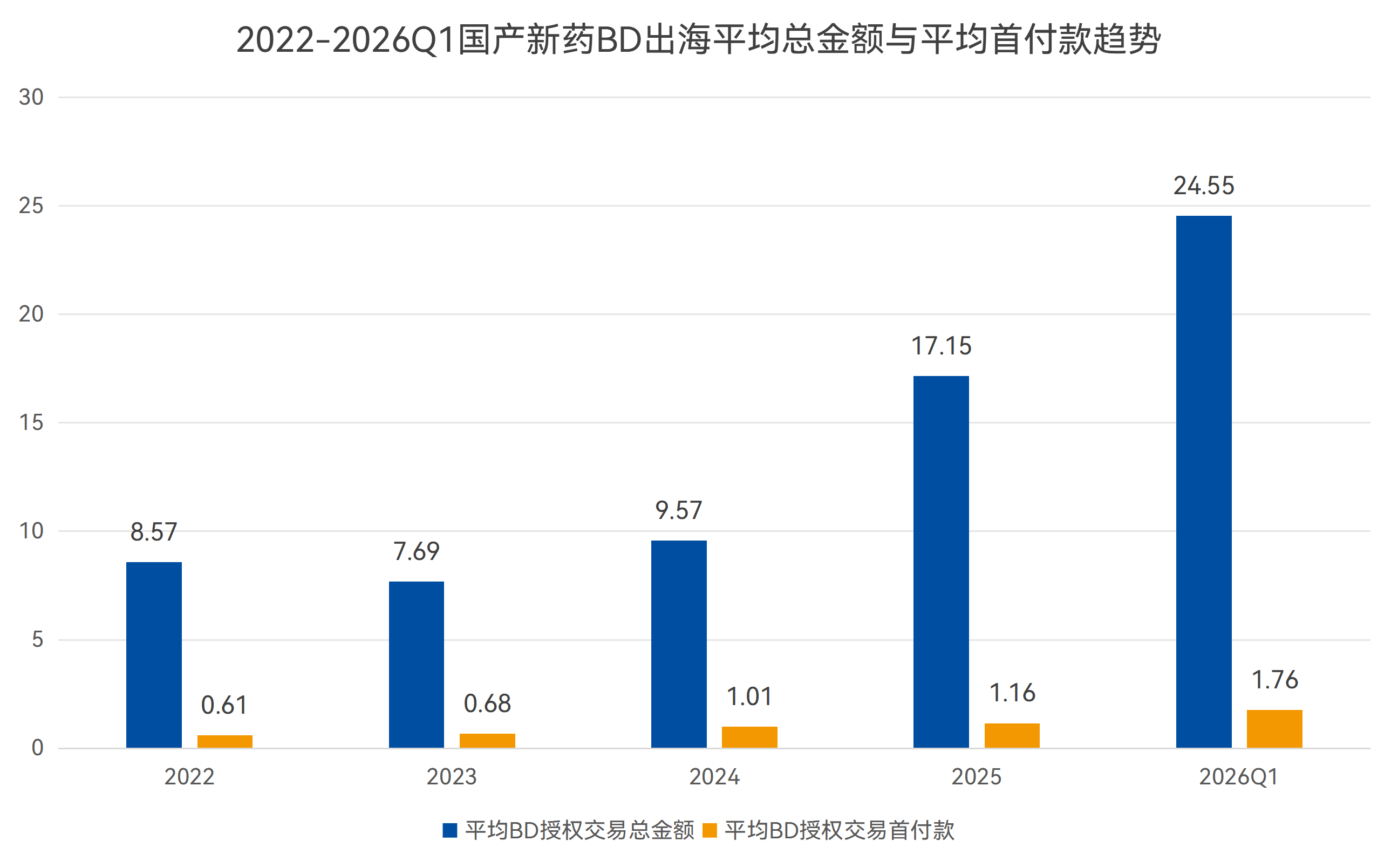
数据来源:药智数据
其中,2026年1月30日,石药集团与阿斯利康关于长效多肽药物开发的授权协议,以185亿美元的天价交易金额,登顶Q1季度出海交易总金额与首付款双榜首,更是直接刷新了中国生物医药对外授权金额最高纪录,成为国产创新药出海的标杆性事件。
业内人员分析表示:中国创新药目前正处在长周期增长的起点,本土药企持续不断地向全球输出优质创新资产。就目前跨国药企和海外PE机构主动接触中国医药资产的数量,以及行业对中国创新资产的兴趣增长趋势来看,未来BD出海交易持续高增长具备较高的可预见性,行业长期向好趋势明确。
赛道多元化趋势显著:前沿疗法优势更大
正常情况下,药企出海的底气归根结底,来源于硬核研发实力。这就意味着除企业自身管线推进能力差异外,GLP-1、PROTAC等全球热门赛道,以及双抗、ADC等国内 Biotech具备差异化优势的赛道,更容易获得海外药企认可,亦成为License-out谈判中的关键筹码。
2026年Q1,中国创新药在热门赛道多点开花,临床研发与国际全面接轨,为出海提供了坚实的技术保障。出海项目方面,除小分子与单抗等常规技术赛道外,小核酸、双抗、TCE三抗等前沿赛道BD较为热门;出海规模方面,RNA与小核酸在Q1季度分别完成了76.03亿美元与80.22亿美元的总金额。
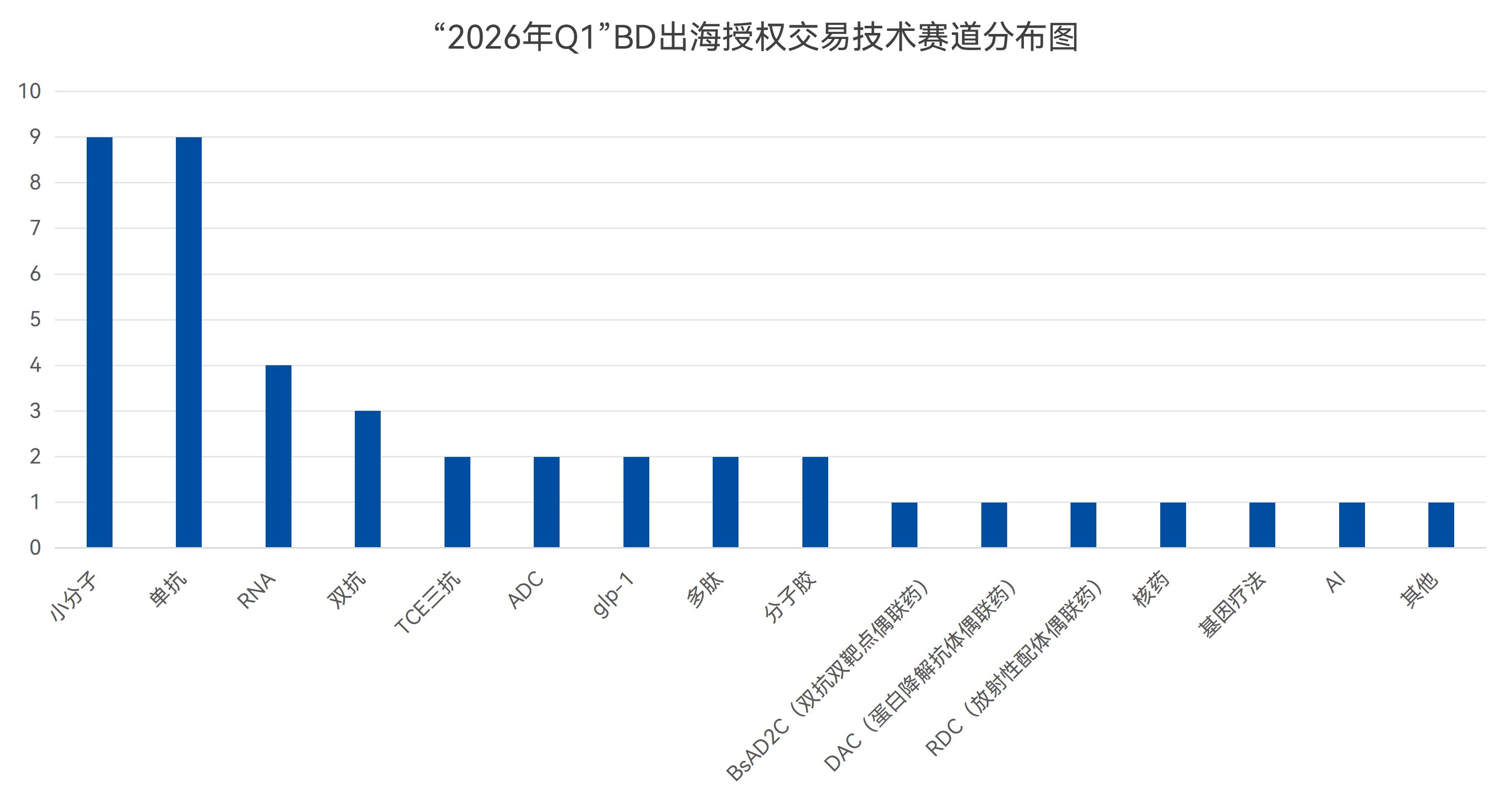
数据来源:药智数据
综上,双抗与小核酸无疑是2026年Q1最受海外市场青睐的BD赛道,也是本季度国产Biotech出海的核心主力。
① 双抗:中国药企全球领跑,PD-(L) 1/VEGF成战略资产
此前,中国创新药出海多集中于小分子、单抗、ADC等领域。但随着当下全球生物药市场从单抗时代逐渐迈入双抗时代,中国Biotech凭借差异化靶点布局抢占先机,逐步实现全球引领。
近年来,国内药企在双抗赛道实现跨越式突破,从早期产品引进、仿创结合,逐步走向源头创新,多款产品相继获批或进入全球临床后期。截至目前,全球临床Ⅲ期及注册申请阶段的在研双抗药物管线中,近7成来自中国药企。而2025年作为双抗出海“爆发年”,全年共完成了17个双抗项目成功出海,预计未来2–3年将迎来新一轮交易爆发期。
2026年Q1季度,国内共有3款双抗完成出海,分别为德琪医药的ATG-201、先声药业的SIM0709与荣昌生物RC148,三者合计交易总额达80.22亿美元(占比 14.85%),首付款合计7.59亿美元(占比19.07%)。
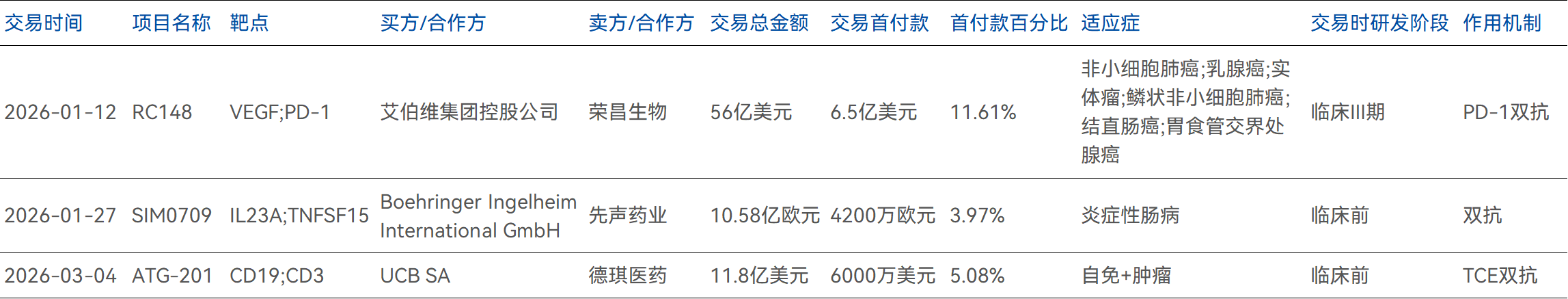
数据来源:药智数据(如有错误请指正,点击查看大图)
其中,荣昌生物与艾伯维56亿美元合作极具标志性意义,其所代表的PD-(L) 1/VEGF双抗赛道,已成为中国新药出海的经典范式。从2022年康方生物依沃西单抗,到2026年Q1荣昌生物RC148,PD-(L) 1/VEGF双抗已不再是区域性热点,而是全球肿瘤治疗领域的核心战略资产。
综合而言,作为肿瘤免疫治疗以及自免最热门方向之一,双抗药物已从概念验证步入商业化前夜,中国药企在这一赛道已占据主导地位。
② 小核酸:短期频现大额交易,中国创新价值获全球MNC认可
如果说,偶尔单一出海意义不大,那么同一赛道短期频现大额交易,或反映出某种行业趋势。
2026年Q1季度,国内已有三项小核酸(除miRNA)项目完成出海授权,合计授权金额已超越过去5年小核酸授权合作金额总和。
2月2日,圣因生物与罗氏旗下基因泰克达成全球研发合作与许可协议,圣因将一款基于其专有RNAi平台的药物全球独家开发和商业化权利授予基因泰克,获得2亿美元首付款,并有权收取后续最高15亿美元的开发和销售里程碑付款。
2月11日,瑞博生物与Madrigal达成全球独家许可协议,授权多款MASH领域单靶点及双靶点临床前siRNA资产的全球独家研发、生产与商业化权利,获得6000万美元首付款,潜在总金额最高可达44亿美元。
2月23日,前沿生物公告与GSK达成独家授权许可协议,将两款小核酸管线产品授予后者全球开发、生产及商业化,交易采用“首付款+里程碑付款+销售分成”的模式,首付款4000万美元,近期里程碑付款1300万美元,潜在总价值接近10亿美元。
更何况,上述三笔交易不仅发生时间密集,其交易对手分别是基因泰克、Madrigal和GSK这样的MNC药企,充分表明全球药企已高度认可中国小核酸资产的战略价值。
尽管,整体上看似中国小核酸产业起步较晚,与如Alnylam等海外头部企业仍存在不小技术差距,但也正因如此,国内企业得以绕开早期技术可行性验证阶段,在前人基础上集中资源聚焦递送系统优化、序列设计效率提升等关键环节突破。
中国小核酸药企深谙“弯道超车”的重要性,与其挑战Alnylam耗时十数年在小核酸罕见病领域建立的权威,不如直接布局国内患者基数更大的MASH、高血脂等千亿级慢病赛道,快速形成竞争力。
就目前数据而言,密集落地的出海合作标志着中国小核酸创新能力已获得全球认可。高金额、全球化BD交易持续落地,既为国内企业带来稳定现金流与国际化开发路径,也是推动中国小核酸产业从「技术追赶」迈向「全球创新价值链」的重要参与者。
出海模式升级:从“卖断”到“联姻”,绑定关系日趋紧密
早年间,国内新药出海的模式大多是传统授权模式,后来逐渐出现NewCo、Co-co等全新的模式,其意义被解读为彻底摆脱早期卖产品的单一模式,从一锤子买卖的简单授权,升级为风险共担、收益共享的全球联姻。
近年来,中国创新药出海模式正经历深刻的范式转型。长期主导的传统授权模式(License-out)已迎来迭代,NewCo(新设公司合作)与Co-co(共同开发)等新型模式的相继涌现标志着行业正从单纯的“产品交易”向“风险共担、收益共享”的深度战略绑定升级,彻底告别了早期“一锤子买卖”的粗放阶段。
但其实,在NewCo刚出现前几年,行业其实普遍持观望态度,核心顾虑源于三重不确定性:
估值虚高:NewCo核心资产大多处于临床前或早期临床阶段,缺乏实质性临床数据支撑,估值泡沫感强。
变现艰难:药企通常在合作中拿到的股权缺乏明确的退出路径,流动性风险高,最终能否兑现收益存疑。
落地风险大:海外运营团队的临床开发能力与本地化运营经验尚未经验证,项目推进的不确定性较大。
但随着2026年一季度NewCo模式迎来重大里程碑事件,即:康诺亚的NewCo被吉利德21.75亿美元收购(康诺亚股权变现共计3.2亿美元),使得NewCo模式从设立到退出的商业闭环彻底跑通,充分印证了该模式的可行性。

图片来源:康诺亚
与此同时,以和铂医药为代表的企业,也在一季度通过与Solstice Oncology就新一代CTLA-4抗体HBM4003达成合作,引入“首付款 +阶段性付款 + 股权”的组合模式。这类案例的频频落地,预示着多元化合作模式正逐步成为国产新药出海的主流迭代方向。
展望:出海易,国际化难,真正的壁垒在于全球化落地
尽管2026年一季度国产新药出海在项目数量与授权金额上再创新高,但行业仍需清醒地认识到:单纯的授权出海,不等于真正的国际化。
对于绝大多数药企而言,当前的BD授权多属于一次性或偶发性事件,难以构建可持续的稳定现金流循环,除非是具备平台化能力的Biotech。
无论是授权出海、NewCo、Co-co终究都只是药企创造海外营收的妥协手段,药企发展的最终目的仍将归于“国际化”三个字。而严格意义上来讲,再多出海授权达成的非经常性收入,其实都不能构成真正意义上的国际化。借用国际通行标准,一家国际化企业至少应满足“海外收入50%+、海外员工50%+以及全球化产品线”这三点关键条件。
而目前来看,阻挡国产药企国际化的最大障碍既不是海外收入,也不是海外员工,反而是全球化的产品搭建。以FDA获批上市为目标,其要求研发阶段必须有国际多中心临床试验数据,中国试验数据只能占整体数据的20%—40%,甚至更低。
中国生物制药首席执行长、执行董事谢承润表示,目前一款新药在国际上开展大三期临床实验,耗资或高达10亿美元,再加上创新药“十不存一”的成功率。国产药企若无200亿美元现金储备+10款大单品的国际多中心临床,“国际化”很难取得突破。
然而,资金只是表象。更深层的挑战在于国产药企的国际化魄力与战略定力。
过去数年间,虽有药企尝试在欧美布局研发中心、开展多中心临床,但由于临床失败风险极高,一次挫折往往消耗大量现金流,导致资本信心受挫。这种“由于缺乏对国产创新价值的坚定自信,从而在全球化战略上畏首畏尾”的心态,或是制约中国药企真正走向全球核心的关键瓶颈。
结 语
综上,2026年Q1中国创新药BD出海授权交易的亮眼成绩单,无疑为行业注入了一剂强心针。
一方面,BD授权交易出海交易总额、首付款金额等数据再创新高,甚至以一季度之力超越2024全年各项指标数据,预示着中国创新药目前仍处在长周期增长的起点,未来BD出海交易持续高增长具备较高的可预见性,行业长期向好趋势明确。
另一方面,除长期以来单抗、小分子等传统领域的零星出海外,当下多肽、双抗、小核酸等前沿疗法逐渐成为国产新药出海增量板块,预示国产新药逐渐成为全球创新价值链的重要组成。
更关键的是,从传统License-out到NewCo、Co-co等全新模式的阶段过渡初见成效,NewCo模式的成功闭环意味着国产新药彻底摆脱早期卖产品的单一模式,从一锤子买卖的简单授权,升级为风险共担、收益共享的全球联姻。
当然,正如数据背后所揭示的,真正的全球化远非一纸授权协议所能定义。当行业沉浸在交易额屡创新高的喜悦中时,我们更应清醒地认识到:BD出海只是“走出去”的第一步,能否真正“走进去”——融入全球医药创新生态、构建可持续的海外营收体系、打造经得起国际多中心临床检验的全球化产品线,才是决定中国药企能否从“出海”走向“入海”的关键。
若想实现从“授权依赖”到“自主国际化”的跨越,行业需要的不仅是资本的热捧与交易的狂欢,更需要在战略定力、全球化运营能力以及创新自信上的深层突破。唯有当越来越多的国产药企敢于投入百亿级资金开展国际多中心临床,勇于在欧美市场搭建本土化团队,善于在风险与收益间找到平衡点时,中国创新药才能真正告别“借船出海”的初级阶段,迎来“造船远航”的黄金时代。

责任编辑:惜姌
声明:本文系药智网转载内容,图片、文字版权归原作者所有,转载目的在于传递更多信息,并不代表本平台观点。如涉及作品内容、版权和其它问题,请在本平台留言,我们将在第一时间删除。
