Immunity:张维绮/刘光慧等构建免疫衰老时钟,发现T细胞年轻因子


编辑丨王多鱼
排版丨水成文
2026 年 4 月 14 日,国家生物信息中心张维绮研究组、中国科学院动物研究所刘光慧研究组、温州医科大学附属衢州医院张峰研究组、国家生物信息中心蒋岚研究组、国家生物信息中心杨运桂研究组与中国科学院动物研究所曲静研究组合作,在 Immunity 期刊发表了题为:Human immune aging clock identifies RUNX1 as a decelerator of T cell senescence 的研究论文。
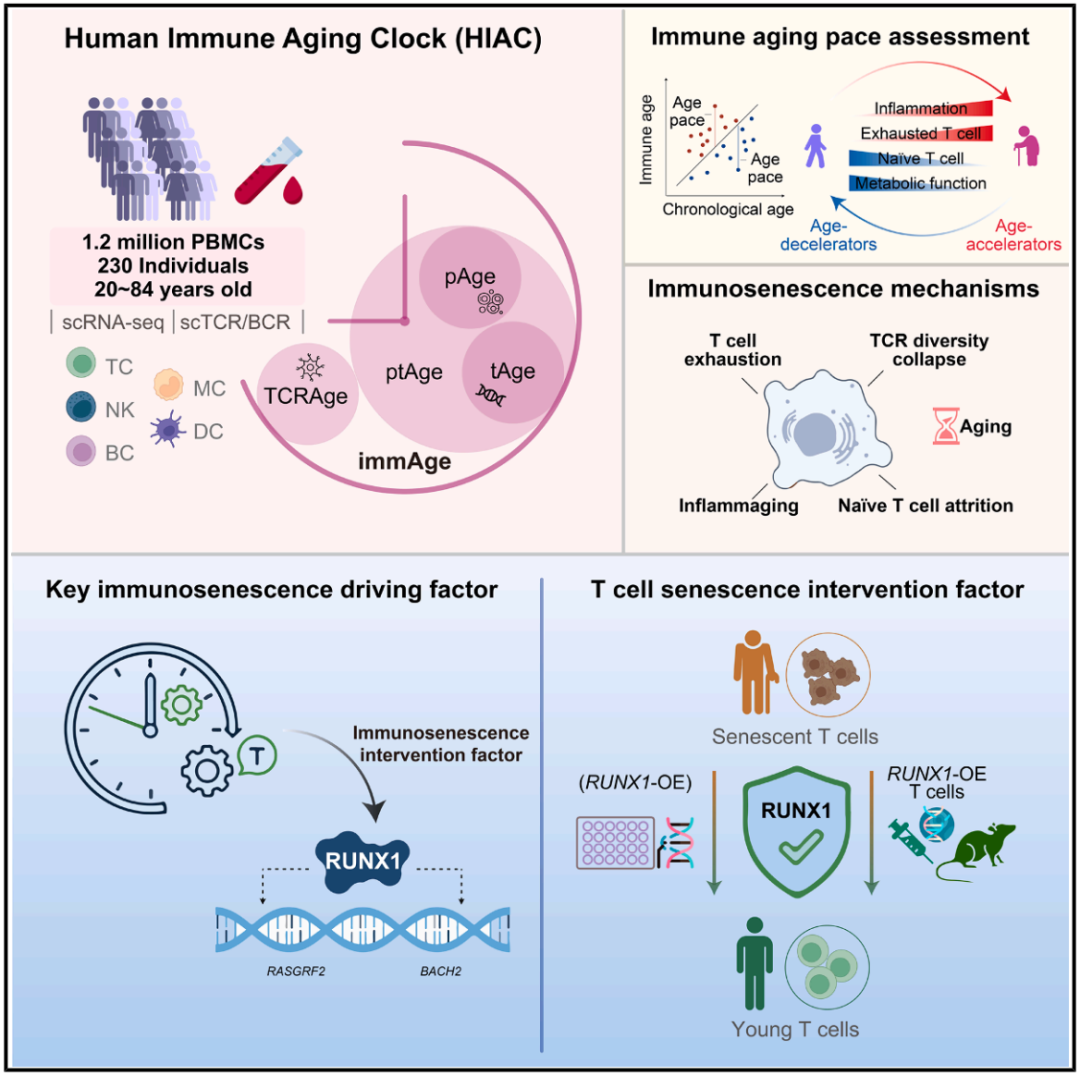
该研究构建了高精度人类免疫衰老时钟(Human immune aging clock,HIAC),系统解析了免疫衰老的多尺度动态变化,发现转录因子 RUNX1 是 T 细胞衰老的功能性“刹车”,并在人免疫细胞及人源化小鼠模型中证明,过表达 RUNX1 可逆转 T 细胞衰老。这项研究形成了从定量评估到因果干预的证据链,将免疫衰老研究推进至可量化、可建模、可靶向的阶段。

该研究的亮点:
该研究建立了一个全身生理健康相关的免疫衰老时钟;
T 细胞构成了衰老的枢纽,其各亚群中的 RUNX1 均在下降;
RUNX1 调控着一个促进年轻的基因网络以抑制 T 细胞衰老;
恢复 RUNX1 的功能可使衰老的人类 T 细胞返老还童。
HIAC:量化免疫衰老
传统免疫衰老评估,通常依赖单一生物标志物或批量转录组分析,难以捕捉免疫细胞亚群的特异性变化。为此,研究团队对 230 名年龄跨度超过 60 年(20-84 岁)的健康志愿者外周血样本进行了单细胞多组学分析,绘制了涵盖近 120 万个外周血单个核细胞的高分辨率图谱,并鉴定出 24 种免疫细胞亚型。结果显示,衰老引发免疫格局的深刻重塑:初始 T 细胞比例显著下降,而耗竭T细胞、单核细胞比例增加,呈现免疫衰竭与慢性炎症并存的特征。
在此基础上,研究团队构建了多层次免疫衰老时钟体系——包括基于细胞比例的 pAge、基于细胞类型特异性转录组的 tAge、基于 TCR 库特征的 TCRAge,以及整合上述信息的多模态复合时钟(immAge)。其中,immAge 预测年龄的平均绝对误差为 5.66 年,T 细胞相关时钟模型在所有细胞类型中表现最优。该结果在单细胞层面表明,T 细胞是外周免疫衰老敏感的指示细胞类型。
免疫年龄:从群体规律到个体画像
HIAC 进一步将免疫衰老评估从群体统计拓展至个体水平。研究团队定义了免疫衰老速率(immune aging pace)——即预测免疫年龄对实际年龄线性回归的残差,并据此将个体划分为“加速衰老者”(预测免疫年龄高于回归线的预期值)与“减速衰老者”(预测免疫年龄低于回归线的预期值)。结果显示,“减速衰老者”保留更多初始 T 细胞,转录组呈现较低的衰老和炎症信号,血浆中富含免疫调节或抗氧化代谢物,并表现出更优的血糖控制、肝功能及心肺储备能力。这些结果将免疫时钟与系统性健康状态直接关联,提示免疫年龄可能比日历年龄更早捕捉到器官功能的衰退信号。
此外,研究团队还在人类中定位了免疫衰老的关键重塑拐点—— 40 岁左右出现显著的细胞与转录组重塑高峰,提示该年龄段是免疫系统加速衰老的重要转折期,也是预防性干预的潜在窗口。
RUNX1:T 细胞衰老的刹车因子
通过基因调控网络分析,研究团队发现,转录因子 RUNX1 下游靶基因在免疫衰老时钟中权重最高。RUNX1 是一种 T 细胞年轻因子——其表达水平的维持有助于对抗 T 细胞衰老,过表达则可逆转衰老特征。RUNX1 蛋白水平在 CD4⁺ T 细胞和 CD8⁺ T 细胞中随年龄增长显著下降,且其在 CD4⁺ T 细胞中的降低与衰老标志物 γ-H2A.X 的积累呈负相关。功能实验证实,RUNX1 是 T 细胞衰老的关键调控因子:在年轻供体 T 细胞中敲除 RUNX1,可诱导细胞周期阻滞、衰老相关分泌表型(SASP)激活、CD8⁺ T 细胞端粒缩短以及细胞毒性功能下降;而在老年供体 T 细胞中过表达 RUNX1,则能逆转上述衰老特征——包括恢复共刺激分子 CD27 的表达(从而增强 T 细胞活化与记忆能力)、延长端粒。
在机制层面,RUNX1 在 CD8⁺ T 细胞中结合并激活一系列调控T细胞活化与免疫应答的关键基因,维持 T 细胞的年轻态转录特征。体内过继转移实验进一步验证了 RUNX1 在生理微环境中能够赋予 T 细胞抵抗衰老的能力。该研究使 RUNX1 成为经验证的可靶向人类 T 细胞衰老的内在调控因子。
综上,RUNX1 不仅是 T 细胞衰老的标志物,更是一种功能性的免疫细胞年轻因子,其表达水平的维持有助于对抗免疫衰老。该研究形成了从关联到因果再到干预的证据链,使 RUNX1 成为首个被验证的可靶向的人类 T 细胞衰老的内在调控因子。
转录因子重激活:赋能老年免疫治疗
该研究基于单细胞分辨率建立了人类免疫衰老时钟,从细胞组成、转录调控、免疫组库等多维度精准量化免疫衰老,并锁定了 T 细胞为免疫衰老的核心驱动群体。在此基础上,研究团队鉴定出转录因子 RUNX1 作为可靶向的 T 细胞衰老调控因子,提出“转录因子重激活”延缓免疫衰老的新策略。这一成果将免疫衰老转化为一个可量化、可干预的系统性生物学框架,为开发针对老年人群免疫功能衰退的干预手段奠定了理论基础,尤其为提升 CAR-T 等 T 细胞免疫疗法在老年患者中的持久性提供了潜在优化路径。
未来,围绕 RUNX1 在不同免疫细胞类型、不同衰老相关疾病中的精细调控机制,及其与其他衰老通路的交互作用,仍需深入探索。作为被验证的人类 T 细胞年轻因子,RUNX1 将为实现健康老龄化提供科学路径,并推动免疫增龄干预走向临床转化。
论文链接:
https://doi.org/10.1016/j.immuni.2026.02.007




点在看,传递你的品味




