科研人必看!免疫组化IHC实验常用固定剂配方集锦
在免疫组织化学(IHC)实验中,科研人可能会把主要精力投入到抗体选择、抗原修复和显色系统优化上,而忽略一个关键的操作步骤:固定。固定并不仅仅是“把组织泡起来”的简单操作,而是需要精心设计、严格把控的实验艺术。固定需要在分子层面“冻结”生命活动的瞬间,保持细胞形态的完整性,并保留抗原的免疫反应性。
蛋白质的物理、化学性质迥异,对应的固定方法和固定液的反应也不尽相同。
本文 将系统梳理IHC常用固定液配方及其配制步骤,为实验者提供一份可信赖的技术参考。
一、甲醛类固定液:经典中的经典
10%中性缓冲福尔马林(NBF)和4%多聚甲醛(PFA)依然是当今IHC实验中应用广泛的固定液。其固定机制在于与蛋白质中的氨基、羟基等基团形成交联,稳定组织结构。
10%中性缓冲福尔马林 配制较简单,常规配方如下:

4%多聚甲醛(PFA) 根据实验目的和使用场景不同,有两种配制方法。
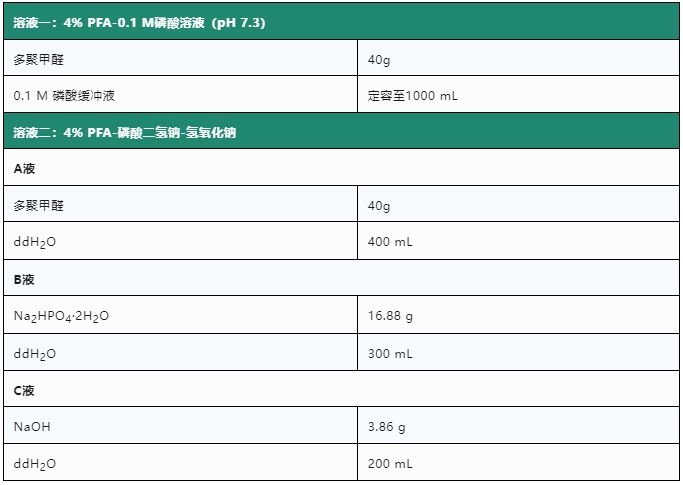
溶液一的配制步骤:
(1) 称取40 g多聚甲醛粉末,置于三角烧瓶中。
(2) 加入500-800 mL 0.1 M磷酸缓冲液(PB)。
(3) 加热至60℃左右,持续搅拌(或磁力搅拌)使粉末完全溶解,通常需滴加少许1N NaOH才能使溶液清亮。
(4) 补足0.1 M磷酸缓冲液至1000 mL,充分混匀。
此固定液较适用于IHC研究,特别是动物灌注固定取材及后续的浸泡固定(2-24 h)。固定液较为温和,适合组织标本的长期保存。
溶液二的配制步骤:
(1) A液在500 mL的三角烧瓶中配制,加热至60℃左右溶解。至多聚甲醛完全溶解后冷却备用。
(2) 配制B液和C液。
(3) 将B液倒入C液中,混合后再加入A液。
(4) 用1N NaOH或HCl将pH值调至7.2-7.4。
(5) 加ddH2O定容至1000 mL,4℃冰箱保存备用。
此固定液适用于光镜和电镜免疫组织或细胞化学研究。用于免疫电镜检测时,建议加入少量新鲜配制的戊二醛(终浓度为0.5-1%)。戊二醛属于双醛类固定剂,交联能力比甲醛强,有利于保存超微结构,但对抗原性的损伤也较大。在IHC实验中,戊二醛与甲醛联合使用,能够满足结构保存和抗原保留平衡的需求。
二、传统固定液的改良与创新
2.1 Bouin's液及其改良配方
Bouin's液是组织学和病理学的传统固定剂,由苦味酸、甲醛和冰醋酸组成。苦味酸沉淀蛋白引起组织收缩,但不会使组织硬化。Bouin's液对组织穿透力较强,固定效果好,对细胞的微细结构显示清晰,适用于富含结缔组织、胚胎及植物组织的标本,尤其在Masson三色法中,经其固定后组织着色鲜艳。
Bouin's液常规配方为饱和苦味酸750 mL、40%甲醛250 mL、冰醋酸50 mL,混合后移至棕色瓶中,存于4℃冰箱。冰醋酸最好临用前加入。改良版Bouin's液不加冰醋酸。
Bouin's液常规固定时间为12-24小时。由于该固定液呈酸性(pH 3-3.5),对抗原可能有一定损害,在固定1-2天后需换入4%的甲醛溶液中保存。
目前常用市售饱和苦味酸溶液直接配制。如果你手上是苦味酸粉末,则需要一种“邪修”方案了。首先在烧杯中加入1000 mL蒸馏水,并不断加入苦味酸粉末,边加边搅拌,直至有少量苦味酸结晶出现为止。静置并过滤。然后取750 mL苦味酸溶液与250 mL 40%甲醛混匀。最后加入冰醋酸。
2.2 Zamboni's液配方及其配制
Zamboni's固定液对超微结构的保存效果好于甲醛,可用于电镜和显微镜IHC检测。实验室常用配方为2.5%的多聚甲醛和30%的饱和苦味酸,固定时间控制在6-18小时。

2.3 PFG固定液 的配制
PFG固定液由对苯醌、多聚甲醛和戊二醛构成,结合了甲醛快速渗透和戊二醛的强效蛋白交联能力,又不影响超微结构的保存,适用于电镜样本的制备或对结果稳定性要求高的IHC实验。
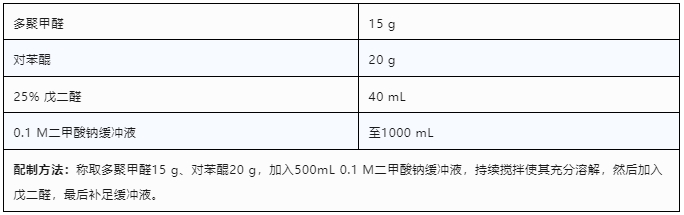
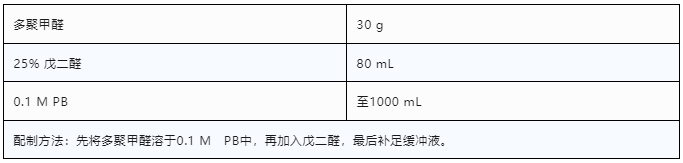
2.4 Karnovsky's固定液配制
适用于电镜免疫化学检测,在4℃短时固定效果好。推荐的操作流程为:先进行灌注固定,随后浸泡固定10-30分钟。“短时冷固定”策略已成为保存超微结构和肽类抗原的常用方法。
读到这里,你是否发现IHC固定液的世界远比“倒点甲醛泡一泡”要精彩的多,甲醛的“好搭子”远超想象。不同的组合、不同的配比,将会在组织或细胞结构中呈现不一样的结果。掌握这些固定液的配制方法,将会获得一张特异性强、背景干净的精美片子。
