功能抗体如何实现免疫调控与治疗干预?
一、功能抗体与传统检测抗体有何本质区别?
传统抗体主要利用其与抗原的特异性结合能力,用于检测目标蛋白的表达水平、定位及相互作用。而功能抗体在结合抗原后,通过占据关键功能域或诱导构象变化,直接干预靶蛋白的生物学活性,产生阻断、中和或激活等效应。这类抗体不再仅仅是"观察者",而是成为"干预者",在信号通路调控、感染防御及肿瘤治疗中发挥主动作用。随着免疫治疗时代的到来,功能抗体的开发与应用正从基础研究走向临床转化,成为药物研发的核心方向。功能性抗体主要包括中和/阻断抗体及刺激性抗体两大类别,其作用机制与应用场景各有特色。
二、中和抗体如何抵御病原体入侵?
中和抗体最初在感染免疫中被发现,是指能够阻止病原体感染宿主细胞的功能性抗体。当病原体如病毒或细菌侵入机体后,免疫系统产生特异性抗体,其中部分抗体结合于病原体表面参与黏附或入侵的关键结构域,通过空间位阻或构象改变,阻断病原体与靶细胞受体的相互作用,使其无法进入细胞。这一机制在体液免疫防御中发挥核心作用。乙肝疫苗的免疫原理即基于中和抗体的诱导。接种乙肝表面抗原后,机体产生针对表面抗原的中和抗体,当病毒入侵时,抗体迅速结合病毒颗粒,阻断其与肝细胞的结合,实现预防感染。在肿瘤领域,中和抗体可用于阻断促肿瘤生长的细胞因子,如抗IL-6抗体通过中和IL-6信号,抑制肿瘤增殖及炎症微环境。
三、阻断抗体如何干预信号通路?
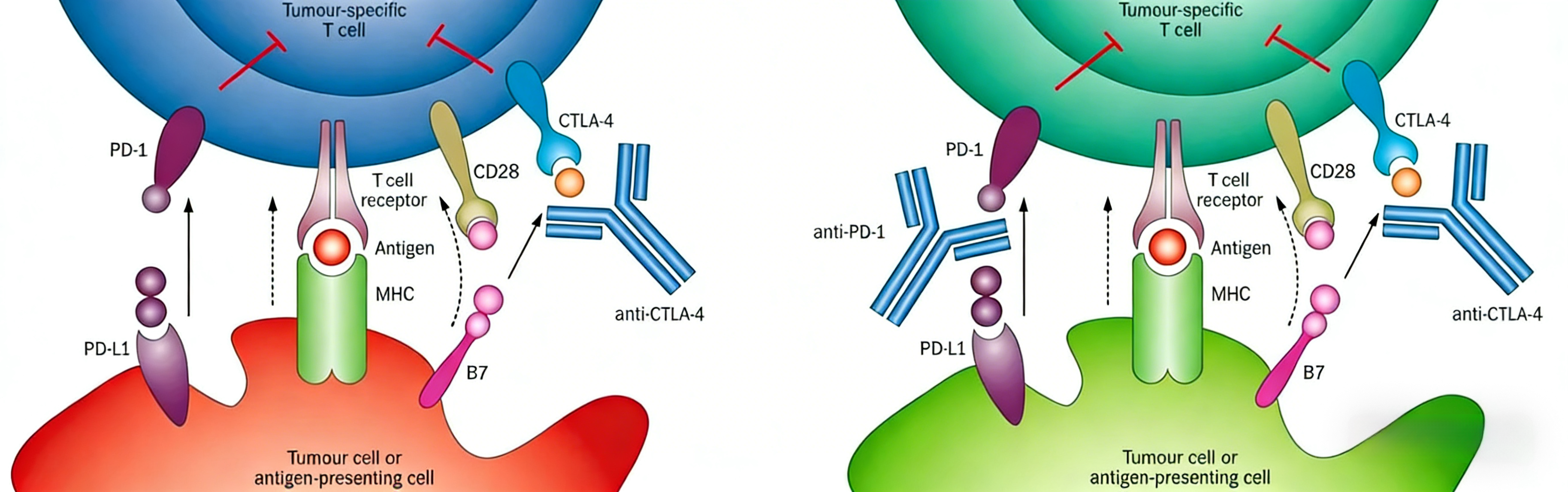
阻断抗体是指与靶蛋白结合后,通过占据配体结合位点或诱导构象变化,直接抑制蛋白功能的抗体。在细胞信号传导中,许多可溶性因子如细胞因子、生长因子及趋化因子,通过与细胞表面受体结合启动下游信号。阻断抗体通过竞争性结合配体或受体,破坏这一相互作用,从而抑制信号传导。阻断抗体通常是指抗体与目的蛋白结合直接影响蛋白的功能,如阻断粘附蛋白与受体配体的结合;而中和指抗体与蛋白结合后,引起该蛋白下游生物学活性的消失,如增殖或趋化。肿瘤治疗中的许多单克隆抗体属于阻断抗体,如抗PD-1抗体结合T细胞表面的PD-1受体,阻断其与肿瘤细胞PD-L1的结合,解除对T细胞的抑制;抗EGFR抗体结合表皮生长因子受体胞外区,阻断配体诱导的二聚化及下游信号,抑制肿瘤细胞增殖。
四、刺激性抗体如何激活免疫应答?
与阻断抗体相反,刺激性抗体通过结合特定受体,模拟天然配体的作用,激活下游信号通路。在肿瘤免疫治疗中,激动型抗体通过靶向共刺激分子,增强T细胞功能。最常用的体外刺激T淋巴细胞增殖的CD3抗体,通过结合T细胞受体复合物中的CD3分子,提供T细胞活化的第一信号,模拟抗原刺激。在体内应用中,抗CD28抗体提供T细胞活化的第二信号;抗4-1BB抗体促进T细胞增殖及存活;抗OX40抗体增强效应T细胞功能及记忆形成。刺激性抗体的设计需精细调控激活强度,过度激活可导致细胞因子风暴等严重不良反应。通过优化亲和力、选择合适亚型及表位,可实现肿瘤局部激活与全身安全性的平衡。
五、功能性抗体在肿瘤治疗中如何应用?
功能性抗体已成为肿瘤治疗的核心药物。PD-1/PD-L1抗体通过阻断抑制性信号,恢复T细胞抗肿瘤功能;CTLA-4抗体通过阻断抑制性受体或清除调节性T细胞,增强免疫应答;HER2抗体通过阻断信号通路及介导抗体依赖的细胞介导的细胞毒作用,清除肿瘤细胞;CD20抗体通过抗体依赖的细胞介导的细胞毒作用及补体依赖的细胞毒作用,靶向B细胞淋巴瘤。联合治疗是功能性抗体发展的方向。阻断PD-1/PD-L1与激动4-1BB或OX40,可同时解除抑制并增强激活,实现协同抗肿瘤效应。双特异性抗体通过同时靶向T细胞及肿瘤细胞,将免疫效应精准导向肿瘤。
六、小结
功能性抗体通过阻断、中和或激活靶蛋白,从"检测工具"跃升为"治疗武器"。在肿瘤免疫、感染防御及自身免疫病中,功能性抗体正发挥日益重要的作用。理解靶点生物学特性、精准选择表位、优化功能验证,可使定制抗体在基础研究及临床转化中释放更大潜力,推动免疫治疗持续进步。
