TIM-3抗体如何突破肿瘤免疫治疗瓶颈?
一、TIM-3在肿瘤免疫中扮演什么角色?
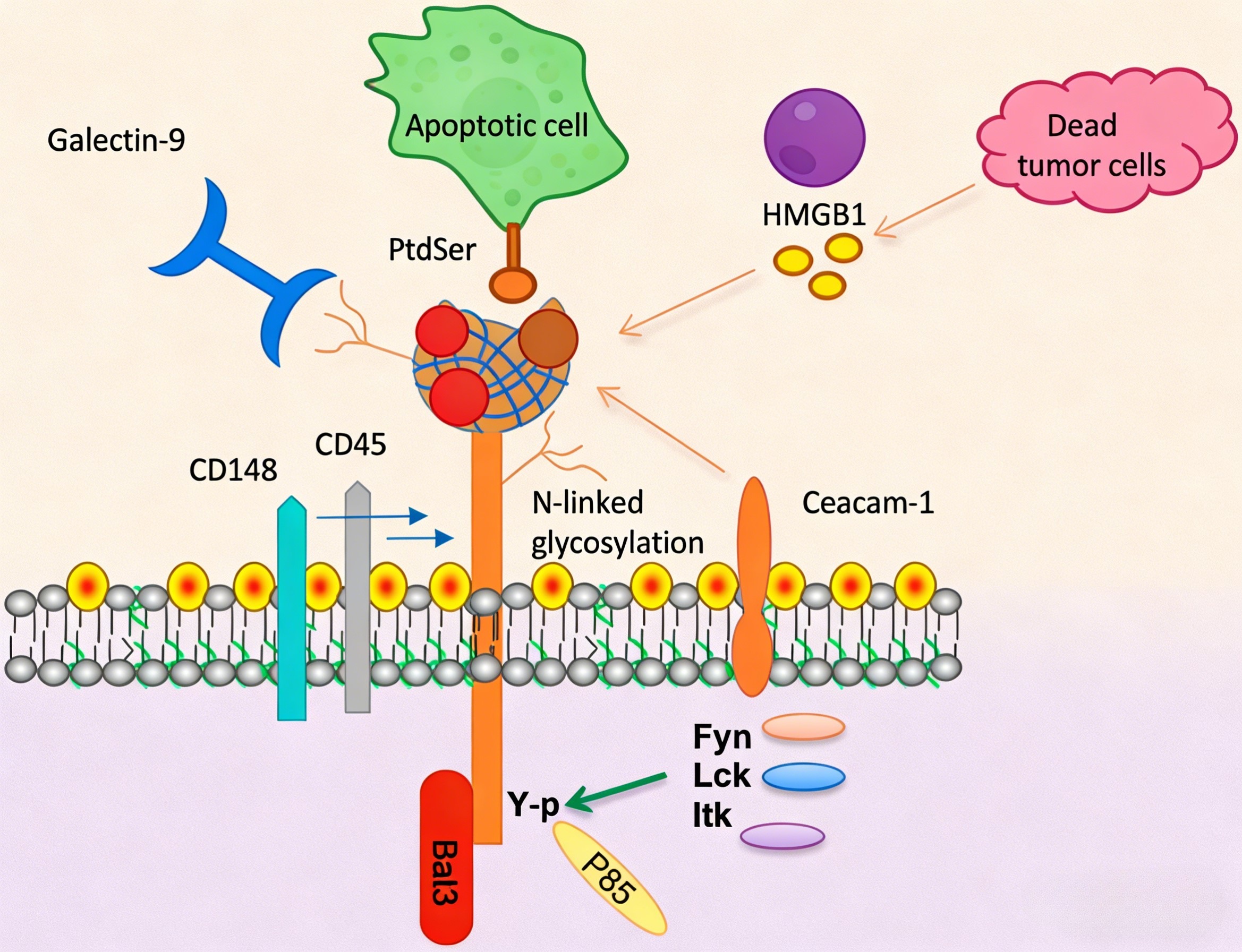
TIM-3是T细胞免疫球蛋白黏蛋白分子3,最初被发现为分化的Th1细胞及CD8+细胞毒性T细胞的特异性标志,随后研究证实其广泛表达于调节性T细胞、单核巨噬细胞、树突状细胞及髓源性抑制细胞表面。TIM-3通过与其配体如半乳凝素-9、磷脂酰丝氨酸、高迁移率族蛋白B-1及癌胚抗原相关细胞黏附分子1相互作用,在肿瘤免疫中发挥负性调控作用。在肿瘤微环境中,TIM-3高表达于功能障碍的CD8+ T细胞,与其配体结合后诱导胞内酪氨酸磷酸化,抑制T细胞活化与增殖,减少正性调控细胞因子的产生,促进免疫逃逸。同时,TIM-3在调节性T细胞及髓源性抑制细胞上的表达进一步放大了免疫抑制效应。因此,TIM-3成为继PD-1及CTLA-4之后最具潜力的免疫检查点靶点。
二、TIM-3抗体的作用机制是什么?
TIM-3抗体通过特异性结合TIM-3分子,阻断其与配体的相互作用,解除对T细胞的抑制。与PD-1抗体不同,TIM-3抗体的作用机制不依赖免疫受体酪氨酸抑制基序,而是通过阻断TIM-3与半乳凝素-9等配体的结合,逆转T细胞耗竭状态。封闭TIM-3信号可恢复T细胞的增殖能力、IFN-γ等效应细胞因子的分泌及肿瘤细胞杀伤活性。TIM-3在肿瘤组织中的选择性表达使其成为精准治疗靶点,与传统免疫检查点抑制剂相比,可能减少对正常组织的免疫相关不良反应。TIM-3抗体还可通过抗体依赖的细胞介导的细胞毒作用清除表达TIM-3的抑制性免疫细胞亚群,重塑肿瘤微环境。
三、TIM-3抗体与PD-1抗体联用有何协同效应?
PD-1抗体在多种肿瘤中取得显著疗效,但耐药问题日益突出。在PD-1阻断后耐药的动物模型中,T细胞表面TIM-3表达显著上调,提示TIM-3是PD-1阻断后获得性耐药的关键机制。联合应用TIM-3抗体与PD-1抗体可同时阻断两个非冗余的免疫检查点,协同逆转T细胞耗竭,增强抗肿瘤免疫应答。临床前研究显示,联合治疗可显著增加IFN-γ产生及T细胞增殖,改善肿瘤控制。在临床试验中,PD-1抑制剂与TIM-3抑制剂联用正在多种实体瘤中进行探索,旨在克服单药治疗的耐药性,提高客观缓解率及无进展生存期。
四、TIM-3抗体在肿瘤免疫治疗中的临床进展如何?
目前全球尚无TIM-3抑制剂获批上市,但多个在研药物已进入临床阶段。处于临床Ⅱ期及Ⅰ期的在研药物各有多项,主要开发方向包括单药治疗、联合PD-1/PD-L1抑制剂及联合化疗。TIM-3抗体的开发策略多采用与PD-1抑制剂联用的联合疗法,以克服耐药、扩大获益人群。双特异性抗体的开发也在推进中,将TIM-3抗体与PD-1抗体整合为单一分子,可实现协同靶向、简化给药方案。临床前研究显示,联合抗TIM-3抗体治疗可带来临床及放射学获益,延长生存期。
五、TIM-3抗体在联合治疗策略中如何应用?
联合治疗是TIM-3抗体的核心开发方向。TIM-3抗体与PD-1/PD-L1抑制剂联用可同时解除T细胞活化的多重抑制,逆转耗竭,增强效应功能。TIM-3抗体与化疗联用可增强化疗诱导的免疫原性细胞死亡,促进肿瘤抗原释放,协同激活抗肿瘤免疫。TIM-3抗体与放疗联用可增强放疗的远隔效应,使未经照射的转移灶也产生退缩。TIM-3抗体与CTLA-4抗体联用可协同调节T细胞活化的早期及效应阶段。双特异性抗体将TIM-3与PD-1靶向结合于同一分子,可同时阻断两条抑制通路,减少系统暴露及联合用药的复杂性。
六、TIM-3抗体研发面临哪些挑战?
TIM-3抗体的临床转化仍面临挑战。TIM-3在多种免疫细胞上的表达使其功能具有复杂性,不同细胞亚群中TIM-3阻断可能产生协同或拮抗效应。TIM-3与其多种配体的相互作用网络尚未完全阐明,不同配体在肿瘤微环境中的相对贡献有待明确。TIM-3抗体单药疗效有限,联合治疗的最佳伙伴、时序及剂量仍需优化。生物标志物的开发将助力患者筛选,TIM-3表达水平、配体状态及免疫微环境特征可能预测治疗反应。长期安全性的评估需在临床试验中严密监测。
七、小结
TIM-3作为新兴免疫检查点靶点,通过阻断其负性调控信号,可逆转T细胞耗竭、重塑肿瘤微环境。TIM-3抗体与PD-1抗体的联合治疗策略在克服耐药、增强疗效方面展现出巨大潜力。随着临床研究的推进及机制研究的深入,TIM-3抗体有望成为肿瘤免疫治疗的新利器,为更多患者带来临床获益。
