58.3% MRD 清除率支持门诊!通用型 CAR-T 关键 II 期亮眼,国内企业布局三大适应症
2026 年 4 月 16 日
医麦客新闻 eMedClub News
4 月 13 日,通用细胞疗法领军企业 Allogene Therapeutics 公布了其核心管线 Cema-Cel 针对一线巩固治疗大 B 细胞淋巴瘤(LBCL)的关键性随机 II 期 ALPHA3 试验的计划内中期无效性分析数据,展示了 Cema-Cel 的疗效与安全性。

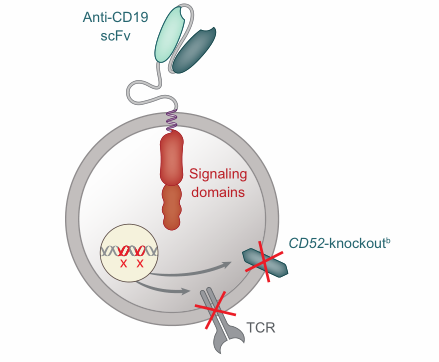
Cema-Cel 是一款靶向 CD19 的通用现货型 CAR-T 细胞疗法,来源于健康供体,敲除了 TRAC 和 CD52,避免移植物抗宿主病(GvHD)及增加 CD52 单抗的耐受性。
疗效提示显著临床获益
在方案规定的数据截止点,即第 24 例患者完成第 45 天微小残留病(MRD)评估时,Cema-Cel 治疗组有 58.3%(7/12)的患者实现 MRD 阴性,观察组这一比例为 16.7%(2/12),两组的 MRD 清除率绝对差异高达 41.6%。根据文献,MRD 清除率差异达到 25-30% 即可预示研究最终可能获得显著临床获益。
此外,在首次 MRD 评估(第 45 天)时,Cema-Cel 治疗组患者的血浆 ctDNA 较基线中位下降 97.7%,而观察组中位上升 26.6%。Allogene 认为,这些中期数据初步支持了 Cema-Cel 作为高危患者一线治疗结束后新型干预策略的潜力。
治疗后 MRD 状态已成为 LBCL 复发的强预测因子,为疾病负荷较低但进展风险仍高的早期干预提供了潜在机会。ALPHA3 试验是唯一采用一项全新开发的在研检测技术——由 PhasED-Seq™ 技术驱动的 Foresight CLARITY™ 来筛选一线治疗后高复发风险的患者。

「0」严重副作用
在安全性方面,12 例接受 Cema-Cel 治疗的患者中,10 例输注后全程在门诊管理;其余 2 例短期住院原因被判定与 Cema-Cel 治疗无关(房颤、非心源性胸痛)。Cema-Cel 总体耐受性良好,无治疗相关严重不良事件,未出现任何 CRS、ICANS 或 GvHD 病例。这一安全性数据远优于传统 CAR-T 治疗数据,即使是在门诊项目下,仍有约 70-90% 的患者需要入院,约 75% 的患者在 30 天内因不良事件住院。
华盛顿大学医学院肿瘤学部教授、Siteman 癌症中心医师 Nancy L. Bartlett 医学博士评价:“Cema-Cel 早期展现出无 CRS 和 ICANS 的优异安全性特征,令人备受鼓舞,为安全开展门诊治疗奠定了重要基础。结合现货型 CAR-T 的可及性,这些数据表明 Cema-Cel 有望突破长期制约 CAR-T 广泛应用的关键临床与实操瓶颈,尤其在前线治疗场景中更具价值。叠加其出色的 MRD 清除效果,该治疗策略有望在显著改善患者预后的同时,大幅扩大治疗可及性。”
真实世界可行性与社区应用
传统 CAR-T 往往要求治疗中心有着过硬的医疗资源,而在本次中期分析中,社区肿瘤中心贡献约 33% 的筛查活动和 Cema-Cel 输注,其中包括多家几乎无 CAR-T 治疗经验的中心,这更加凸显了 Cema-Cel 在社区场景应用的可行性。
Willamette Valley 癌症研究所、SCRI 淋巴瘤研究执行委员会主席 Jeff Sharman 医学博士表示:“在繁忙的社区临床实践中,目标很简单:让治疗走近患者,而非患者奔赴治疗。传统 CAR-T 在社区机构基本难以开展。现货型 CAR-T 可在社区安全实施、甚至门诊给药,有望覆盖更多患者,拓展治疗可及范围。”
据官网报道,该研究在全球超 60 家中心开展,计划入组约 220 例患者,预计 2027 年底完成入组,到 2028 年完成主要无事件生存期(EFS)分析。若结果积极,有望支持生物制品许可申请(BLA)递交。
国内通用型CAR-T近期进展
Cema-Cel 的亮眼表现为通用型细胞疗法赛道带来了里程碑式验证,打破了「疗效不如自体、安全性存疑」的质疑,加上成本可控、批量生产的优势有望让 CAR-T 实现真正可及。近期,国内通用型细胞疗法已经取得诸多亮眼进展。
茂行生物
茂行生物的 MT026 是一款靶向 IL-13Rα2 的通用型 CAR-T 细胞疗法,其治疗复发性高级别胶质瘤的 I 期临床研究数据已经于今年 1 月发表在了 Nature Communications 杂志上,结果显示:在入组的 5 例患者中,客观缓解率(ORR)达到 80%,包括 1 例完全缓解和 3 例部分缓解,整体安全性较好。
MT027 是一款靶向 B7H3 的通用型 CAR-T 细胞疗法,其采用非病毒基因编辑工艺,进一步提升了候选产品的安全,支持规模化生产和冻存,患者确诊后无需等待,即可迅速获得治疗,被开发用于治疗复发性胶质母细胞瘤(rGBM)。2025 年 12 月,MT027 获得 FDA 批准开展针对 rGBM 的 II 期临床研究。
邦耀生物
邦耀生物的 BRL-303 是基于 TyUCell® 开发的一款靶向 CD19 的通用型 CAR-T 细胞疗法,通过多重基因编辑技术实现异体 T 细胞的免疫逃逸和功能优化。2025 年 12 月,BRL-303 针对中度或重度难治性系统性红斑狼疮(rSLE)的 IND 申请获得默示许可。值得一提的是,BRL-303 是全球首款在研究者发起的临床试验中,针对自身免疫性疾病显示出疗效的异体通用型 CAR-T 产品。
科济药业
科济药业的 CT0596 是一款通用型 BCMA CAR-T。2025 年 12 月,科济药业在美国 ASH 年会上展示了该候选产品在复发/难治性多发性骨髓瘤(R/R MM)患者中的首次人体研究成果:
截至 2025 年 8 月 31 日,8 例已输注患者均为可评估疗效人群,中位随访时间为 4.14 个月(范围:0.9-7.9 个月),6 例患者达到部分缓解(PR)及以上疗效。其中一位患者截至第 8 个月仍持续达到 sCR 且 MRD 阴性,另一位患者经第二次输注后,达到 PR,且髓外疾病获得缓解。科济药业计划在今年开启 CT0596 的 Ib 期注册临床研究。
北恒生物
北恒生物的 CTD402 是一款靶向 CD7 的通用型 CAR-T,采用了 TCR 和 HLA II 类基因敲除设计,并结合了北恒生物专有的 ANSWER® 抑制性配体,以增强对宿主免疫排斥的抵抗力。
2025 年 12 月,北恒生物在 ASH 年会上,公布了 CTD402 的最新临床研究成果:10 例复发/难治性急性髓系白血病(R/R AML)患者接受了 CTD402 的治疗,ORR 达到 62.5%,所有应答者均达到 MRD 阴性,部分患者在后续接受造血干细胞移植后,缓解持续时间已超过四年。
针对复发/难治性 T 细胞急性淋巴细胞白血病/淋巴母细胞淋巴瘤(T-ALL/LBL)患者的治疗中,39 例患者的 CR 率达到 64.1%,其中 91.7% 的应答患者达到疾病阴性状态。整体安全性良好。
总结
此处不再一一举例,整体而言可以看到通用型 CAR-T 细胞疗法赛道呈现出「逐步推进临床,适应症全面拓展」的趋势,就全球范围而言,进展最快的通用型 CAR-T 疗法已经进入关键临床 II 期,国外领跑,国内企业则逐步完成临床转化并推进临床,进展较快的企业已经初步公布了候选产品的试验数据,初步验证了通用型 CAR-T 的有效性和安全性。同时,通用型 CAR-T 的适应症已经从血液瘤逐步拓展到实体瘤并延伸到了非肿瘤的自免领域,有望在未来为更多患者带来可及性更高的治疗选择。
责任编辑丨浔
校对丨浔
参考资料:
1.企业官网
精彩活动
长按识别二维码立即参与↓
推荐 1
4 月 16 日 19:00-20:30
2026 核酸药物爆发启示,开发、药效机制研究与爆发的底层逻辑


点点“分享”、“点赞”和“在看”
给我充点儿电吧~