中国结直肠癌手术病例登记数据库2025年度报告:一项全国性前瞻性登记研究

目的 分析中国结直肠癌手术病例登记数据库(CCCD)自2020年1月升级后纳入的前瞻性登记数据,特别关注直肠癌MRI检查率及新辅助治疗比例等规范化诊治的关键指标,为国内结直肠癌外科治疗策略制定和临床实践提供循证医学证据。
方法 前瞻性纳入2020年1月至2025年9月期间CCCD收集的结直肠癌手术病人临床病理学资料,标准化整理后分析其临床特征、外科诊疗方案及术后短期结局。
结果 CCCD更新后,共纳入86个医学中心的结直肠癌手术病例19 806例,其中36.0%的病例来自地市级医院。结直肠癌手术病人中,直肠癌(50.2%)比例稍高于结肠癌(49.8%),中、低位直肠癌占所有直肠癌的70.9%。直肠癌病人术前MRI检查及格式化报告的填报率为73.9%。结直肠癌病人术前行新辅助治疗占10.5%,其中结肠癌新辅助治疗占6.7%,直肠癌新辅助治疗占16.0%,中低位直肠癌中16.6%行新辅助治疗。腹腔镜手术占88.7%,其中完全腹腔镜下结直肠手术占48.5%。手术根治性方面,R0手术切除占96.2%,而R2手术切除占2.9%。总体术后并发症发生率为8.4%,吻合口漏是术后最常见的并发症,发生率为2.0%,中低位直肠癌术后吻合口漏发生率为2.9%,其余部位(上段直肠癌及结肠癌)手术后吻合口漏发生率为1.7%。
结论 CCCD前瞻性登记研究结果表明,近年来中国结直肠癌手术病人的基线情况、外科诊疗模式呈现动态变化,规范化诊断和治疗程度在提升。未来应重点关注标准化诊疗流程的推广普及及地市级医院诊疗能力提升,进一步优化随访数据采集机制。
李 杨1,李心翔2,崔 龙3,张 卫4,池 畔5,王自强6,石晋瑶1,揭志刚7,孙跃明8,卢 云9,韩方海10,何显力11,陶凯雄12,王 权13,王贵英14,王振宁15,李 海16,钱 群17,李乐平18,卫洪波19,李伟华20,房学东21,姚宏伟1,张忠涛1,
代表中国结直肠癌手术病例登记数据库研究者团队
基金项目:国家科技重大专项-四大慢病防治研究项目(No.2024ZD0520302);国家重点研发计划项目(No.2017YFC0110904);北京市医院管理中心扬帆计划临床技术创新项目(No.ZLRK202302);首都医科大学结直肠肿瘤临床诊疗与研究中心专项基金项目(No.1192070313);首都医科大学结直肠癌免疫治疗基础-临床联合实验室项目(No.2023-175);首都医科大学附属北京友谊医院“友谊种子计划”人才项目(No.YYZZ202420)
作者单位:1首都医科大学附属北京友谊医院普通外科 消化系统疾病国家临床医学研究中心 消化健康全国重点实验室,北京 100050;2复旦大学附属肿瘤医院大肠外科,上海 200032;3上海交通大学附属新华医院结直肠外科,上海 200092;4海军军医大学第一附属医院肛肠外科,上海 200433;5福建医科大学附属协和医院结直肠外科,福建福州 350001;6四川大学华西医院胃肠外科,四川成都 610041;7南昌大学第一附属医院普通外科,江西南昌 330006;8南京医科大学第一附属医院结直肠外科,江苏南京210029;9青岛大学附属医院胃肠外科,山东青岛 266000;10中山大学孙逸仙纪念医院胃肠外科,广东广州 510120;11空军军医大学唐都医院普外科,陕西西安 710038;12华中科技大学同济医学院附属协和医院胃肠外科,湖北武汉 430022;13吉林大学白求恩第一医院胃肠外科,吉林长春 130021;14河北医科大学第四医院普通外科,河北石家庄 050011;15中国医科大学附属第一医院胃肠外科,辽宁沈阳 110001;16宁夏医科大学总医院普通外科,宁夏银川 750004;17武汉大学中南医院结直肠肛门外科,湖北武汉 430071;18山东省立医院胃肠外科,山东济南 250021;19中山大学附属第三医院胃肠外科,广东广州 510630;20福建省立医院肿瘤外科,福建福州 350001;21吉林大学中日联谊医院胃肠结直肠肛门外科,吉林长春 130012
通信作者:姚宏伟:E-mail:yaohongwei@ccmu.edu.cn;张忠涛,E-mail:zhangzht@ccmu.edu.cn
注:李杨,李心翔,崔龙,张卫,池畔,王自强和石晋瑶对本文具有同等贡献,为共同第一作者
为进一步推进结直肠癌诊疗规范化与个体化,2017年9月,中华医学会外科学分会结直肠外科学组牵头成立了中国结直肠外科大数据研究协作组(Chinese Task Force of Colorectal Big Data,C-CBD),同时设计并建立了中国结直肠癌手术病例登记数据库(Chinese Colorectal Cancer Surgery Database,CCCD),该数据库的建立为推动国内结直肠癌领域的临床研究的开展奠定了基础[1-2]。近年来,依托该数据库所登记的病例信息,CCCD研究团队已多次发布关于中国结直肠癌手术病例的详细报告[3-4],向全国结直肠外科同道展示了中国大样本量结直肠癌手术病人的诊疗现状,以及中国结直肠癌手术病例的特征。为进一步扩大数据覆盖范围、提升数据录入质量,确保数据库更精准、全面地反映结直肠癌诊疗的实际情况,自2020年1月起,CCCD启动了全面优化与升级工作,采用前瞻性的数据收集与录入模式。这一转变,使数据获取更具时效性与准确性,为后续研究提供了坚实支撑。截至2025年9月,CCCD中前瞻性数据病例数量已突破19 000例。基于此,本文拟对CCCD中前瞻性数据进行系统梳理与深入分析。现将相关分析结果报告如下。
1 |资料与方法
1.1 CCCD介绍 2017年9月,中华医学会外科学分会结直肠外科学组牵头正式构建了CCCD。该数据库依托在线填报系统(网址:https://www.c-cbd.cn/),为全国范围内开展结直肠癌手术的医学中心搭建了标准化的病例信息登记平台。在数据库建设初期(即2019年10月之前),CCCD主要聚焦于回顾性数据的收集工作,数据导入方式以各医学中心数据库字段匹配导入为主。自2020年1月起,CCCD完成了系统升级,全面转向前瞻性数据采集模式。为进一步提升数据录入的准确性与完整性,此次升级在保留原有平台架构的基础上,对各模块所涵盖的字段内容及填报方式进行了系统性优化与扩展。
目前,CCCD录入系统包含以下核心模块:(1)病人基本信息。(2)术前肠镜检查结果。(3)术前CT影像学资料。(4)术前MRI影像学资料。(5)术前诊断评估。(6)手术治疗方案。(7)术后并发症监测。(8)术后病理学诊断。(9)长期随访信息。截至2025年9月,全国已有86家医学中心参与CCCD的前瞻性数据录入工作。
1.2 病例登记对象 CCCD的纳入标准为经病理学检查结果确诊为结直肠腺癌,且已行外科手术治疗的病人。CCCD的临床研究方案通过首都医科大学附属北京友谊医院医学伦理委员会的严格审查并获得批准(No.2018-P2-045-01)。此外,CCCD所有资料的披露与发表事宜均已征得各参与医学中心同意。
2 |结果
2.1 CCCD登记统计 截至2025年9月,CCCD累计纳入结直肠癌手术病例102 869例,2020年1月之前回顾性登记的病例数为83 063例。本文所分析的数据为该数据库系统升级后(2020年1月至2025年9月)前瞻性收集的病例数据。在此阶段,数据库共收录来自我国30个省、自治区、直辖市的86家医学中心上报的结直肠癌手术病例19 806例。
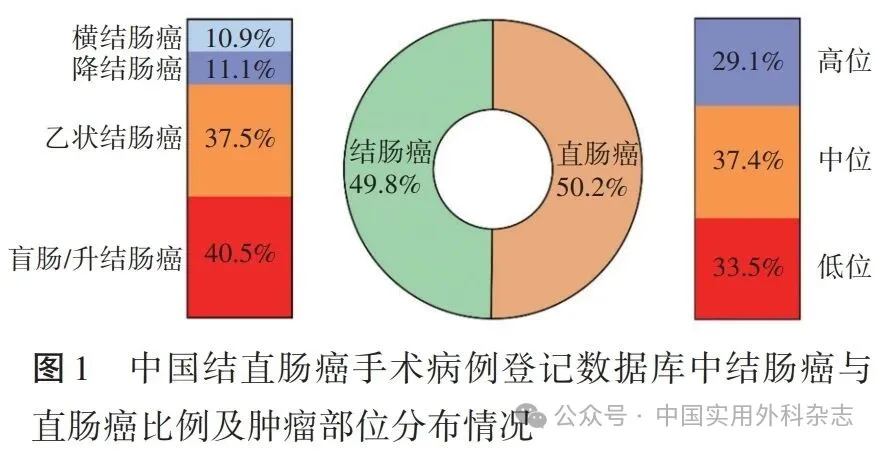
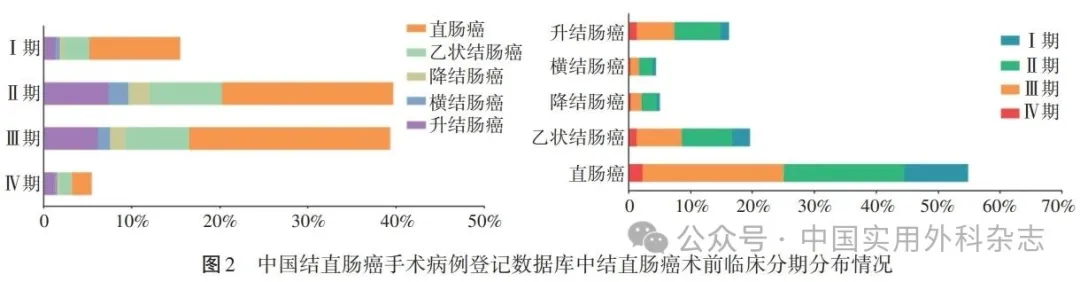
2.2 病人临床基本特征 19 806例结直肠癌手术病人中,男性占60.4%,女性占39.6%。中位年龄63(55, 70)岁,平均BMI为23.11±4.23。术前内镜评估结果显示,结直肠癌手术病人中结肠癌与直肠癌的构成比分别为49.8%和50.2%。直肠癌手术病人中,中、低位直肠癌占70.9%,低位直肠癌占33.5%、中位直肠癌占37.4%,高位直肠癌占29.1%。结肠癌手术病人中以盲肠或升结肠癌最为常见,占40.5%,其次为乙状结肠癌,占37.5%,降结肠癌及横结肠癌相对较少,分别占11.1%与10.9%。见图1。基于术前影像学检查结果的临床TNM分期中,Ⅰ、Ⅱ、Ⅲ、Ⅳ期结直肠癌病人分别占15.2%、39.4%、39.4%、6.0%,不同部位结直肠癌临床分期情况见图2。远处转移模式分析结果表明,肝脏为最常见转移靶器官(77.7%),其次为肺(11.1%)、腹膜(9.8%)及骨骼(1.4%)。
在所有结直肠癌病人群体中,依据血清白蛋白检测结果分析,术前合并低白蛋白血症的病人占33.7%。通过外周血血红蛋白检测结果评估,术前合并轻度、中度和重度贫血的病人比例分别为22.2%、6.1%和0.4%。关于肿瘤标记物指标情况,术前血清癌胚抗原(CEA)水平呈现不同程度的升高,其分布情况为:升高幅度<2倍的病人占15.1%,升高2~4倍占8.0%,升高4~8倍占4.3%,升高>8倍占5.9%,术前CEA处于正常水平的病人占66.7%。见图3。
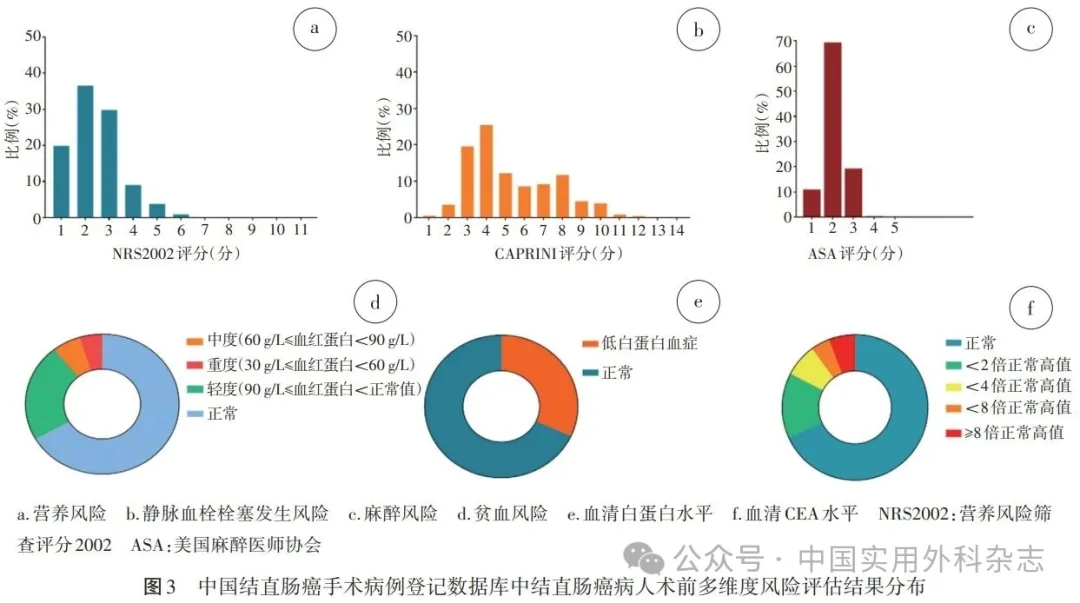
此外,CCCD还全面涵盖了病人的基本风险评估信息,包括营养风险、静脉血栓栓塞(VTE)发生风险以及麻醉风险等。营养风险筛查采用营养风险筛查评分2002(NRS 2002),评分≥3分的病人占34.5%,评分<3分的病人占65.5%。静脉血栓栓塞性并发症风险评估采用VTE评分(CAPRINI评分),所有病人CAPRINI评分中位数为6(4,8)分;麻醉风险评估采用美国麻醉师协会(ASA)评分,Ⅰ~Ⅴ级病人分别占17.60%、66.70%、15.20%、0.48%、0.02%。见图3。
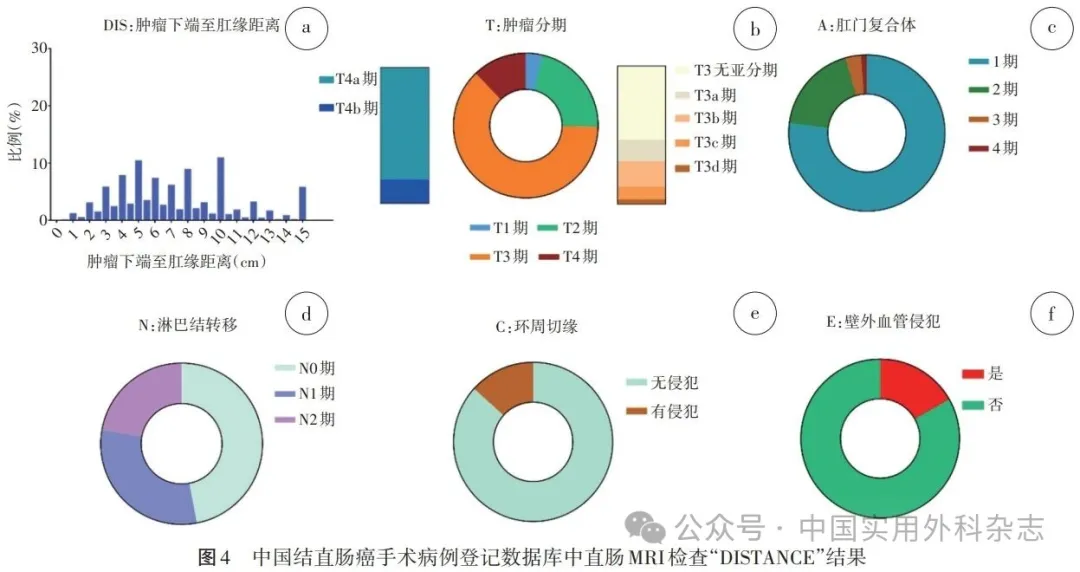
2.3 直肠癌术前MRI检查情况 所有直肠癌手术病例中,73.9%的病人通过直肠MRI检查进行术前评估并进行了信息登记。直肠MRI检查完成情况在各中心相差较大,来自直辖市及省会城市的三级甲等医院中,部分医学中心的直肠MRI检查完善率可高达100.0%,而来自地市级的部分医学中心,直肠MRI检查率仅有39.2%。CCCD的直肠癌MRI数据填报模式采用了“DISTANCE”格式化报告系统,结果如下:(1)肿瘤下缘离肛缘(DIS)中位距离为(6.5±3.2)cm。(2)肿瘤浸润深度T分期(T)中,T1期占3.9%,T2期占25.5%,T3期占60.1%,其中T3a期占11.5%、T3b期占10.4%、T3c期占5.1%、T3d期占1.9%,T4a期和T4b期分别占8.1%和2.4%。(3)肛门复合体(A)评估中,1~4期分别占69.2%、23.9%、5.1%以及1.8%。(4)淋巴结转移N分期(N)中,49.1%直肠癌病人无淋巴结转移(N0),28.8%存在≤3枚转移淋巴结(N1),22.1%的病人有≥4枚淋巴结转移(N2)。(5)环周切缘(C)评估中,有15.2%的直肠系膜筋膜受侵犯,即环周切缘(circumferential resection margin,CRM)阳性。(6)肠壁外血管侵犯(E)情况评估中,肠壁外血管侵犯(extramural venous invasion,EMVI)比例占16.5%。见图4。
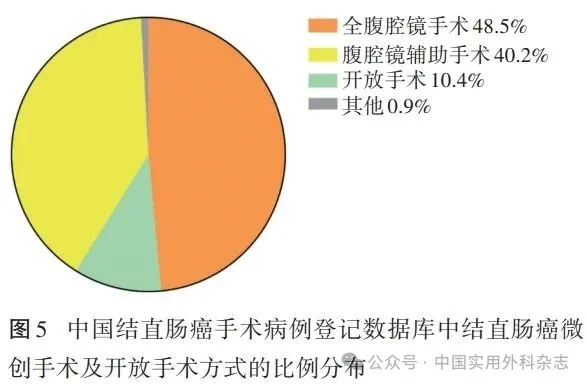
2.4 手术治疗及术后并发症情况 在纳入研究的19 806例结直肠癌病人中,腹腔镜手术占88.7%(完全腹腔镜下结直肠手术占48.5%,腹腔镜辅助手术占40.2%),开放手术占10.4%,另有0.9%的病人采用了其他手术方式,如经肛操作平台等。见图5。关于手术切除范围,96.2%的病人实现了R0切除,R1和R2切除的比例分别为0.9%和2.9%。在淋巴结清扫方面,D1、D2、D3淋巴结清扫的比例依次为1.3%、23.4%和75.3%。在消化道重建方式上,97.6%的病人采用了器械吻合,仅2.4%的病人进行了手工吻合。就吻合方式而言,端-端吻合、端-侧吻合和侧-侧吻合的比例分别为69.7%、13.0%和17.3%。术后总并发症发生率为8.4%,其中,吻合口漏是结直肠癌术后最常见的并发症,总体发生率为2.0%。中、低位直肠癌术后吻合口漏发生率为2.9%,其余部位(上段直肠癌及结肠癌)吻合口漏发生率稍低,为1.7%。吻合口漏以B级吻合口漏最常见,占53.0%,A级及C级吻合口漏分别占25.3%与21.7%。发生率排名第二的术后并发症是手术部位切口感染(surgical site infection,SSI),发生率为0.9%;腹腔内感染的发生率排第三,发生率为0.8%。
2.5 术后病理学检查结果 在所有结直肠癌病人群体中,肿瘤最大径的平均值为(4.0±1.2)cm。关于淋巴结检出情况,检出淋巴结数目的中位数为15(12,21)枚,转移淋巴结数目的中位数为0(0,5)枚。从肿瘤组织学类型来看,中分化腺癌是最为常见的类型,占83.3%;其次为低分化腺癌,占8.5%。在术后病理TNM分期方面,Ⅰ、Ⅱ、Ⅲ、Ⅳ期病人比例分别为16.5%、39.7%、37.9%、5.9%。
2.6 围手术期治疗情况 在纳入研究的19 806例结直肠癌病人中,约10.5%的病人行新辅助治疗,与2022年度CCCD报告数据(11.5%)相比稍有下降。具体到不同部位,结肠癌病人中行新辅助治疗的比例为6.7%,其新辅助治疗模式以单纯化疗为主;相比之下,直肠癌病人行新辅助治疗的比例显著升高,达16.0%,且新辅助治疗模式多采用放疗联合化疗方案。中、低位直肠癌中16.6%的病人进行了新辅助治疗。在辅助治疗方面,有25.8%的病人行不同方案的辅助治疗。其中,辅助治疗模式以单纯化疗为主,占95.2%。
3 |讨论
2025年全球癌症统计结果显示,结直肠癌的发病率仍排名第三,病死率仅次于肺癌位居第二[5]。同时,结直肠癌是全球新增癌症病例中负担第三重的癌症,仅次于乳腺癌和肺癌[6]。在我国,2022年新发结直肠癌病例51.71万例,占全部恶性肿瘤发病的10.7%;死亡病例24.00万例,占全部恶性肿瘤死亡的9.3%。在我国男性恶性肿瘤中,结直肠癌发病率仅次于肺癌,位居第二位,严重威胁着国人的健康水平[7]。
在结直肠癌患病人群规模日益庞大的现实背景下,癌症登记数据库的价值愈发凸显。结直肠癌数据库能够系统且全面地收录癌症病人的人口学特征、肿瘤基线数据、治疗过程详情以及随访信息等关键资料。这些翔实的数据为开展高质量的临床研究提供了坚实的数据基础,同时也是制定科学、精准的相关诊疗指南不可或缺的重要依据,对于提升结直肠癌的防治水平具有不可替代的作用。在当前全球癌症研究与实践的格局中,发达国家在癌症数据库的建立及使用方面明显处于优势地位。基于高质量数据库所生成并发表的数据报告,为制定科学、精准且具有循证医学依据的结直肠癌规范化诊疗指南提供了坚实的数据支撑[8-13]。
近年来,国内在结直肠癌临床科学研究方面取得了飞速进展,这在一定程度上为结直肠癌数据库的建设起到了推动作用。然而,仍缺乏能够全面涵盖结直肠癌手术病人详细临床信息的全国性数据资源。为有效解决这一关键问题,中华医学会外科学分会结直肠外科学组于2017年9月正式成立中国结直肠癌病例登记数据库协作组(C-CBD),并基于此构建了CCCD。CCCD作为国家级多中心临床登记研究平台,对于持续监测结直肠癌诊疗质量,发现地区与机构差异,指导临床实践规范化,推动诊疗同质化具有不可替代的战略价值。本数据库经过8年的持续完善,已成为中国最大规模的结直肠癌外科专病登记系统,为推进精准防治、优化医疗资源配置、制定循证医学指南提供了坚实的数据基础。
本次报告的CCCD前瞻性登记结直肠癌病例数据涵盖了我国30个省、自治区、直辖市的86个医学中心。其中三级甲等医院占92.0%,本次报告数据覆盖医院范围更广且有代表性。19 806例结直肠癌手术病人中,直肠癌比例较结肠癌略高,此数据较2019及2022年度报告数据均明显下降[3-4]。直肠癌中,肿瘤部位仍以中、低位直肠为主,占70.9%,较往年报告数据有所下降[3-4]。分析其下降原因,可能与以下因素相关:(1)中、低位直肠癌手术难度相较于高位直肠癌手术更大,为规避可能增加的手术风险,同时满足病人保肛需求,病人更倾向于前往大型三级甲等医院就诊治疗。(2)CCCD数据显示,前瞻性数据中地市级医院比例(36.0%)相较于前期回顾性数据明显增加,这也在一定程度上可能影响了整体数据里中低位直肠癌的比例。面对中低位直肠癌病人比例仍居高位且保肛诉求持续攀升的临床现状,以经肛全直肠系膜切除(transanal total mesorectal excision,taTME)、改良Bacon术式及经自然腔道标本取出术(natural orifice specimen extraction surgery,NOSES)为代表的创新微创技术,正展现出广阔的临床应用前景与学术研究价值。经过十余年临床实践经验与临床研究结果,taTME安全性及肿瘤学有效性均得到了充分验证[14-16]。taTME显著拓展了超低位直肠癌的保肛适应证,使更多的病人得以保留肛门功能,同时将CRM阳性率控制在<3.0%,较传统腹腔镜手术降低近40.0%[17]。此次报告数据中也有约0.2%的病人通过行taTME避免了永久结肠造口。
直肠MRI检查对于评估直肠癌局部分期、CRM、EMVI等情况,并为病人制定个性化治疗方案具有重要意义,且术前直肠MRI评估对于术后病理学检查CRM阳性有预测意义[17-19]。本次报告数据表明,73.9%的直肠癌病人于术前行直肠MRI检查以评估肿瘤局部浸润范围及分期情况,这一结果提示,我国直肠癌诊疗体系中MRI规范化检查的普及率仍有待提升。不同医学中心间MRI检查率存在显著差异的主要原因可能归结于两点:其一为硬件资源不均,部分医疗机构仍缺乏符合精准分期要求的设备[如确保图像分辨率符合欧洲胃肠道和腹部放射学会(European Society of Gastrointestinal and Abdominal Radiology,ESGAR)分期标准[20]的3.0T MRI设备];其二为临床认知与实践差异,部分外科医师对MRI在评估CRM、EMVI以及新辅助治疗效果中的核心作用认识不足,且对标准化报告的解读缺乏系统培训。这种区域性差异可能直接影响直肠癌初始分期的准确性与治疗策略制定的同质性。
基于19 806例结直肠癌临床数据,我国围手术期治疗呈现新辅助治疗应用率偏低(所有病人中10.5%,直肠癌病人中16.0%,中、低位直肠癌病人中16.6%),而术后辅助治疗覆盖率>25.0%的现状,与“新辅助优先”的国际趋势相反[21-23]。特别是直肠癌,新辅助治疗可通过生物学降期、器官功能保全及预后改善三大机制发挥核心作用,同步放化疗、联合免疫治疗等方案可使直肠癌病理完全缓解(pCR)率提升至27.0%~78.4%,显著降低局部复发风险并延长生存期[21, 23-24]。当前亟须构建风险分层指导的精准治疗体系,通过多模态影像学评估、生物标记物检测及动态方案调整,推动治疗重心前移,最终实现结直肠癌疗效与生存质量的双重提升。
结直肠癌病人术后总体并发症发生率为8.4%,低于既往回顾性研究数据(10.1%)。与前两次阶段性报告结果存在显著差异的是,术后并发症的构成发生改变:SSI已不再占据首位并发症地位,当前最常见的术后并发症变为吻合口相关并发症吻合口漏,其发生率为2.0%。其中,以B级吻合口漏最为多见。进一步分析数据库中数据显示,中、低位直肠癌术后吻合口漏发生率为2.9%,其余部位(上段直肠癌及结肠癌)吻合口漏发生率为1.7%。值得注意的是,本次监测到的吻合口漏发生率较前期研究数据出现明显升高。经笔者分析推测,吻合口漏发生率上升的潜在关联因素可能与直肠癌病人行新辅助治疗(尤其是新辅助放化疗)的比例增加有关,此类治疗可能通过影响吻合口局部血供及组织愈合能力,进而增加吻合口漏的发生风险。
本次CCCD数据显示,中低位直肠癌新辅助治疗率为16.6%,吻合口漏发生率为2.9%,吻合口漏发生率显著低于既往文献报道数据(5.9%~13.6%)[14, 25-29]。该差异强烈提示数据库中存在字段填报缺失或不全,反映了数据质量仍有较大提升空间。为解决此问题,亟须各参与中心协同努力,确保数据的完整性与准确性。
全国性结直肠癌数据库意义重大。CCCD前瞻性登记数据覆盖广,根据本次报告的数据,可以看出当前结直肠癌治疗领域存在的问题,如直肠癌MRI检查普及率低,区域差异大,需从硬件和能力建设改进;同时,围手术期治疗与“新辅助优先”国际趋势存在反差。此外,在数据库数据录入方面也存在一些问题。如部分信息填写不准确、个别字段缺失较多,随访资料完整性较差等。在后续的结直肠癌数据库建设进程中,需着重聚焦于以下几个关键方面以提升数据库录入数据质量:(1)在全国范围内广泛招募更多具备资质的医学中心参与数据库的构建,以丰富数据库的层级结构,确保数据库能充分契合全国性数据库所要求的广泛性与代表性。(2)组织参与CCCD数据填报的各医学中心,就数据库字段规范化登记进行探讨及培训。重点明确并发症的登记范畴以及具体的诊断标准,以提升数据库中并发症数据的规范性与准确性。(3)持续优化并完善病例随访机制,为全面评估病人的长期预后提供可靠依据。(4)要持续高度重视数据安全问题,严格遵循相关法律法规,采取多重加密技术与严格的访问权限管理措施,切实保护病人的个人隐私信息。与此同时,为满足未来开展国际数据跨境比较研究的潜在需求,应提前做好数据格式标准化、兼容性处理等工作,以期为推动我国结直肠癌诊疗水平与国际接轨创造有利条件。
综上,CCCD为推动我国结直肠癌防治事业的发展奠定了坚实基础,积累了大量宝贵数据,为临床研究实施、指南制定等提供了关键支撑。然而,当前在直肠癌诊疗的诸多环节,如MRI检查普及、围手术期治疗模式等方面,仍与国际先进水平存在差距,数据库建设本身也面临数据质量提升等挑战。未来,CCCD建设将持续完善。广泛吸纳各方力量,强化数据规范化管理,优化随访机制,筑牢数据安全防线。相信在诸多同仁的共同努力下,CCCD必将成为引领我国结直肠癌精准防治的核心平台,助力我国结直肠癌诊疗水平向国际前沿迈进。
利益冲突 所有作者均声明不存在利益冲突
作者贡献声明 李杨、石晋瑶负责数据分析、初稿撰写及修订;李心翔、崔龙、张卫、池畔、王自强负责数据收集、资源支持;揭志刚、孙跃明、卢云、韩方海、何显力、陶凯雄、王权、王贵英、王振宁、李海、钱群、李乐平、卫洪波、李伟华、房学东负责研究执行、数据收集;姚宏伟负责质量控制、方法设计、审稿与修订、研究资源获取;张忠涛负责方法设计、审稿与修订、研究资源获取
参考文献
(在框内滑动手指即可浏览)
[1] Eng C, Yoshino T, Ruíz-García E, et al. Colorectal cancer [J]. Lancet, 2024, 404(10449): 294-310. DOI: 10.1016/S0140-6736(24)00360-X.
[2] Zheng R, Zhang S, Zeng H, et al. Cancer incidence and mortality in China, 2016 [J]. J Natl Cancer Center, 2022, 2(1): 1-9. DOI: 10.1016/j.jncc.2022.02.002.
[3] 姚宏伟, 李心翔, 崔龙, 等. 中国结直肠癌手术病例登记数据库2022年度报告: 一项全国性登记研究 [J]. 中国实用外科杂志, 2023, 43(1): 93-99. DOI:10.19538/j.cjps.issn1005-2208.2023.01.13.
[4] 姚宏伟, 李心翔, 崔龙, 等. 中国结直肠癌手术病例登记数据库2019年度报告: 一项全国性登记研究 [J]. 中国实用外科杂志, 2020, 40(1): 106-110+116. DOI: 10.19538/j.cjps.issn1005-2208.2020.01.19.
[5] Siegel RL, Kratzer TB, Giaquinto AN, et al. Cancer statistics, 2025 [J]. CA Cancer J Clin, 2025, 75(1): 10-45. DOI: 10.3322/caac.21871.
[6] Stafford LK, Gage A, Xu YY, et al. Global, regional, and national cascades of diabetes care, 2000-23: A systematic review and modelling analysis using findings from the Global Burden of Disease Study [J]. Lancet Diabetes Endocrinol, 2025, 13(11): 924-934. DOI: 10.1016/s2213-8587(25)00217-7.
[7] 国家卫生健康委员会. 结直肠癌筛查与早诊早治方案(2024年版) [J]. 消化肿瘤杂志(电子版), 2024, 16(4): 410-411. DOI:10.3969/j.issn.1674-7402.2024.04.003.
[8] Liang W, He J, Shen Y, et al. Impact of examined lymph node count on precise staging and long-term survival of resected non-small-cell lung cancer: A population study of the US seer database and a Chinese multi-institutional registry [J]. J Clin Oncol, 2017, 35(11): 1162-1170. DOI:10.1200/JCO.2016.67.5140.
[9] Epstein JI. Prostate cancer grade groups correlate with prostate-specific cancer mortality: SEER data for contemporary graded specimens [J]. Eur Urol, 2017, 71(5): 764-765. DOI: 10.1016/j.eururo.2016.12.014.
[10] Renfro LA, Sargent DJ. Findings from the Adjuvant Colon Cancer End Points (ACCENT) Collaborative Group: the power of pooled individual patient data from multiple clinical trials [J]. Chin Clin Oncol, 2016, 5(6): 80. DOI: 10.21037/cco.2016.12.02.
[11] Ozawa H, Kotake K, Ike H, et al. Prognostic impact of the length of the distal resection margin in rectosigmoid cancer: An analysis of the JSCCR database between 1995 and 2004 [J]. J Anus Rectum Colon, 2020, 4(2): 59-66. DOI: 10.23922/jarc.2019-013.
[12] Tomita N, Ishida H, Tanakaya K, et al. Japanese Society for Cancer of the Colon and Rectum (JSCCR) guidelines 2020 for the clinical practice of hereditary colorectal cancer [J]. Int J Clin Oncol, 2021, 26(8): 1353-1419. DOI: 10.1007/s10147-021-01881-4.
[13] Hashiguchi Y, Muro K, Saito Y, et al. Japanese Society for Cancer of the Colon and Rectum (JSCCR) guidelines 2019 for the treatment of colorectal cancer [J]. Int J Clin Oncol, 2020, 25(1): 1-42. DOI:10.1007/s10147-019-01485-z.
[14] 李杨, 任明扬, 张宏宇, 等. 经肛全直肠系膜切除术中困难或意外及术后并发症发生情况调查报告(一项基于全国性登记数据库的研究) [J]. 中国实用外科杂志, 2022, 42(11): 1260-1264. DOI:10.19538/j.cjps.issn1005-2208.2022.11.14.
[15] Li Z, Liu H, Luo S, et al. Long-term oncological outcomes of transanal versus laparoscopic total mesorectal excision for mid-low rectal cancer: A retrospective analysis of 2502 patients [J]. Int J Surg, 2024, 110(3): 1611-1619. DOI: 10.1097/JS9.0000000000000992.
[16] Zeng Z, Luo S, Zhang H, et al. Transanal vs laparoscopic total mesorectal excision and 3-year disease-free survival in rectal cancer: the TaLaR randomized clinical trial [J]. JAMA, 2025, 333(9): 774-783. DOI: 10.1001/jama.2024.24276.
[17] 姚宏伟, 张宏宇, 任明扬, 等. 经肛全直肠系膜切除术后病理标本环周切缘阳性危险因素分析:基于全国性病例登记数据库805例直肠癌研究结果 [J]. 中国实用外科杂志, 2020, 40(1): 111-116. DOI:10.19538/j.cjps.issn 1005-2208.2020.01.20.
[18] Horvat N, Carlos TRC, Clemente OB, et al. MRI of rectal cancer: Tumor staging, imaging techniques, and management [J]. Radiographics, 2019, 39(2): 367-387. DOI: 10.1148/rg.2019180114.
[19] Feng Y, Hu T, Gu W, et al. Mesorectal fascia involvement by tumor deposits or extramural vascular invasion at MRI predicts prognosis in rectal cancer [J]. Radiology, 2025, 317(1): e243627. DOI: 10.1148/radiol.243627.
[20] Boraschi P, Donati F, Cervelli R, et al. MR staging of rectal cancer: Comparison between the 2012 and 2016 European Society of Gastrointestinal and Abdominal Radiology (ESGAR) Guidelines [J]. Eur J Radiol, 2024, 181: 111804. DOI:10.1016/j.ejrad.2024.111804.
[21] Cercek A, Lumish M, Sinopoli J, et al. PD-1 blockade in mismatch repair-deficient, locally advanced rectal cancer [J]. N Engl J Med, 2022, 386(25): 2363-2376. DOI: 10.1056/NEJMoa2201445.
[22] Chalabi M, Verschoor YL, Tan PB, et al. Neoadjuvant immunotherapy in locally advanced mismatch repair-deficient colon cancer [J]. N Engl J Med, 2024, 390(21): 1949-1958. DOI: 10.1056/NEJMoa2400634.
[23] Wang F, Chen G, Qiu M, et al. Neoadjuvant treatment of IBI310 plus sintilimab in locally advanced MSI-H/dMMR colon cancer: A randomized phase 1b study [J]. Cancer Cell, 2025, 43(10): 1958-1967. DOI:10.1016/j.ccell.2025.09.004.
[24] Lin ZY, Zhang P, Chi P, et al. Neoadjuvant short-course radiotherapy followed by camrelizumab and chemotherapy in locally advanced rectal cancer (UNION): Early outcomes of a multicenter randomized phase Ⅲ trial [J]. Ann Oncol, 2024, 35(10): 882-891. DOI: 10.1016/j.annonc.2024.06.015.
[25] Degiuli M, Elmore U, De Luca R, et al. Risk factors for anastomotic leakage after anterior resection for rectal cancer (RALAR study): A nationwide retrospective study of the Italian Society of Surgical Oncology Colorectal Cancer Network Collaborative Group [J]. Colorectal Dis, 2022, 24(3): 264-276. DOI:10.1111/codi.15997.
[26] Yi X, Chen C, Diao J, et al. Clinical prediction model for anastomotic leakage in rectal cancer surgery: A single-center large-sample cohort study [J]. Surg Endosc, 2025, 39(7): 4345-4356. DOI: 10.1007/s00464-025-11821-2.
[27] Ochiai K, Hida K, Yamaguchi T, et al. Risk factors for and oncologic impact of anastomotic leakage after sphincter-preserving proctectomy for mid/low rectal cancer: A multi-institutional cohort study in Japan [J]. Ann Surg Oncol, 2025, 32(10): 7315-7325. DOI: 10.1245/s10434-025-17763-2.
[28] Jayne D, Pigazzi A, Marshall H, et al. Effect of robotic-assisted vs conventional laparoscopic surgery on risk of conversion to open laparotomy among patients undergoing resection for rectal cancer: The ROLARR randomized clinical trial [J]. JAMA, 2017, 318(16): 1569-1580. DOI:10.1001/jama.2017.7219.
[29] Penna M, Hompes R, Arnold S, et al. Transanal total mesorectal excision: international registry results of the first 720 cases [J]. Ann Surg, 2017, 266(1): 111-117. DOI: 10.1097/SLA.0000000000001948.
【引用本文】李 杨,李心翔,崔 龙,等. 中国结直肠癌手术病例登记数据库2025年度报告:一项全国性前瞻性登记研究[J]. 中国实用外科杂志,2026,46(2):239-246.
DOI:10.19538/j.cjps.issn1005-2208.2026.02.15