国产ADC崛起:从Cancer Cell到ESMO亚洲年会,三款重磅新药有望重塑实体瘤治疗格局
发布时间:2026-04-16来源:药事纵横
肺癌、乳腺癌等实体瘤长期以来占据全球恶性肿瘤发病率和死亡率的前列。尽管近年来靶向治疗和免疫治疗取得了长足进步,但针对特定靶点突变或表达异常的晚期患者,传统疗法仍面临缓解率低、耐药性强及生存期短等严峻挑战。在这一背景下,抗体药物偶联物(ADC)凭借其“精准制导+强力杀伤”的独特机制,成为了肿瘤治疗领域的破局之光。ADC药物由靶向特异性抗原的单克隆抗体、高活性的细胞毒性载荷以及连接两者的连接子三部分构成。这种精巧的结构使得ADC能够像“生物导弹”一样,在血液中稳定循环并精准识别肿瘤细胞表面的抗原,通过内吞作用进入细胞内部,随后释放毒素诱导肿瘤细胞死亡。近年来,中国创新药企在ADC领域的研发势头强劲,多款国产ADC在关键临床试验中展现出不亚于甚至超越跨国药企同类药物的卓越疗效与安全性。近期,从国际顶级学术期刊Cancer Cell、Signal Transduction and Targeted Therapy,到欧洲肿瘤内科学会亚洲年会(ESMO-Asia),三款分别靶向B7-H3、HER2以及EGFR/HER3的国产ADC新药(HS-20093、SHR-A1811、T-Bren/Iza-bren)接连公布了重磅临床数据。本文将深入剖析这三款药物的分子机制与临床结果,客观探讨国产ADC如何引领实体瘤治疗的下一个浪潮。(一)HS-20093:靶向B7-H3破局肺癌治疗困境
1.药物作用机制
B7-H3(CD276)是一种I型跨膜免疫检查点分子。在生理状态下,B7-H3在正常组织中的表达极低;但在病理状态下,其在非小细胞肺癌(NSCLC)和小细胞肺癌(SCLC)中均呈现异常高表达。这种极度受限的正常组织表达与广泛的肿瘤高表达特征,使得B7-H3成为ADC药物开发的“理想靶点”,能够最大程度保证靶向特异性并降低脱靶毒性。HS-20093(Risvutatug Rezetecan)是由翰森制药自主研发的靶向B7-H3的ADC药物。在分子设计上,HS-20093采用全人源单克隆抗体,通过一种可响应肿瘤微环境的可裂解连接子,将拓扑异构酶I抑制剂(TOP1i)作为有效载荷进行偶联,其平均药物抗体比(DAR)为4。当HS-20093结合肿瘤细胞表面的B7-H3并被内吞进入溶酶体后,连接子在特定微环境下降解,释放出TOP1i,通过阻断DNA复制和转录,引发肿瘤细胞凋亡。2.临床研究结果
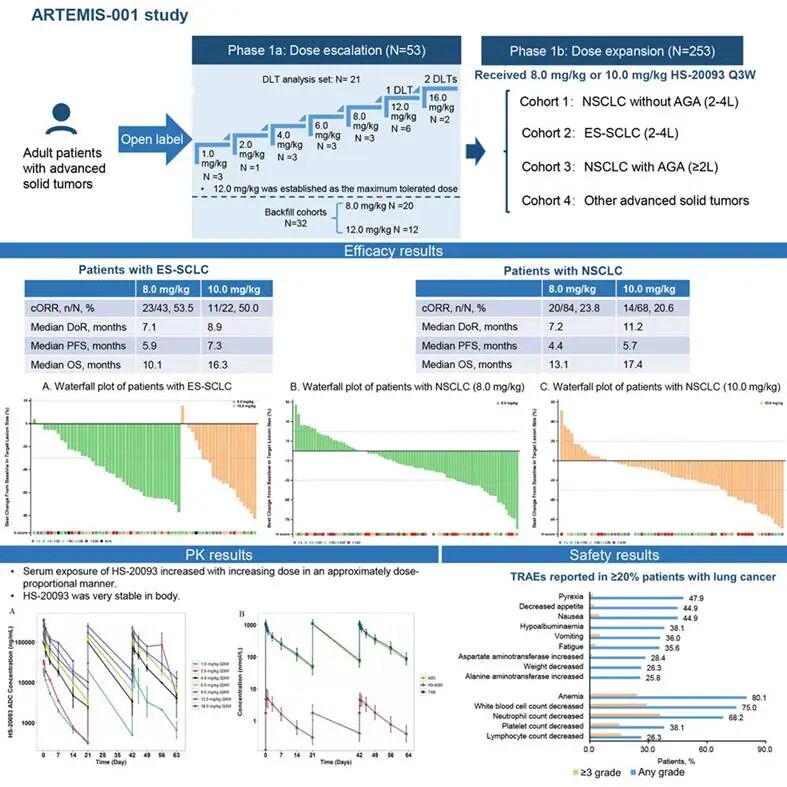
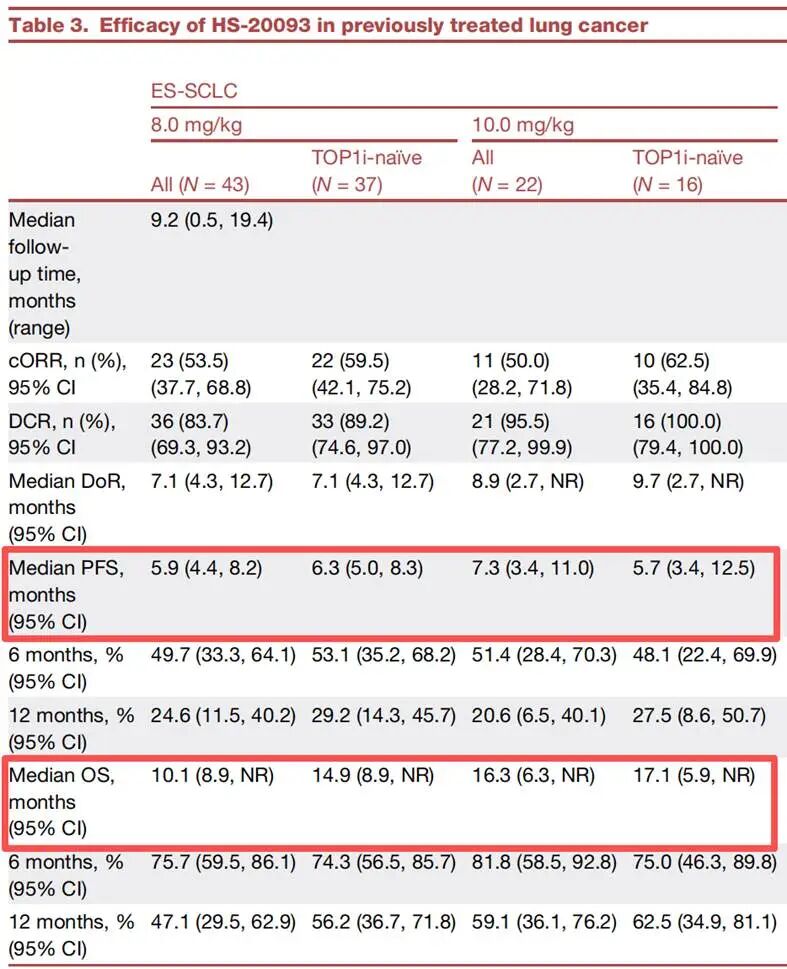
2026年3月,中国医学科学院肿瘤医院王洁教授、段建春教授团队在Cancer Cell上发表了HS-20093的ARTEMIS-001(1a/1b期)临床研究数据。该研究共纳入306名既往接受过治疗的晚期实体瘤患者,重点评估了其在肺癌中的疗效与安全性。在疗效方面,HS-20093展现出强大的抗肿瘤活性。在可评估的广泛期小细胞肺癌(ES-SCLC)患者中(N=65),确认客观缓解率(ORR)高达52.3%,疾病控制率为 87.7%。。考虑到SCLC是一种侵袭性极强、极易复发且缺乏有效后线靶向治疗的恶性肿瘤,这一数据尤为瞩目。在非小细胞肺癌(NSCLC)患者中(N=152),确认ORR也达到了22.4%。研究同时证实,8.0 mg/kg和10.0 mg/kg剂量组的ORR相近。图1. ARTEMIS-001临床研究结果图2. 疗效结果在安全性方面,临床前研究提示的高体内稳定性在临床试验中得到了验证——其有效载荷的血清暴露量极低,表明毒素在血液中过早释放的情况很少。在236名接受8.0或10.0 mg/kg剂量治疗的肺癌患者中,最常见的3级及以上治疗相关不良事件(TRAE)为血液学毒性,包括中性粒细胞减少(25.5% vs 50.5%)、白细胞计数减少(19.7% vs 42.4%)和贫血(16.8% vs 34.3%)。值得临床关注的是,治疗相关间质性肺病(ILD)发生率为3.4%,导致死亡的不良事件率为3.8%。综合疗效与安全性数据,8.0 mg/kg被确立为后续3期临床试验的推荐剂量。该研究确立了HS-20093在难治性肺癌中的治疗潜力。(二)SHR-A1811:优化载荷设计,挑战HER2靶向治疗极限
1.药物作用机制
人类表皮生长因子受体-2(HER2)的异常激活与乳腺癌、胃癌、非小细胞肺癌等多种实体瘤的发病机制密切相关。以德曲妥珠单抗(T-DXd)为代表的抗HER2 ADC虽然取得了巨大成功,但在临床实践中仍面临两大痛点:一是间质性肺病(ILD)发生率较高且存在致死风险;二是肿瘤耐药机制的涌现限制了持久响应。恒瑞医药自主研发的SHR-A1811(瑞康曲妥珠单抗,艾维达)在机制上进行了针对性的优化。该药物同样以曲妥珠单抗为抗体骨架,通过可裂解连接子偶联了新型拓扑异构酶I抑制剂有效载荷SHR169265。与T-DXd相比,SHR-A1811的载荷在膜通透性和细胞杀伤效力上表现更优,从而赋予了药物更强的“旁观者效应”——即不仅能够杀死表面高表达HER2的肿瘤细胞,还能杀伤周围低表达或不表达HER2的肿瘤细胞,这对于异质性极高的实体瘤至关重要。此外,SHR-A1811将药抗比(DAR)设定为适中的6,并在连接子稳定性上进行了深度改良。临床前数据显示,其循环中释放的极少量毒素(有效载荷释放率低于1%)共同奠定了其高稳定性的基础,从机制层面降低了脱靶毒性和ILD的发生风险。2.临床研究结果
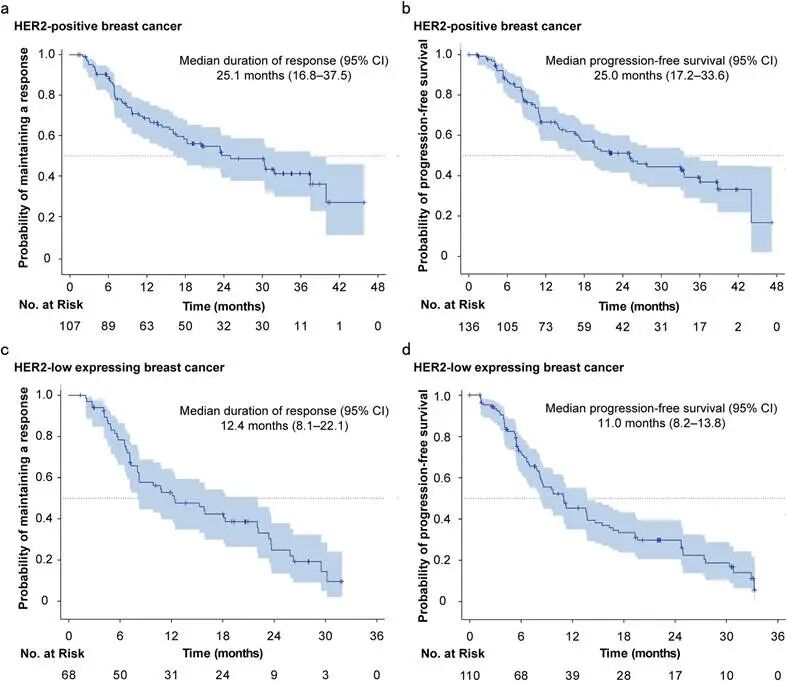
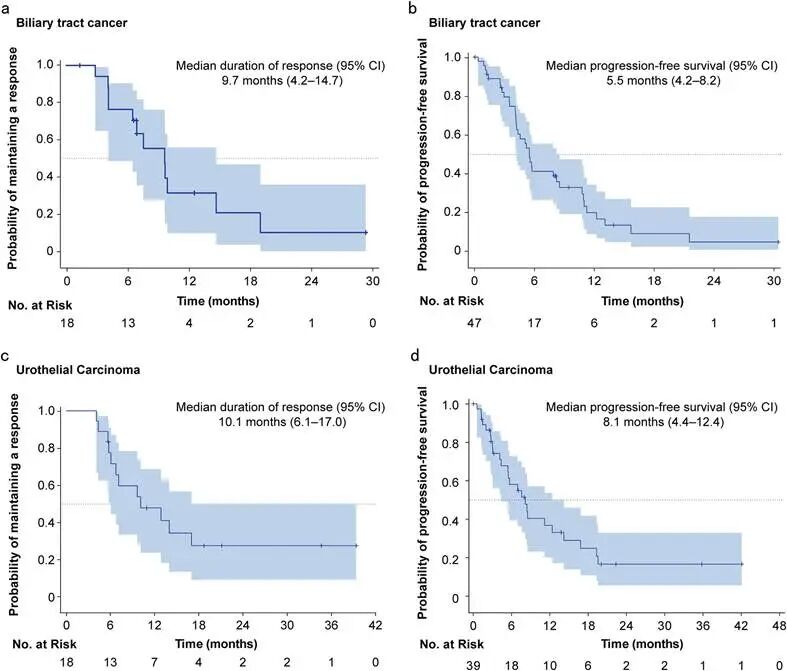
2026年3月,中山大学孙逸仙纪念医院宋尔卫院士团队在Signal Transduction and Targeted Therapy上发表了SHR-A1811的HORIZON-X全球多中心1期临床试验最终分析结果。该研究在38家医院纳入了396例既往接受过2-4线治疗的晚期HER2表达或突变实体瘤患者。在疗效方面,SHR-A1811展现了令人瞩目的长期生存获益。在HER2阳性乳腺癌患者中,中位无进展生存期(PFS)达25.0个月;在HER2低表达乳腺癌患者中,中位PFS也达到了11.0个月。图3. 乳腺癌患者无进展生存期和缓解持续时间结果此外,在非乳腺癌领域(如胆道癌、尿路上皮癌等),中位PFS范围为3.5至17.2个月。这种跨瘤种的显著疗效,再次印证了HER2作为泛实体瘤治疗靶点的价值,以及SHR-A1811优异的旁观者杀伤效应。图4. 非乳腺癌患者的无进展生存期和缓解持续时间结果在安全性方面,SHR-A1811证明了其机制优化的临床转化价值。整体队列中,65.9%的患者出现3级及以上TRAE,但任何级别的间质性肺病(ILD)发生率仅为2.5%,显著低于已上市的某些同类HER2 ADC药物(既往部分药物ILD发生率超10%)。极低的ILD发生率结合卓越的PFS数据,使得SHR-A1811有望成为HER2靶向治疗中更具优势的替代方案。(三)T-Bren登陆ESMO-Asia:零间质性肺病,新型HER2 ADC重塑非小细胞肺癌治疗格
在非小细胞肺癌(NSCLC)的靶向治疗领域,HER2突变患者(约占2%-4%)长期面临后方乏力的困境。传统化疗及免疫治疗的客观缓解率有限,且容易产生耐药。而在近期公布的2025年新加坡欧洲肿瘤内科学会亚洲年会(ESMO-Asia)上,由百利天恒研发的新型HER2抗体偶联药物(ADC)T-Bren(BL-M07D1)携惊艳数据登场,为HER2突变晚期NSCLC患者带来了具有突破性的治疗新选择。1.药物作用机制
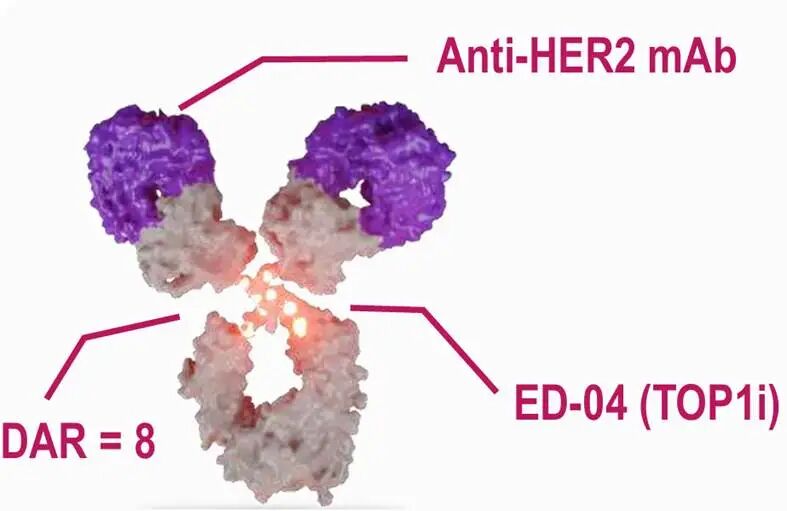
T-Bren之所以被称为“精准抗癌导弹”,源于其精妙的分子架构设计。该药物由三大核心组件构成:人源化抗HER2抗体、组织蛋白酶B可裂解连接子以及新型拓扑异构酶I抑制剂(Ed-04)。在靶向识别阶段,抗HER2抗体如同制导系统,能够精准锚定带有HER2标志物的肿瘤细胞。这种特异性结合不仅实现了对肿瘤的物理定位,还能激活患者自身的免疫系统,形成“药物直接杀伤+免疫细胞攻击”的双重抗肿瘤机制。图5. T-Bren(BL-M07D1)药物结构示意图在杀伤阶段,药物被内吞进入肿瘤细胞后,连接子在特定酶的作用下断裂,释放出高活性的Ed-04毒素。该毒素能直接破坏癌细胞DNA,阻断其增殖。更关键的是,T-Bren具备卓越的“旁观者效应”,释放的毒素能够穿透细胞膜,对邻近即使HER2表达水平较低的癌细胞也产生杀伤,从而有效克服了肿瘤内部异质性带来的治疗盲区。在安全性设计上,T-Bren引入了创新的酸性稳定基团。这一设计确保了药物在血液的中性环境中保持极高稳定性,避免毒素提前释放造成的脱靶损伤;只有在进入肿瘤细胞内部的酸性微环境中,连接子才会被触发断裂。这种“酸控释放”机制将治疗窗口最大化,从源头提升了用药安全性。2.临床研究结果
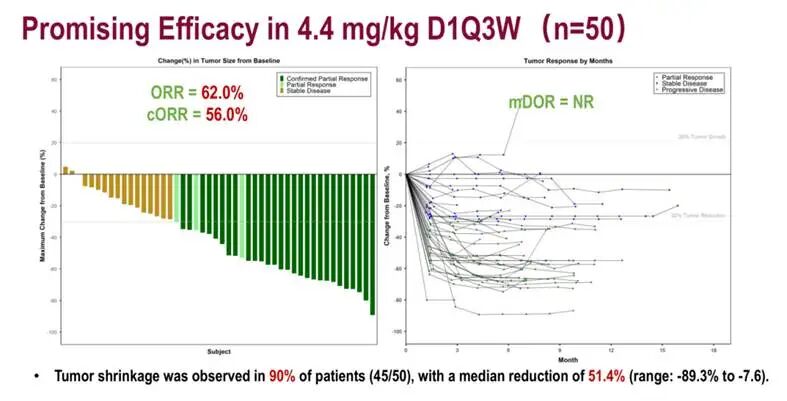
在本次ESMO-Asia大会上公布的BL-M07D1-201研究,是一项针对既往经治的HER2突变晚期NSCLC患者开展的单臂、多中心Ⅱ期临床试验。其疗效数据展现了极强的疾病控制力:首先是肿瘤缓解深度极佳。在50例接受4.4 mg/kg剂量治疗的患者中,客观缓解率(ORR)高达62.0%,经独立评审委员会确认的客观缓解率也达到了56.0%。这意味着超过六成的难治性晚期患者,其肿瘤病灶出现了超过30%的显著缩小。其次是疾病控制率(DCR)高达96.0%。绝大多数患者的病情在用药后得到了有效遏制,阻断了癌细胞进一步“疯长”的进程。图6. T-Bren(BL-M07D1)短期疗效结果最令人瞩目的在于其长期的生存获益。数据显示,患者1年无进展生存(PFS)率达到73.5%,且中位PFS尚未达到,提示疗效持续时间极长;同时,1年总生存(OS)率高达86.2%。中位缓解持续时间同样未达到。这些指标共同印证了T-Bren不仅起效迅速,更能为患者提供持久的疾病控制期。此外,在备受关注的ADC类药物安全性方面,T-Bren交出了一份极其优异的答卷:研究中未观察到任何级别的间质性肺病(ILD)病例且无新的非预期严重安全信号,排除了这一高危致命副作用的临床顾虑;其发生率超20%的常见不良反应主要为贫血、血小板减少等血液学毒性及恶心、乏力等消化道与全身反应,绝大多数为轻中度且症状温和,通常无需强化医疗干预即可保证患者良好的耐受性;此外,少数3级及以上严重不良事件多属血液学相关,通过常规剂量调整或对症治疗即可有效控制,因不良反应导致永久停药的比例低至3.4%,远优于同类药物历史数据,这从根本上确保了绝大多数患者能够持续用药,不因毒副作用而错失长期生存获益。(四)总结
综上所述,从靶向泛肿瘤标志物B7-H3的HS-20093在难治性小细胞肺癌中斩获超50%的客观缓解率,到SHR-A1811通过优化载荷结构在HER2阳性乳腺癌中创下25个月的中位无进展生存期并大幅降低间质性肺病风险,再到T-Bren以“零ILD”和73.5%的1年PFS率在HER2突变肺癌中展现同类最佳潜力——这三款国产ADC新药的临床进展,不仅是单点药物的突破,更是中国创新药研发体系在ADC底层逻辑(靶点选择、连接子优化、载荷创新、双抗融合)上全面成熟的缩影。当前,现代肿瘤学正加速迈入“精准递送”时代,相较于传统化疗的“无差别杀伤”和单抗的“信号阻断”,ADC药物真正实现了将强效化疗武器精确空投至肿瘤内部。中国药企在这一轮技术周期中,不仅紧跟国际前沿,更在安全性控制(如降低ILD发生率)和双抗架构创新上实现了“弯道超车”。随着这三款药物及其后续管线的3期临床试验推进与适应症拓展,国产ADC有望在全球实体瘤治疗格局中扮演更加核心的角色,从而为广大晚期肿瘤患者带来更长生存期与更高质量生活的双重希望。[1] Duan J, Sun Y, Wang Q, et al. HS-20093, a B7-H3-targeted antibody-drug conjugate in lung cancer: Results from the ARTEMIS-001 phase 1a/b trial. Cancer Cell. 2026 Mar 5:S1535-6108(26)00104-2. doi: 10.1016/j.ccell.2026.02.006.[2] Yao H, Yan M, Tong Z, et al. SHR-A1811, a novel HER2-targeting antibody-drug conjugate, in advanced solid tumors (HORIZON-X): a global phase 1 trial. Signal Transduct Target Ther. 2026 Mar 19;11(1):104. doi: 10.1038/s41392-026-02612-9.[3] Xue J, el. BL-M07D1, a novel anti-HER2 antibody-drug conjugate (ADc), in subjects with metastaic HER2-mutant non-smalcellung cancer (NSCLC). 2025 ESMO Asia. 160MO.[4] Li X, Zhao C, Su C, et al. Epidemiological study of HER-2 mutations among EGFR wild-type lung adenocarcinoma patients in China. BMC Cancer. 2016 Oct 28;16(1):828. doi: 10.1186/s12885-016-2875-z.[5] Saalfeld FC, Wenzel C, Christopoulos P, et al. Efficacy of Immune Checkpoint Inhibitors Alone or in Combination With Chemotherapy in NSCLC Harboring ERBB2 Mutations. J Thorac Oncol. 2021 Nov;16(11):1952-1958. doi: 10.1016/j.jtho.2021.06.025.[6] Wang Y, Zhang S, Wu F, et al. Outcomes of Pemetrexed-based chemotherapies in HER2-mutant lung cancers. BMC Cancer. 2018 Mar 27;18(1):326. doi: 10.1186/s12885-018-4277-x.作者介绍:Ketty,主要从事药物研发和科普,制药行业政策和发展研究
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。