【药渡每周渡选-创新药篇】吉利德50亿美元收购德国ADC新锐;纽瑞特医疗完成10亿元E轮融资创核药领域新高……
发布时间:2026-04-15来源:药渡


全球生物医药行业动态
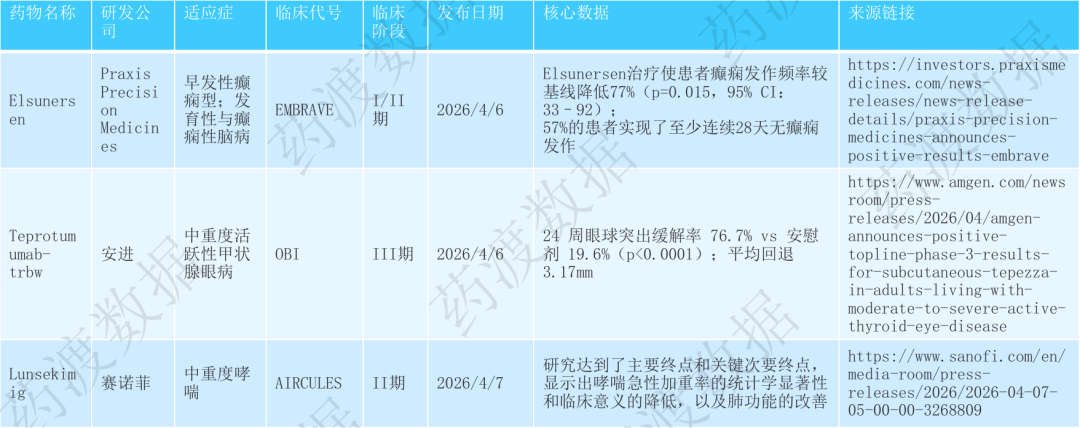
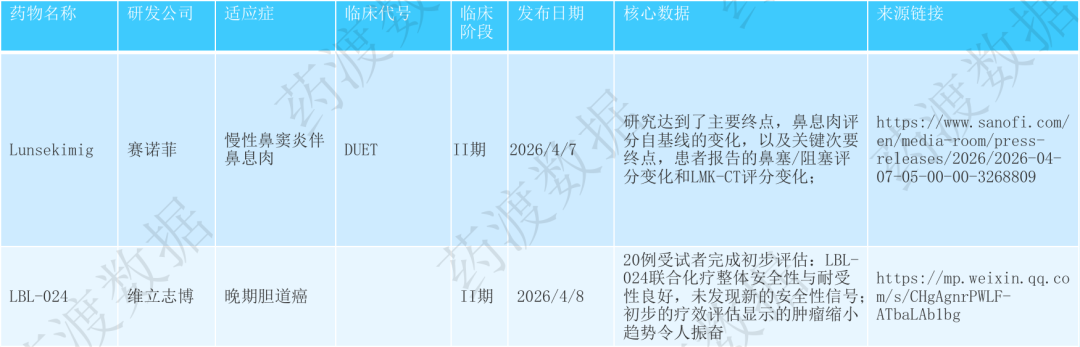
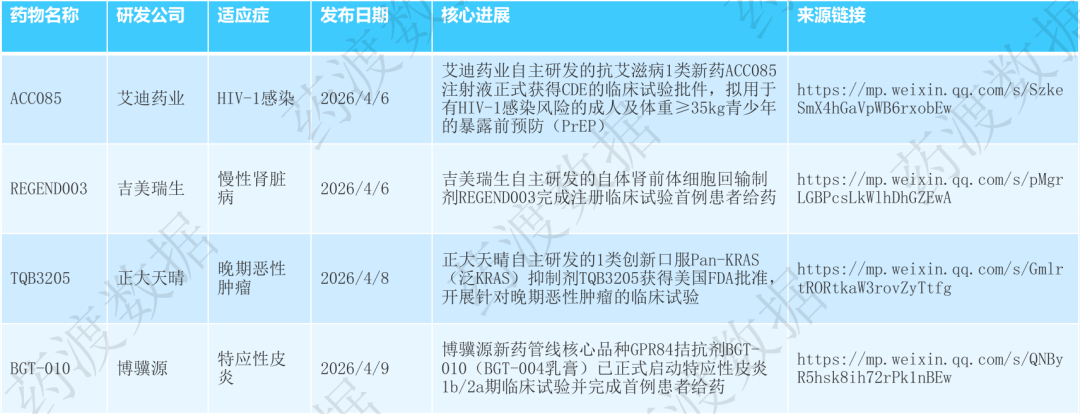
产业合作与融资并购密集落地:吉利德以50亿美元收购德国ADC新锐Tubulis加强肿瘤产品线;纽瑞特医疗完成10亿元E轮融资创核药领域单轮融资新高;原启生物完成1.1亿美元Pre-IPO轮融资推进肝细胞癌CAR-T药物;蔚程医药超额完成5400万美元A轮融资加速肝外递送小核酸疗法;美赛生物完成超1.5亿人民币A轮融资专注巨噬细胞靶点药物开发;迈威生物港股IPO通过聆讯实现A+H布局;天演药业与Incyte合作评估CTLA-4单抗联合TGFβR2/PD-1双抗治疗结直肠癌;甘李药业与JW制药就GLP-1RA双周制剂达成8110万美元独家许可合作;轩竹生物两款自研新药超1亿美元授权出海中东及北非;安斯泰来1500万美元引进AI设计AAV衣壳;康桥资本、合肥国资借道云顶新耀2.5亿美元退出海森生物;武田终止Denali合作归还FTD疗法DNL593并裁员634人;汇伦医药递表港交所。代谢、肿瘤、神经等领域频传佳音:Praxis公司Elsunersen治早发性癫痫I/II期癫痫发作频率降低77%,57%患者实现28天无发作;安进Teprotumumab治中重度甲状腺眼病III期眼球突出缓解率76.7%;赛诺菲Lunsekimig治中重度哮喘及慢性鼻窦炎伴鼻息肉II期双适应症达主要终点;维立志博LBL-024治晚期胆道癌II期显示肿瘤缩小趋势;艾迪药业ACC085获IND批件用于HIV暴露前预防;吉美瑞生REGEND003完成慢性肾脏病注册临床首例给药。药企资本化提速,研发模式持续升级:迈威生物、汇伦医药、靖因药业等多家企业推进港股IPO;泰诺麦博冲刺科创板核心产品上市首年销售5122万元;多家企业加码核心技术平台研发,聚焦ADC、核药、小核酸、细胞治疗等方向;吉利德、武田等MNC通过并购或收缩优化管线布局,标志着平台化授权与战略聚焦已成为行业升级核心驱动力。

全球创新药
重要投融资与交易事件
2025年4月6日-4月12日,全球生物医药领域交易与投融资持续活跃,涵盖7起重磅交易授权与战略合作——包括吉利德50亿美元收购德国ADC新锐Tubulis加强肿瘤产品线、天演药业与Incyte合作评估CTLA-4单抗联合TGFβR2/PD-1双抗治疗结直肠癌、甘李药业与JW制药就GLP-1RA双周制剂达成8110万美元独家许可合作、轩竹生物两款自研新药超1亿美元授权出海中东及北非、安斯泰来1500万美元引进AI设计AAV衣壳、康桥资本与合肥国资借道云顶新耀2.5亿美元退出海森生物、武田终止Denali合作归还FTD疗法DNL593并裁员634人;以及7起重大投融资事件——涉及纽瑞特医疗10亿元E轮融资创核药领域单轮融资新高、原启生物1.1亿美元Pre-IPO轮融资推进肝细胞癌CAR-T药物、蔚程医药超额完成5400万美元A轮融资加速肝外递送小核酸疗法、美赛生物完成超1.5亿人民币A轮融资专注巨噬细胞靶点药物开发、迈威生物港股IPO通过聆讯实现A+H布局、汇伦医药递表港交所、北辰生物完成Pre-A轮融资;交易聚焦ADC、核药、小核酸、细胞治疗、GLP-1、AI制药等领域,集中体现跨国药企通过巨额并购优化管线布局、双特异性抗体及联合疗法持续受市场追捧、核药与小核酸等前沿疗法获资本持续加注、中国创新药企通过港股IPO及NewCo模式加速国际化与资本化进程,同时行业战略收缩与聚焦成为理性选择。
动态:4月完成10亿元E轮融资,上海科创集团、上海国鑫、南京高科新浚共同领投,上海科创集团旗下知识产权基金、鼎泰星、中启资本等十余家机构跟投,公司已于2025年1月启动A股IPO辅导。意义:此次融资规模创下国内核药领域单轮融资新高,若后续顺利上市,纽瑞特医疗或将成为四川首家本土核医疗领域上市公司,体现核药赛道持续获资本加注。动态:4月10日累计完成1.1亿美元Pre-IPO轮融资,维梧资本、北京市医药健康产业投资基金、启明创投及一家全球领先医疗基金共同领投,国际主权基金、亦庄国投、鲁信创投、NGS、骊宸投资、瑞锋资本等知名机构跟投。意义:资金用于推进核心产品Ori-C101靶向GPC3自体CAR-T药物关键性临床试验,该产品有望成为全球首款获批上市的针对肝细胞癌的CAR-T药物,体现细胞治疗前沿疗法持续获资本青睐。动态:4月10日超额完成5400万美元A轮融资,启明创投与一家知名产业基金联合领投,弘晖基金、一家知名投资基金、泰福资本共同参与,原有投资方杏泽资本持续追加投资。意义:资金用于核心肝外递送技术平台迭代优化、多条管线临床推进及全球研发网络搭建,专注肝外靶向小核酸药物研发,体现小核酸赛道差异化布局价值。动态:4月2日完成超1.5亿元A轮融资,康君资本领投,宏沣投资、瑞华资本、行业头部投资机构和知名产业基金共同参与。意义:资金用于巨噬细胞靶点发现与验证、抗体药物临床转化,聚焦自身免疫性疾病与肿瘤两大领域,体现以巨噬细胞为核心研究对象的创新靶点开发受市场关注。动态:近日完成Pre-A轮融资,启迪之星创投领投,众合益资本担任独家财务顾问。意义:资金用于核心技术研发升级、产品产业化推进及市场拓展,专注抗菌微生态与生物医药领域,体现微生物组学赛道创新潜力。动态:4月通过港交所聆讯,拟在香港主板上市,此前于2026年3月25日递表,实现A+H双资本市场布局。意义:公司拥有15个处于临床前、临床或上市阶段的重点品种,其中11个为创新品种、4个为生物类似药,已有4个品种成功上市,体现中国创新药企国际化资本化进程加速。动态:近期完成数亿元战略融资,倚锋资本领投,拱墅国投与宏诚资本跟投,同步完成工商迁址落户杭州市拱墅区。意义:资金用于全球首个CRISPR抗病毒基因编辑药物BD111 II期临床、BD211地贫项目转化及BD312青光眼、BD115生殖器疱疹IND申报,体现基因编辑疗法临床转化提速。
动态:4月7日宣布以31.5亿美元现金预付款加最高18.5亿美元里程碑付款收购德国ADC新锐Tubulis全部已发行股权,交易总金额最高可达50亿美元,预计2026年第二季度完成。意义:Tubulis专注开发下一代抗体药物偶联物(ADC),此次收购将显著加强吉利德肿瘤产品线,聚焦高度未满足需求领域,体现跨国药企通过巨额并购加速ADC赛道布局。- 甘李药业与JW制药 —— 8110万美元独家许可合作
动态:4月8日与韩国头部药企JW Pharmaceutical签署独家许可协议,就GLP-1RA双周制剂博凡格鲁肽注射液在韩国的临床开发、注册申报及商业化开展合作。意义:甘李药业将获得500万美元首付款及总计7610万美元里程碑付款,潜在交易总金额高达8110万美元,体现中国创新药企GLP-1产品出海授权能力增强。- 轩竹生物与Boston Oncology —— 超1亿美元授权合作
动态:4月9日与Boston Oncology就两款1类创新药吡洛西利片及地罗阿克片达成独家授权许可及供货协议,授权区域覆盖中东及北非地区超20个国家。意义:轩竹生物将获得首付款和后续可能累计超1亿美元的监管和商业里程碑付款,以及授权区域内销售总额的固定比例特许权使用费,体现中国创新药出海中东及北非等新兴市场突破。
- 安斯泰来引进Dyno AAV衣壳 —— 1500万美元
动态:近日安斯泰来行使许可权,引进一种利用人工智能设计的用于骨骼肌治疗递送的新型腺相关病毒(AAV)衣壳,Dyno将获得1500万美元许可费。意义:此次授权是行业内首次有生物技术公司成功将"AI设计的AAV衣壳"对外授权,用于中枢神经系统和肌肉靶向递送,体现AI技术在基因治疗递送系统中的商业化突破。动态:4月8日云顶新耀新加坡全资附属公司与海森生物制药(亚洲)签署股权购买协议,以2.5亿美元总对价收购海森新加坡公司100%股权,获得亚太地区14种品牌慢性病产品商业化权利。意义:该交易实际为康桥资本、合肥国资等资方借道云顶新耀实现投资部分退出,体现PE/VC通过并购交易实现退出的创新模式。- 武田终止Denali合作 —— 归还DNL593权益
动态:近日武田制药宣布终止与Denali Therapeutics的合作,归还FTD疗法DNL593的全球开发和商业化权利,同时在美国裁员634人。意义:面对神经退行性疾病高达99.6%的III期临床试验失败率,武田通过战略收缩实现每年超2000亿日元成本节约目标,体现药企理性评估风险收益比、壮士断腕成为行业趋势。
- 天演药业与Incyte合作 —— 联合治疗结直肠癌
动态:4月2日宣布与Incyte达成临床合作,评估CTLA-4单抗muzastotug与TGFβR2×PD-1双特异性抗体INCA33890联合治疗微卫星稳定型结直肠癌疗效,Incyte将出资并运营该项研究。意义:此前muzastotug联合KEYTRUDA在三线MSS结直肠癌中显示令人鼓舞的客观缓解率,此次合作体现双特异性抗体联合免疫治疗在难治性肿瘤中的探索价值。
2026 年 4 月 6 日 - 12 日,国内创新药在抗肿瘤、心血管、细胞治疗等领域迎来多项关键进展,多款 First-in-class / 全球首创药物获批上市或临床,同时突破性治疗品种公示加速临床急需药物研发。
详情:经优先审评程序获 NMPA 附条件批准,用于既往接受过至少 2 种系统性(包括含铂化疗)失败的广泛期小细胞肺癌(ES-SCLC)成人患者。是全球首个且目前唯一获批的靶向 DLL3 和 CD3 的双特异性 T 细胞衔接器(TCE),为小细胞肺癌后线治疗提供全新治疗选择。详情:1 类化药获批上市,为心脏负荷试验药物,适用于核素心肌灌注显像(MPI)以评估心肌缺血,历时 20 年研发,填补国内相关领域空白。详情:获批上市,用于治疗重度嗜酸性粒细胞性哮喘,为重度哮喘患者提供新的靶向治疗选择。- GKL-006Allo 注射液(异体通用现货型 iNKT 细胞注射液)
详情:1 类创新药 IND 申请获 CDE 临床试验默示许可,拟用于经标准治疗失败或不耐受的强直性脊柱炎,是国内 iNKT 细胞疗法在自身免疫病领域的重要突破。日期:2026 年 4 月上旬(4 月 6-12 日区间内)详情:小分子药物 IND 申请获 NMPA 批准,用于治疗腓骨肌萎缩症(CMT),是国内首款针对腓骨肌萎缩症的 1 类创新药,计划于 2026 年第一季度开启 I 期临床试验。详情:CDE 官网公示拟纳入突破性治疗品种,适应症为含铂化疗及 PD-(L) 1 抑制剂治疗失败的复发或转移性宫颈癌。该药物有效载荷为拓扑异构酶Ⅰ抑制剂,通过靶向 Nectin-4 在肿瘤组织中的高表达实现精准杀伤,加速其临床研发与上市进程。
2026 年 4 月 6 日 - 12 日,FDA 在仿制药提速、监管政策优化等方面发布重要信号,同时完成多款创新药审评决策,推动全球创新药研发与可及性提升。
日期:2026 年 4 月 6 日(PDUFA 目标日期)详情:异基因 T 细胞免疫疗法,用于治疗血液系统恶性肿瘤,此前已获 FDA 授予生物制品许可申请(BLA)优先审评资格,于 PDUFA 日期完成审评决策,为血液肿瘤患者提供全新细胞治疗选择。- “快速 IND(Expedited IND)” 新路径
详情:FDA 宣布计划引入全新的 “快速 IND” 路径,替代传统 IND 途径用于部分 I 期临床试验。该路径适用于可通过新替代试验法(NAMS)满足监管标准的临床前数据,在保障安全性与伦理标准的前提下,大幅加速早期临床试验启动,降低研发成本。详情:FDA 联合 EMA、MHRA 发布重磅监管信号,推进 AI 药物研发监管制度化,同时强化仿制替代提速与药物安全监测,为 AI 驱动的创新药研发提供清晰监管框架。

转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。