【识林心得】“这是给我‘返回’到哪儿来了?”
本文通过五个典型场景,展示这一小按钮如何帮助识林用户快速定位文件来源、查阅配套资料、追溯法规沿革,让每一次“返回”都变得更有价值。
场景1:从欧美GAiP【返回】EMA的AI索引,一览EMA的AI布局
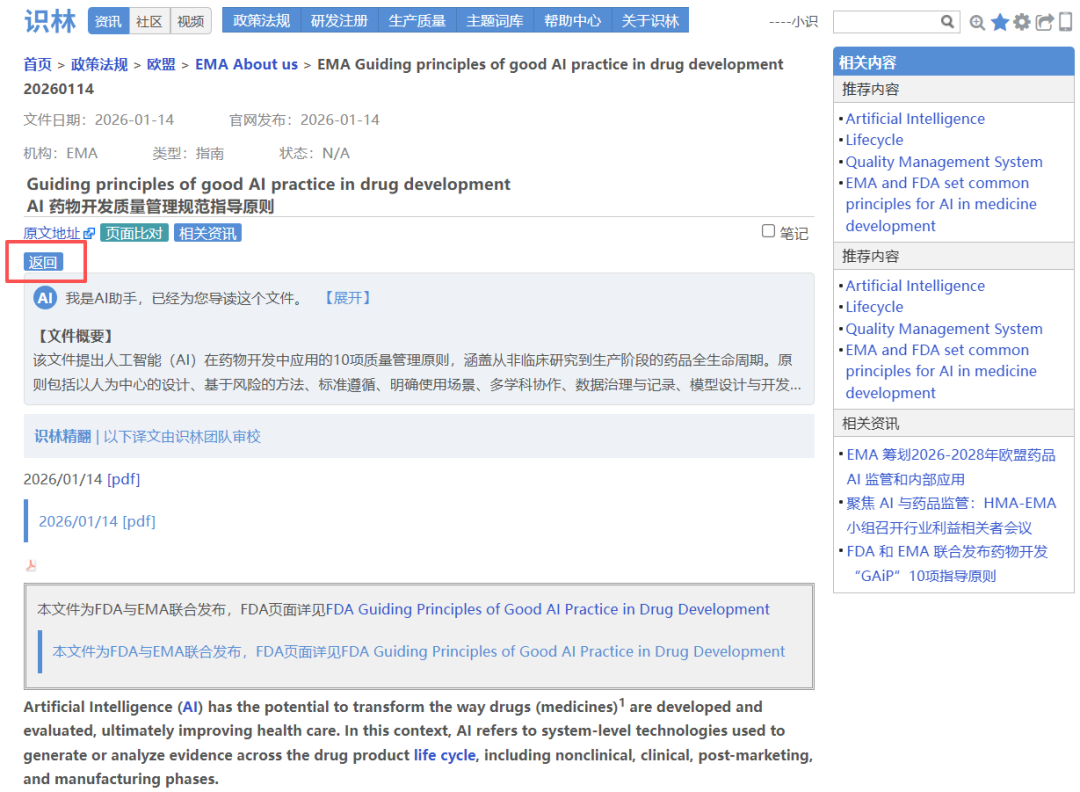
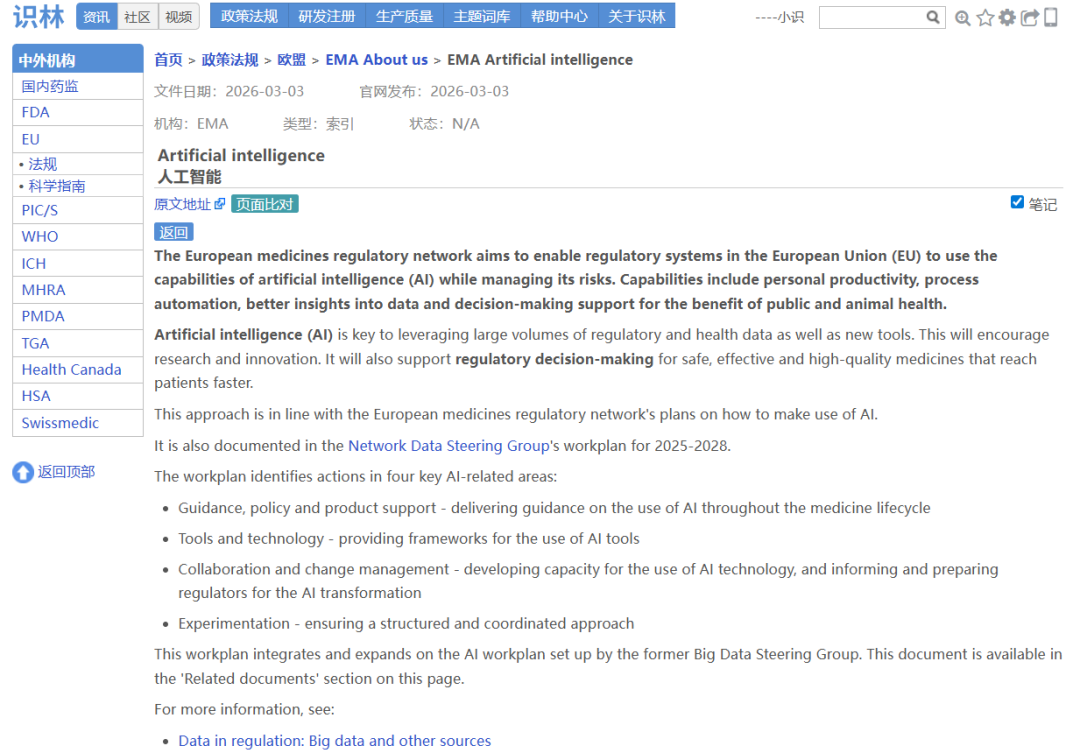
AI在药物开发和监管中的应用日益增多,但相关指南分散在不同页面,官方来源也需要反复核对。识林将《AI药物开发质量管理规范指导原则》与EMA人工智能总索引页通过“返回”键关联,从一份文件即可回溯至EMA全部AI资源库(思考性文件、AI观察站报告、Scientific Explorer工具及首个AI临床工具资质认证案例),并可通过“原文地址”进一步溯源至EMA官网原始发布页面,可供快速定位、交叉核对,确保每一份文件都有据可查。
——从——
场景2:从CDE指南正文【返回】发布通告,查询实施日期和文件号
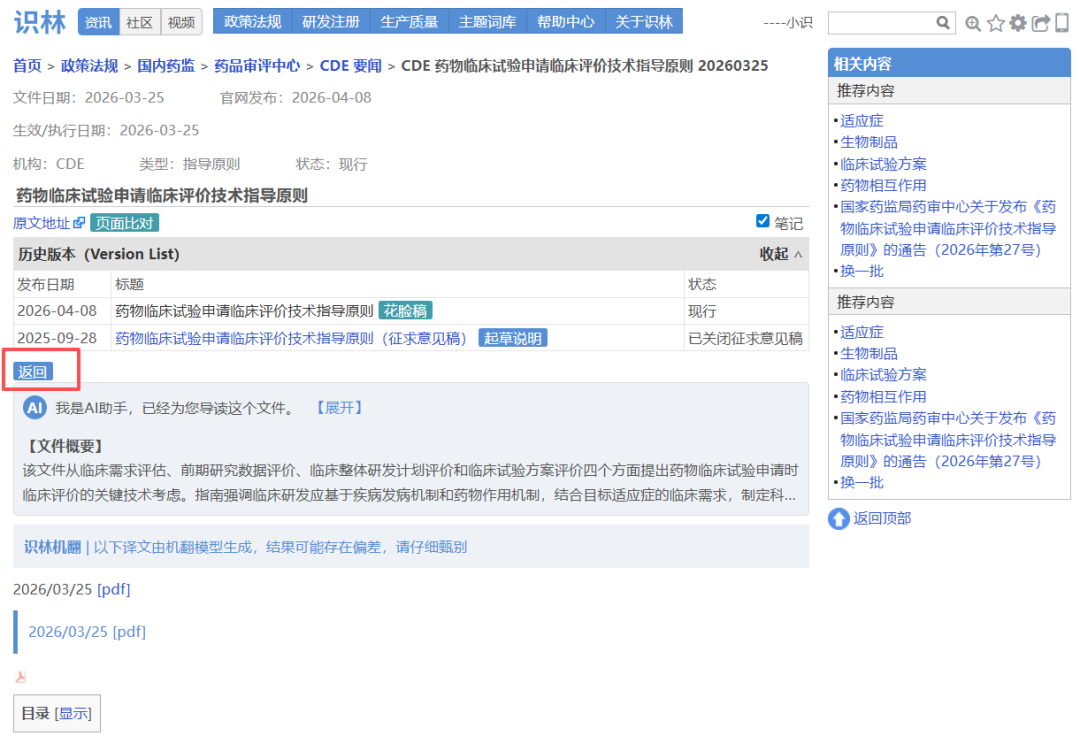
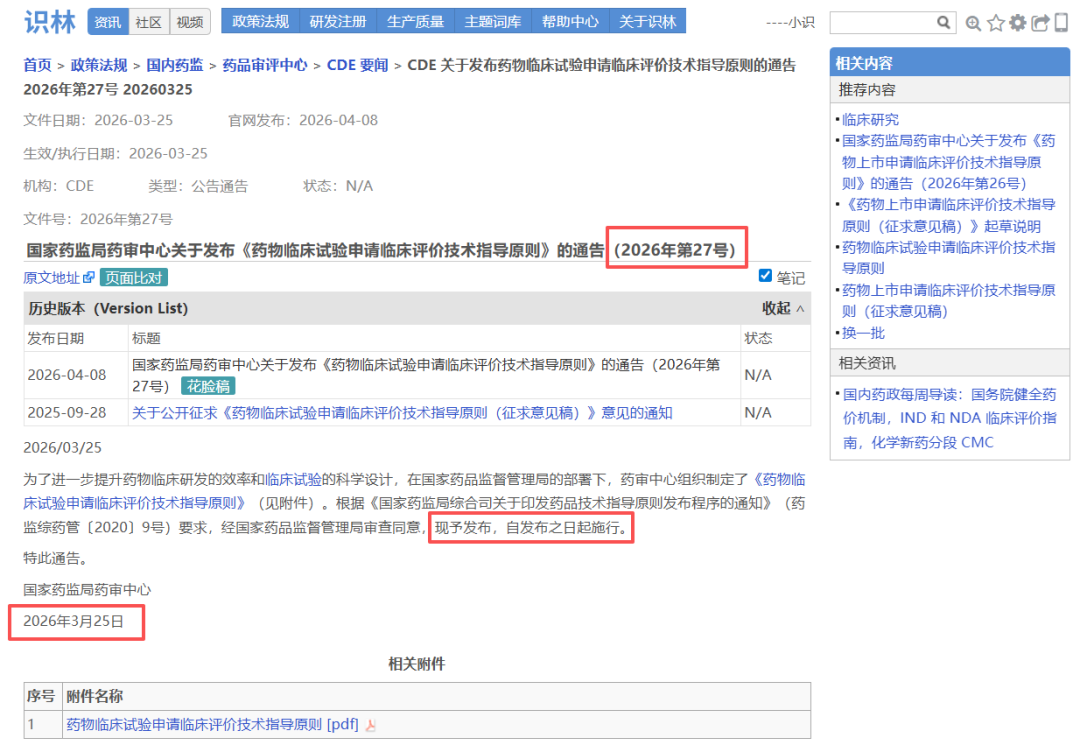
大家熟悉的CDE指导原则,其技术要求集中在指导原则正文,但官方发布背景、文件号、生效日期均在另一份通告中。例如从《药物临床试验申请临床评价技术指导原则》正文点击“返回”即可直达通告页面,确认文件编号(2026年第27号)、发布日期和施行日期,并可下载原始PDF附件。对于需要确保申报合规的注册和临床研发人员,这一设计让技术内容与官方依据始终对应,避免因信息分离导致疏漏。另外,这也是考虑到用户们常用“27号文”来指代指导原则的实际场景。
——从——
场景3:从ICH Q9【返回】查阅历史版本,中文版以及最新培训资料包
ICH 《Q9(R1)质量风险管理》指南配套的培训材料、概念性文件等分散在不同页面,且多为英文原文。当您找到Q9页面,点击“返回”即可打开完整索引,查看完整文件清单,包括CDE和CFDI的两份中文翻译版,以及最近更新的培训资料包。ICH的官方PPT完整细致,具有相当的学习参考价值。
——从——
场景4:从新加坡GMP检查总结【返回】查询新加坡GMP法规指南
新加坡卫生科学局(HSA)作为PIC/S正式成员,其GMP标准、GDP要求、历年缺陷趋势及配套指南是企业现场检查准备的参考依据之一。当用户找到《2025年生产商GMP缺陷趋势》(例如从识林发布的专题文章《新加坡HSA总结2025年药品GMP检查缺陷》找到),此时点击“返回”即可抵达HSA的“GMP和GDP标准”总览页面,回溯至HSA全部资源库,涵盖GMP(PIC/S PE 009-17及附录)、GDP、历年GMP/GDP缺陷趋势分析(2023-2025)、场地主文件编制指南、基于健康暴露限值的交叉污染控制指南等关键文件。
——从——
场景5:从一封日本PMDA“橙色警告信”【返回】完整清单
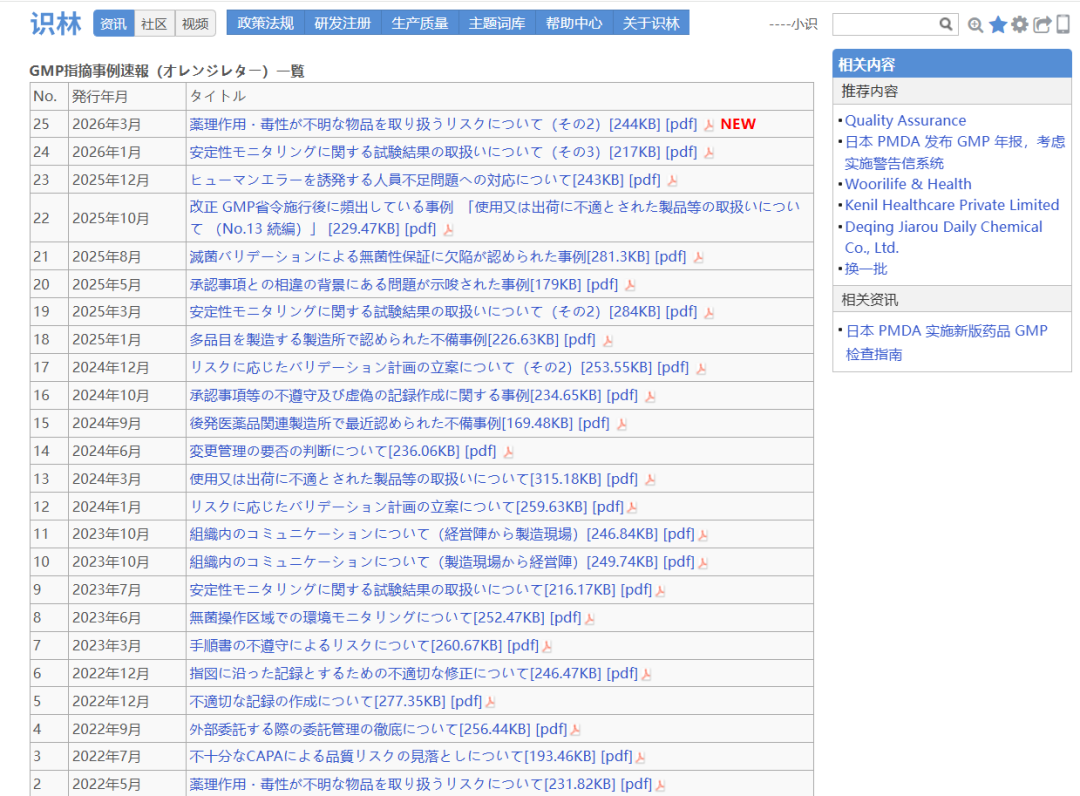
日本药品和医疗器械管理局(PMDA)“橙色警告信”是PMDA分享的GMP检查缺陷典型案例。识林将单份警告信与《品質確保に関する取り組み》页面通过“返回”键关联,从一份案例即可回溯至全部橙色警告信列表、GMP/GCTP年度报告等资源。PMDA发布的GMP/GCTP年度报告详细介绍了其在药品质量管理方面的业务实施与未来展望;另外,页面列出的GMP橙色警告信索引涵盖稳定性试验结果处理、无菌性保证缺陷等具体问题案例,为行业提供了实用参考。
——从——
|责任编辑:识林-木姜子
|编辑:识林-雪见
识林®版权所有,未经许可不得转载

【关于识林-常见问题与解答】

