J Pharm Anal:中国药科大学叶慧团队—优化后的TRAP技术显著提高靶标识别精度

叶慧教授
靶向响应性可及性谱分析(Target-responsive accessibility profiling,TRAP)是一种用于药物靶点发现的强效化学蛋白质组学策略,可监测配体诱导的赖氨酸可及性变化。然而,TRAP 及相关方法仍受限于样品消耗量大、分析时间长,而孵育温度对靶点识别的系统性影响至今尚未被探究。
2026年3月11日,中国药科大学叶慧团队在J Pharm Anal(IF=8.9)发表了题为“DT-TRAP enables accurate target recognition via simplified dosing and low-temperature incubation”的研究文章,建立了对剂量和温度两个关键参数进行优化的TRAP(DT-TRAP)工作流程,证明采用三剂量设计并结合4°C低温孵育,能够显著抑制非特异性背景、减少假阳性,从而在降低实验复杂性和样品消耗的同时,可靠地识别药物真实靶点并解析肽段水平的结合位点。

一、主要内容
本文中,作者提出了剂量与温度优化的TRAP(DT-TRAP),这是一种精简的工作流程,将合理的剂量策略与可控的孵育温度相结合,以提高配体-蛋白质相互作用谱分析的特异性和可靠性。以丙酮酸激酶M2(PKM2)激活剂TEPP-46 和热休克蛋白90(HSP90)抑制剂格尔德霉素(geldanamycin)为模型化合物,作者证明简化的三剂量设计足以稳健地识别真实靶点。值得注意的是,与25 °C 或37 °C 相比,在4 °C下孵育可显著抑制非特异性相互作用并提高结合特异性。将DT-TRAP 应用于星形孢菌素(staurosporine)和阿司匹林(aspirin),作者成功识别了复杂蛋白质组中的多个靶点,且肽水平分析将结合位点主要定位在配体结合口袋内。总体而言,这些发现将DT-TRAP 确立为一个用于优化化学蛋白质组学实验参数的实用框架,从而提高靶点识别的准确性并促进药物发现。
Graphical abstract
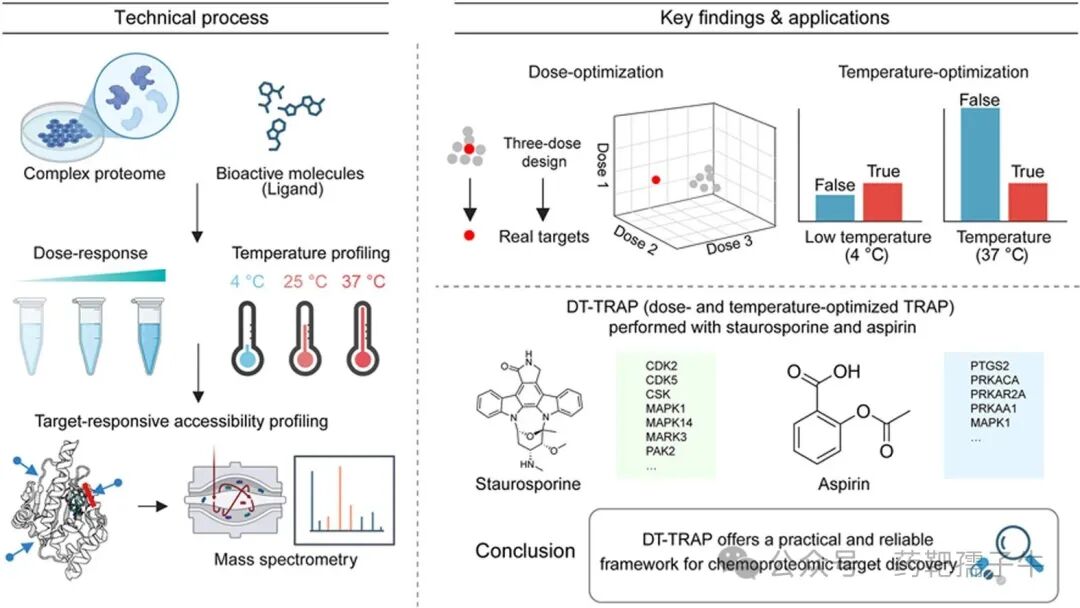
Highlights
•对TRAP 中剂量与温度的合理优化显著提高了靶点识别的准确性。
•三剂量TRAP 策略能够可靠地区分真实药物靶点,同时最大限度减少实验负担。
•低温孵育(4 °C)可降低非特异性相互作用,从而减少假阳性。
•DT-TRAP 成功识别了staurosporine和aspirin的多个靶点,并在肽段分辨率水平上定位了结合位点。
•DT-TRAP 工作流程为准确、高效的药物靶点发现提供了一个稳健的框架。
二、主要结果
1、剂量响应型TRAP识别模型化合物TEPP-46的真实靶点
在复杂蛋白质组中,TEPP-46处理可诱导其已知靶点PKM2上K305/K311位点的赖氨酸可及性发生显著且浓度依赖的变化(R²=0.9951),并且该肽段与TEPP-46在PKM2晶体结构中的结合口袋(PDB: 3U2Z)空间位置接近,验证了剂量响应型TRAP在肽段水平上区分特异性靶点与背景信号的能力。
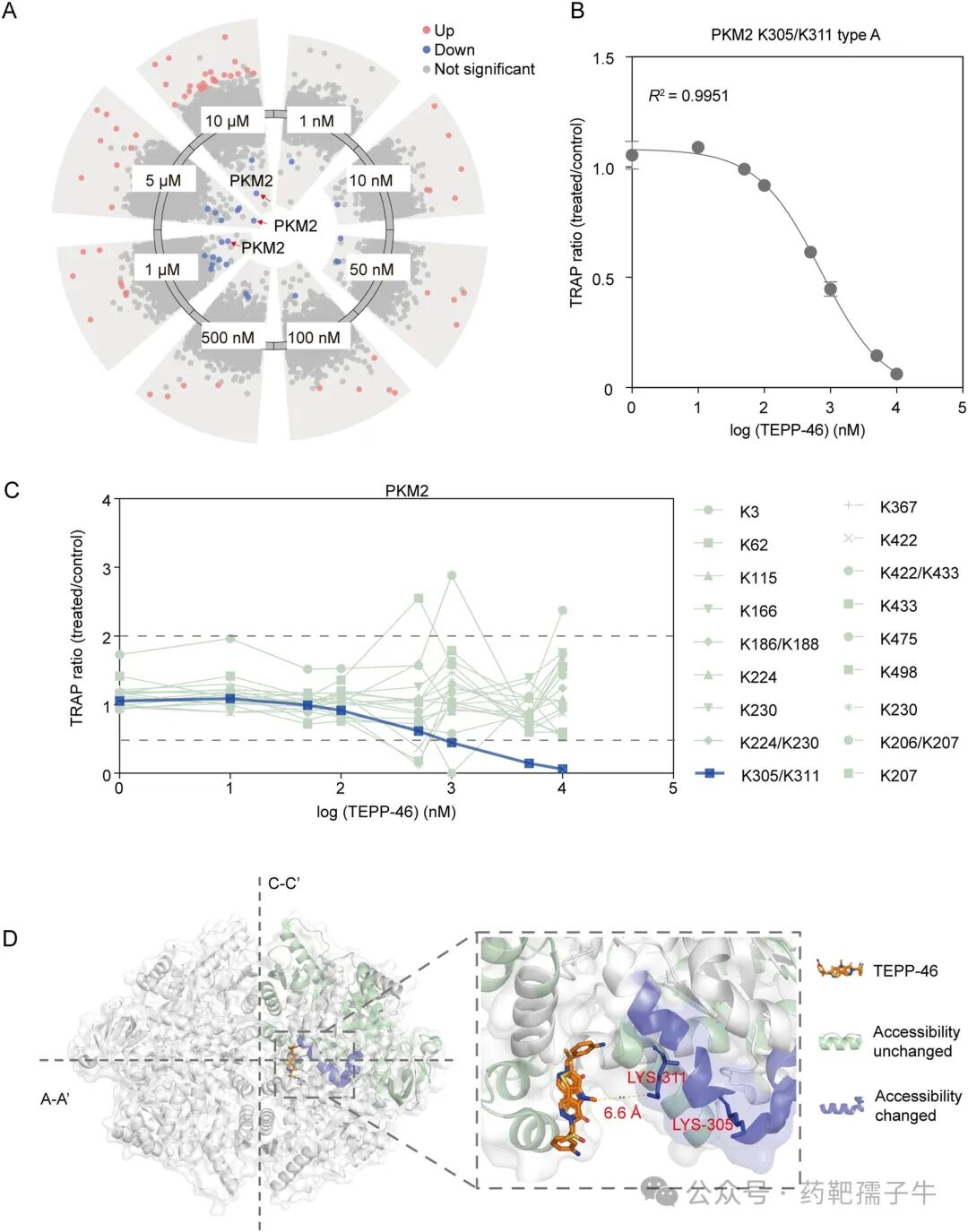
图1 剂量响应性TRAP在复杂蛋白质组中识别TEPP-46 的靶点
2、两剂量与三剂量分析确认TEPP-46的真实靶点
两剂量设计(1 µM和5 µM)存在假阳性或结果模糊的风险;而三剂量设计(1、5、10 µM)中,PKM2是唯一在所有剂量下均表现出一致可及性变化的蛋白,表明三剂量策略可有效识别真实阳性药物靶点。
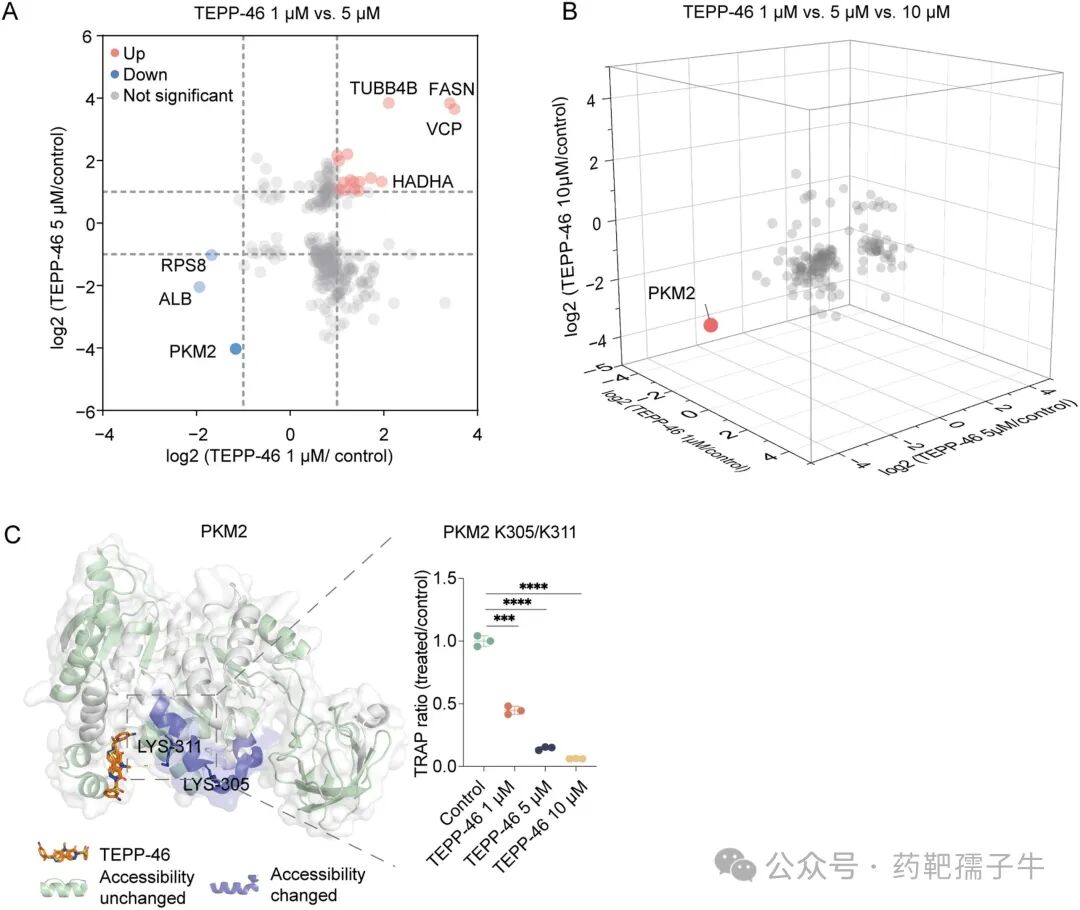
图2 使用两剂量和三剂量TRAP对TEPP-46 进行靶点识别
3、剂量响应型TRAP识别geldanamycin的特异性靶点
在HSP90抑制剂geldanamycin处理下,HSP90AA1的K58、HSP90AB1的K53以及TRAP1的K126位点呈现出剂量依赖性的可及性变化,并且这些位点在晶体结构中均位于geldanamycin结合口袋附近,而非响应肽段则远离结合区域。
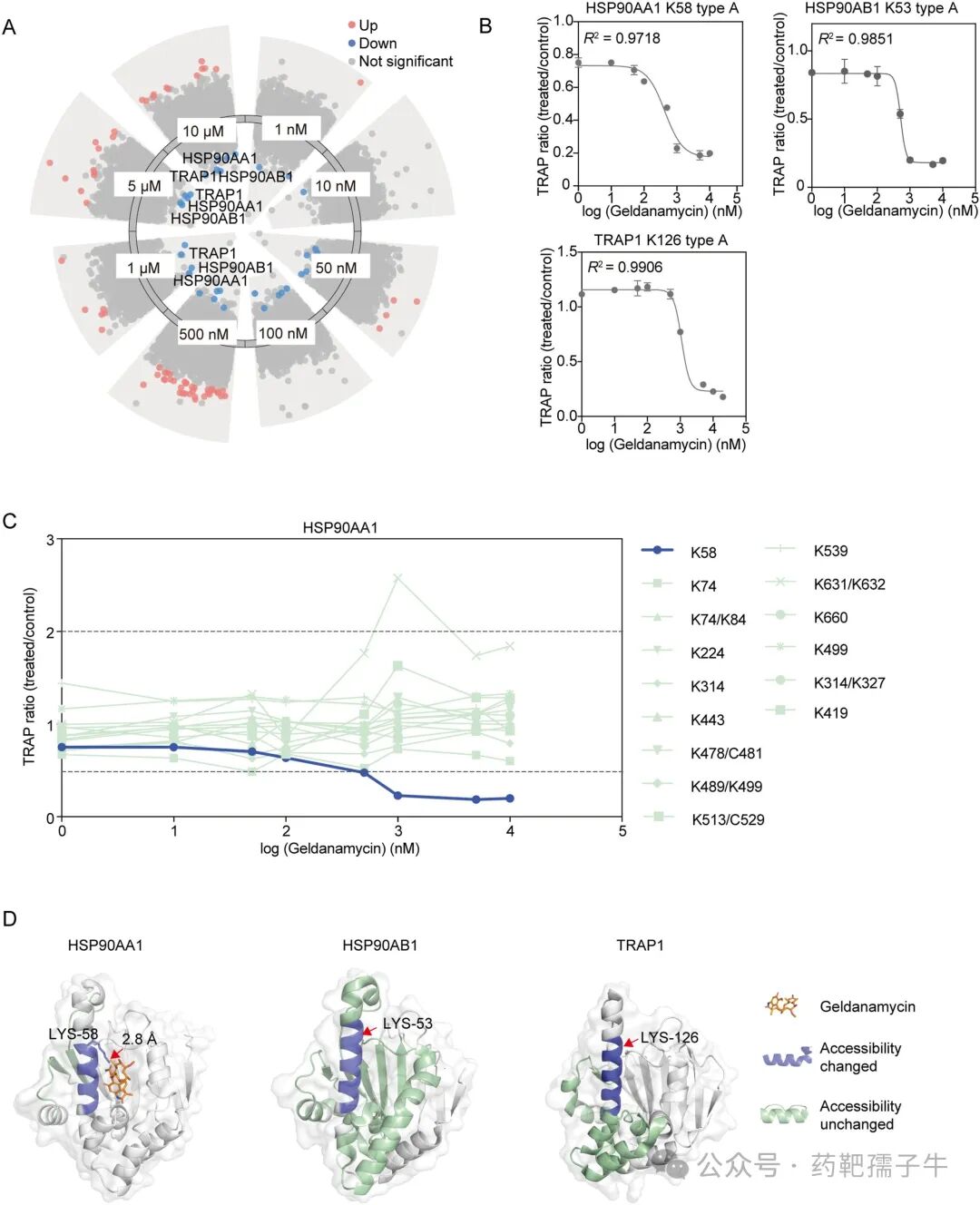
图3 剂量响应性TRAP在复杂蛋白质组中确认geldanamycin的靶点
4、两剂量与三剂量分析确认geldanamycin的特异性靶点
两剂量设计(5 µM和10 µM)中HSP90家族蛋白虽有显现,但三剂量设计(1、5、10 µM)下HSP90家族蛋白成为唯一在所有浓度下均被一致识别的靶点,进一步支持三剂量策略可有效捕获真实靶点并降低背景噪声。
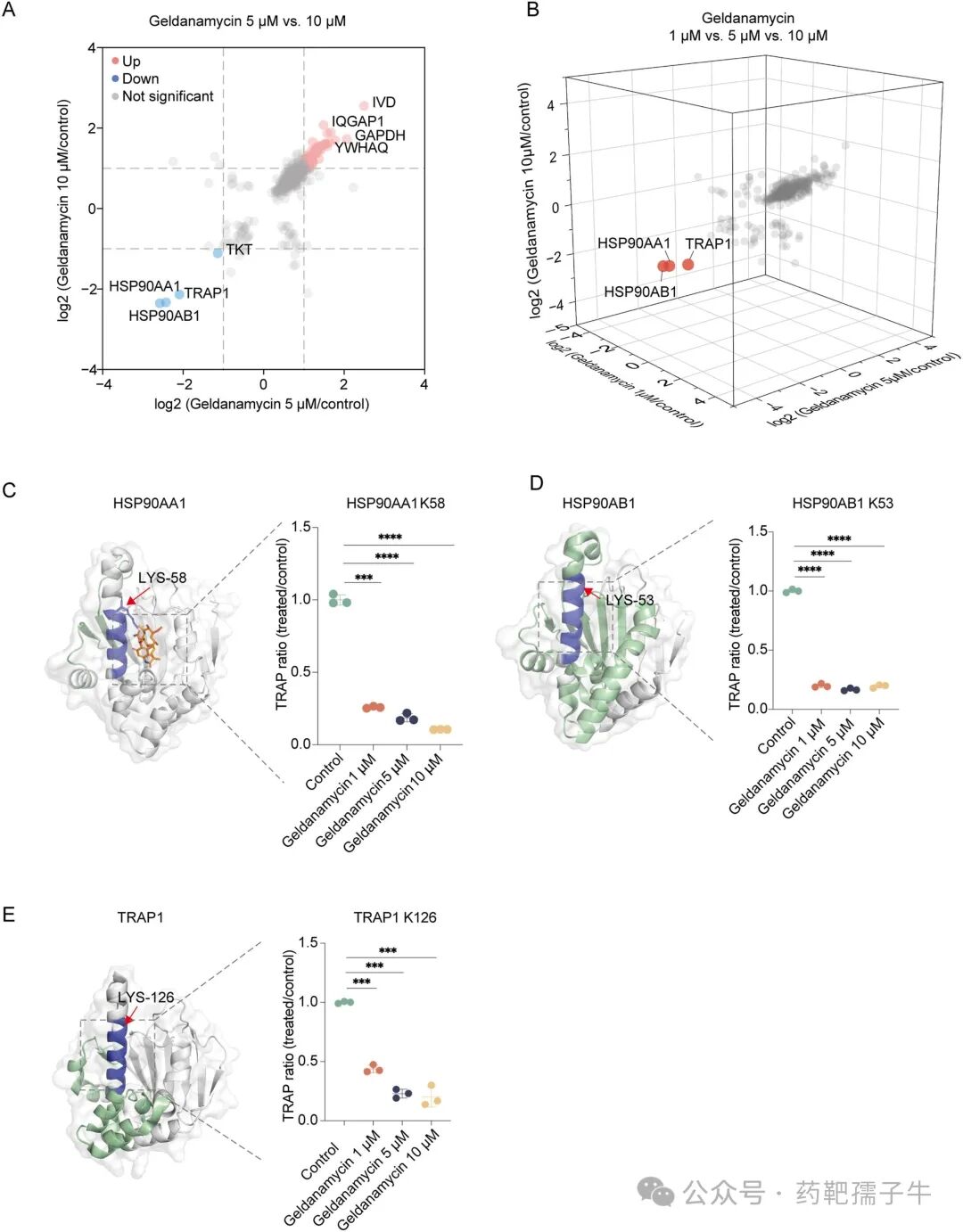
图4 使用两剂量和三剂量TRAP对geldanamycin进行靶点识别
5、温度响应型TRAP的基准测试
在4°C、25°C和37°C三种孵育温度下,TRAP标记效率相近(约50%),且各温度下均能识别出已知靶点。然而,37°C条件下非特异性相互作用显著增加(geldanamycin的潜在靶点从9个增至24个,TEPP-46从8个增至51个),而低温(4°C)可有效减少非特异性信号,提高靶点检测的特异性。
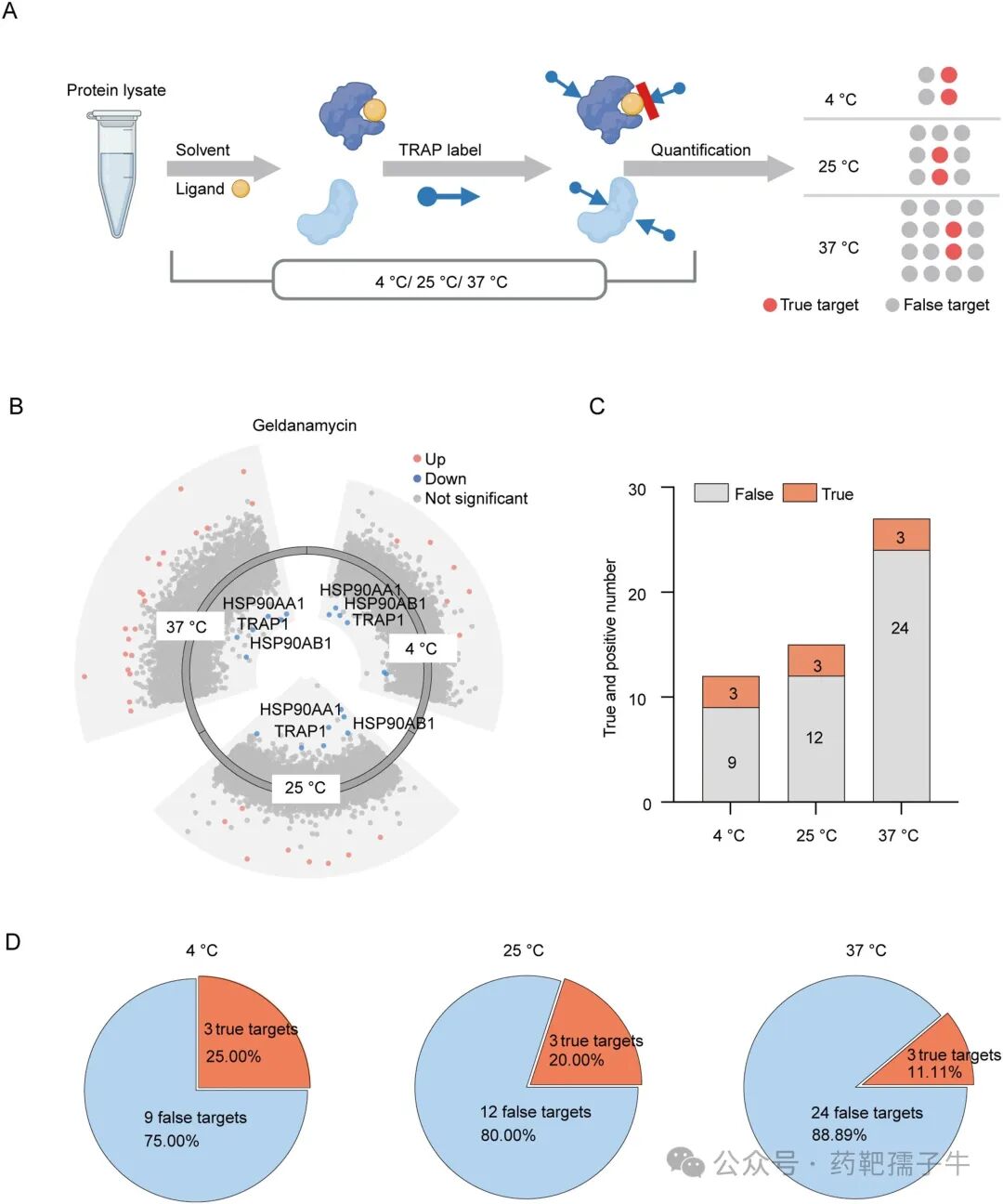
图5 在不同温度条件下对温度响应性TRAP进行基准测试
6、DT-TRAP策略识别广谱激酶抑制剂staurosporine的靶点
采用三剂量(10、20、50 µM)结合4°C孵育的DT-TRAP策略,在K562细胞裂解液中识别出45个剂量响应候选蛋白,其中28个为激酶(占62.22%),显著高于25°C(43.38%)和37°C(33.66%)。肽段水平分析表明,发生可及性变化的赖氨酸残基(如CDK2的K33、AURKA、PRKACA、MAP2K2等)多位于ATP/ADP结合口袋或staurosporine结合位点附近,而未响应肽段则远离这些区域。
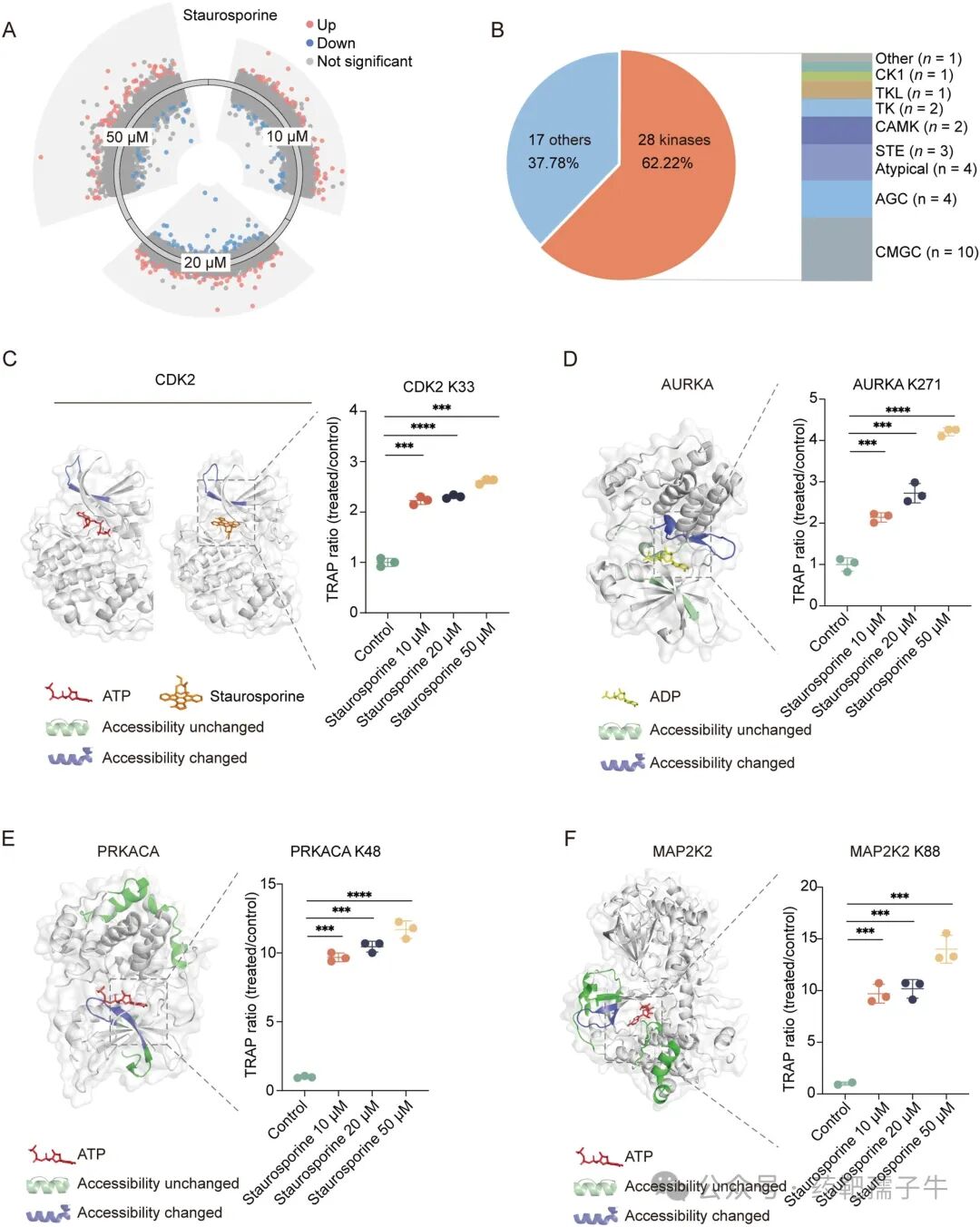
图6 使用DT-TRAP对staurosporine进行靶点识别
7、DT-TRAP策略识别多靶点药物aspirin的靶点
在4°C条件下,DT-TRAP从aspirin处理中识别出13个高置信度靶点,包括经典靶点PTGS2(K432)以及PRKACA(K49)等AMPK通路相关蛋白。KEGG和GO富集分析显示这些靶点富集于能量代谢、激素信号和癌症相关通路。分子对接进一步证实发生可及性变化的赖氨酸残基位于aspirin结合口袋附近。
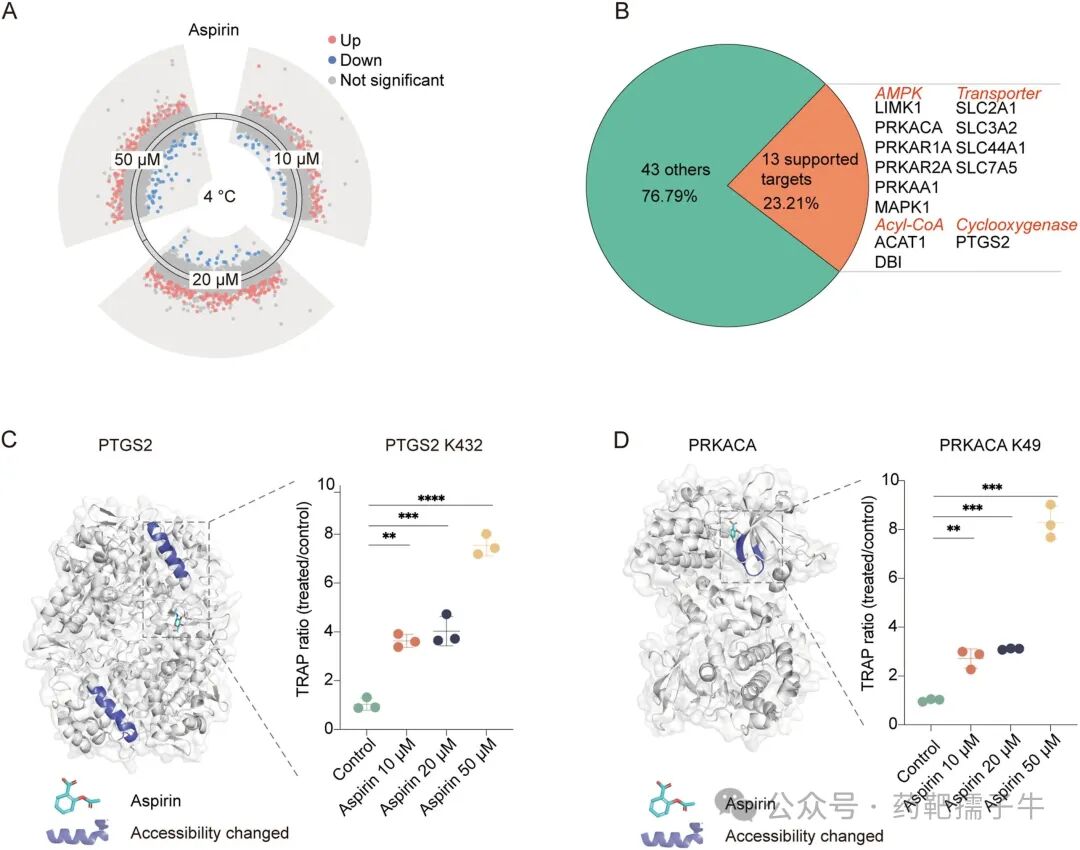
图7 使用DT-TRAP对aspirin进行靶点识别
三、总结
在本研究中,作者通过系统评估剂量和温度参数,利用具有明确靶点或广泛多靶点谱的模型化合物(包括TEPP-46、格尔德霉素、星形孢菌素和阿司匹林),建立了一个优化的DT-TRAP 工作流程。结果表明,简化的三剂量设计结合低温(4 °C)孵育,能够可靠地捕获真实靶点,同时有效最小化非特异性背景信号。尽管该工作流程优先考虑稳健且可重复的相互作用,但它仍然具有适应性,允许调整孵育时间或剂量梯度,以适应低亲和力或慢结合速率的配体。因此,低温实施代表了在抑制实验噪声与维持高可信度靶点识别之间的一种策略性平衡。
总之,优化的DT-TRAP 策略为药物靶点发现提供了一个可靠且精简的框架。通过有效区分特异性结合与背景噪声,并提供残基水平的分辨率,该方法拓宽了化学蛋白质组学在阐明复杂药理学制剂作用机制方面的适用性。
文献链接
https://doi.org/10.1016/j.jpha.2026.101605
信息来源:药靶孺子牛




免责声明
“汇聚南药”公众号所转载文章来源于其他公众号平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请在留言栏及时告知,我们会在24小时内删除相关信息。
本平台不对转载文章的观点负责,文章所包含内容的准确性、可靠性或完整性提供任何明示暗示的保证。
喜欢的点个“看一看”和"喜欢"吧

不然微信推送规则改变,有可能每天都会错过我们哦~
