Cell:邵峰院士、袁钧英院士等系统总结癌症中的细胞死亡,指名癌症治疗新思路


编译丨王聪
编辑丨王多鱼
排版丨水成文

封面图片展示了《癌症的特征》持久的影响——促进了癌症研究界的合作,将科学家、临床医生、患者和教育工作者团结起来,共同推动癌症研究的进步。

“我们的身体由活着的细胞组成,同样也由必然死亡的细胞组成。”(Our bodies are made of cells that live, and just as surely, of cells that must die.)
这句来自诺贝尔奖得主 Sydney Brenner(因细胞程序性死亡的研究获得 2002 年诺贝尔生理学或医学奖)的名言,道出了生命与死亡在细胞层面的紧密联系。在癌症治疗领域,科学家们正越来越深刻地认识到:让癌细胞“正确死亡”,可能是攻克这一顽疾的关键。
“逃逸细胞死亡”(Evasion of cell death)是癌症的一个显著特征,可以说,癌细胞最擅长的就是逃逸死亡,这使其能够抵御致癌和治疗带来的压力。恢复癌细胞的死亡机制,是一种颇具吸引力的癌症治疗策略,但这需要对细胞死亡程序有深入的理解。
在过去的二十年里,细胞死亡领域已从凋亡(Apoptosis)扩展到包括坏死性凋亡(Necroptosis)、焦亡(Pyroptosis)、铁死亡(Ferroptosis)以及其他新兴细胞死亡方式(例如铜死亡、NETosis、Disulfidptosis、Alkaliptosis、Oxeiptosis、Parthanatos 等),重塑了癌症生物学,并揭示了癌症治疗的新机会。尽管凋亡仍是放疗和化疗诱导的主要细胞死亡程序,但非凋亡程序能够驱动炎症反应,并协调肿瘤、基质和免疫成分之间的相互作用,影响免疫治疗的效果。铁死亡是一种铁依赖的、由脂质过氧化驱动的细胞死亡方式,没有典型的诱导信号,而是源于脂质、铁和氧化还原代谢的紊乱。
该综述提出了一个统一框架,用于理解主要的细胞死亡程序在癌症发生、发展和治疗反应中的作用,以及应对癌细胞死亡抵抗和免疫抑制的问题。
癌症的“不死”之谜
早在 2000 年,《癌症的特征》就提出了“逃逸凋亡”是癌症的标志之一。正常细胞在受损或不再需要时,会通过程序性细胞死亡被清除,但癌细胞却学会了绕过这一机制,实现无限增殖。
细胞病理学之父 Rudolf Virchow 在 19 世纪就指出,疾病的本质是细胞层面的变化,导致增殖与死亡之间的平衡被打破。这一观点在今天看来依然深刻——癌细胞不仅增殖失控,更重要的是它们逃避了本该发生的死亡。
传统上,科学家们主要关注细胞凋亡这种程序性死亡方式。凋亡是细胞主动、有序的自我毁灭过程,不会引发炎症反应。然而,随着研究的深入,科学家们发现,凋亡远非细胞死亡的唯一方式。
主要的细胞死亡方式
这篇综述系统梳理了目前已知的主要的细胞死亡方式——凋亡、坏死性凋亡、焦亡、铁死亡,每种都有其独特的机制和生物学意义。
凋亡是最经典的程序性细胞死亡方式,通过线粒体途径或死亡受体途径启动。凋亡过程中,细胞会收缩、染色质凝聚、细胞膜起泡,最终被吞噬细胞清除而不引发炎症。许多化疗和放疗正是通过诱导癌细胞凋亡来发挥治疗作用。
坏死性凋亡和焦亡是两种裂解性、炎症性的细胞死亡方式。与凋亡不同,这两种方式会释放细胞因子和损伤相关分子模式,影响肿瘤抗原的可用性、树突状细胞的活化,从而影响免疫检查点阻断治疗的效果。
铁死亡则是一种机制独特的细胞死亡方式,它依赖于铁和脂质过氧化,缺乏经典的遗传编码触发信号。有趣的是,那些对凋亡产生抵抗的癌细胞,往往对铁死亡特别敏感,这为治疗耐药性肿瘤提供了新思路。
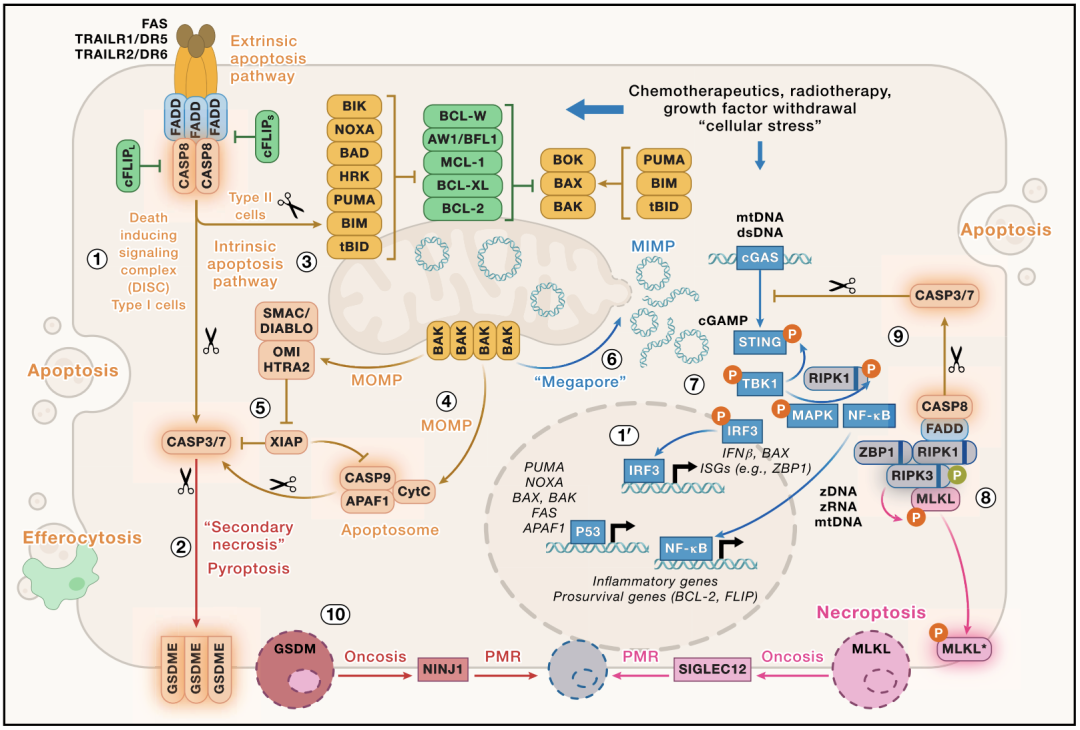
外源性和内源性细胞凋亡通路,以及与 cGAS/STING 通路的相互作用导致细胞凋亡和坏死性凋亡
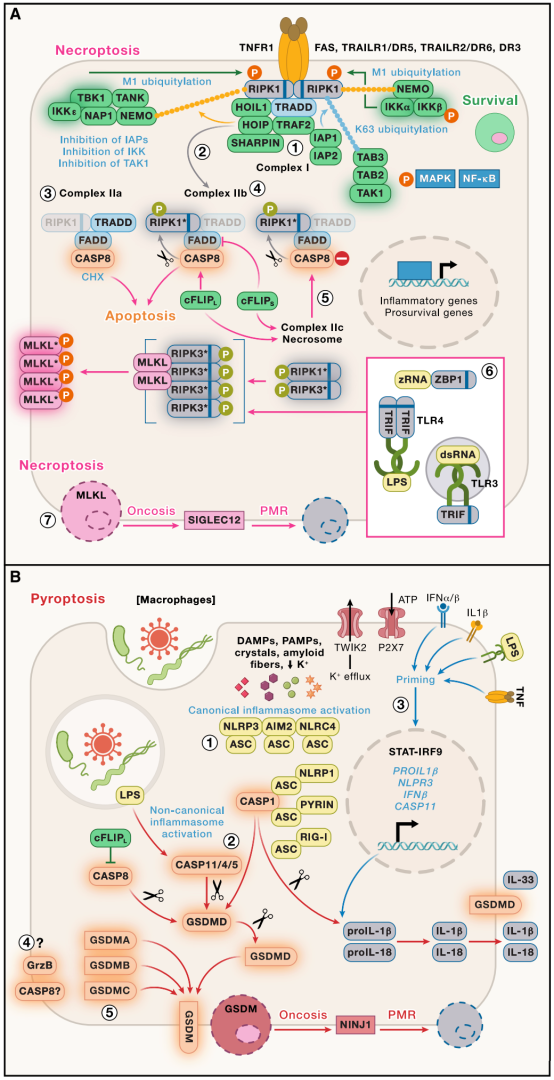
诱导坏死性凋亡和焦亡
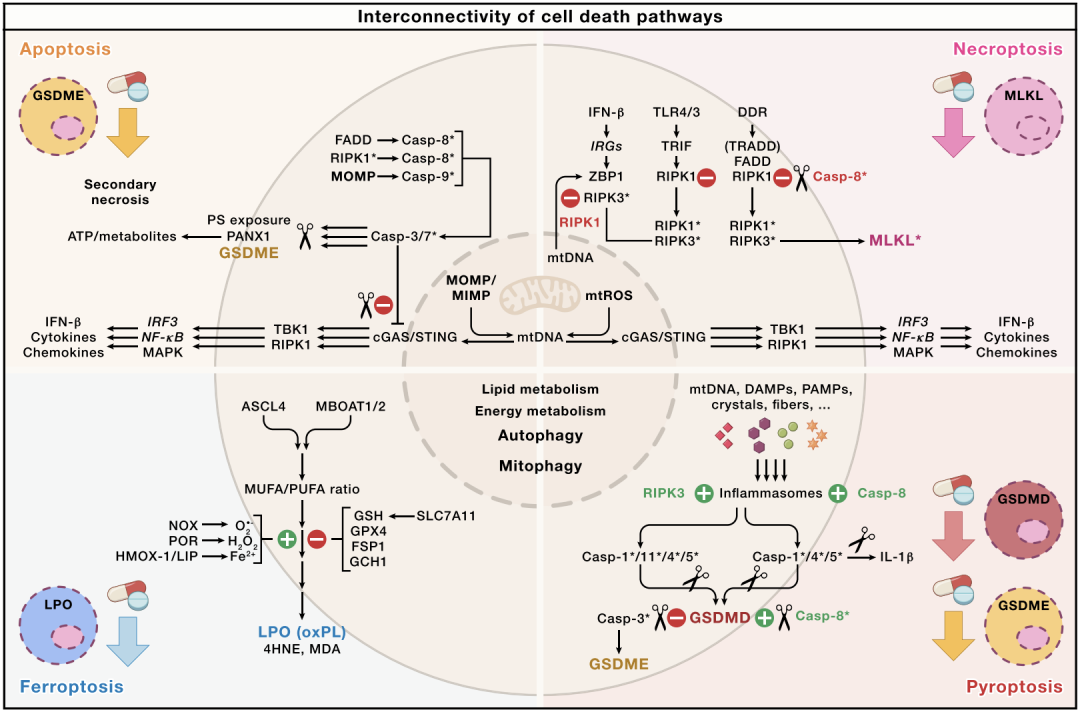
细胞死亡通路的相互关联性
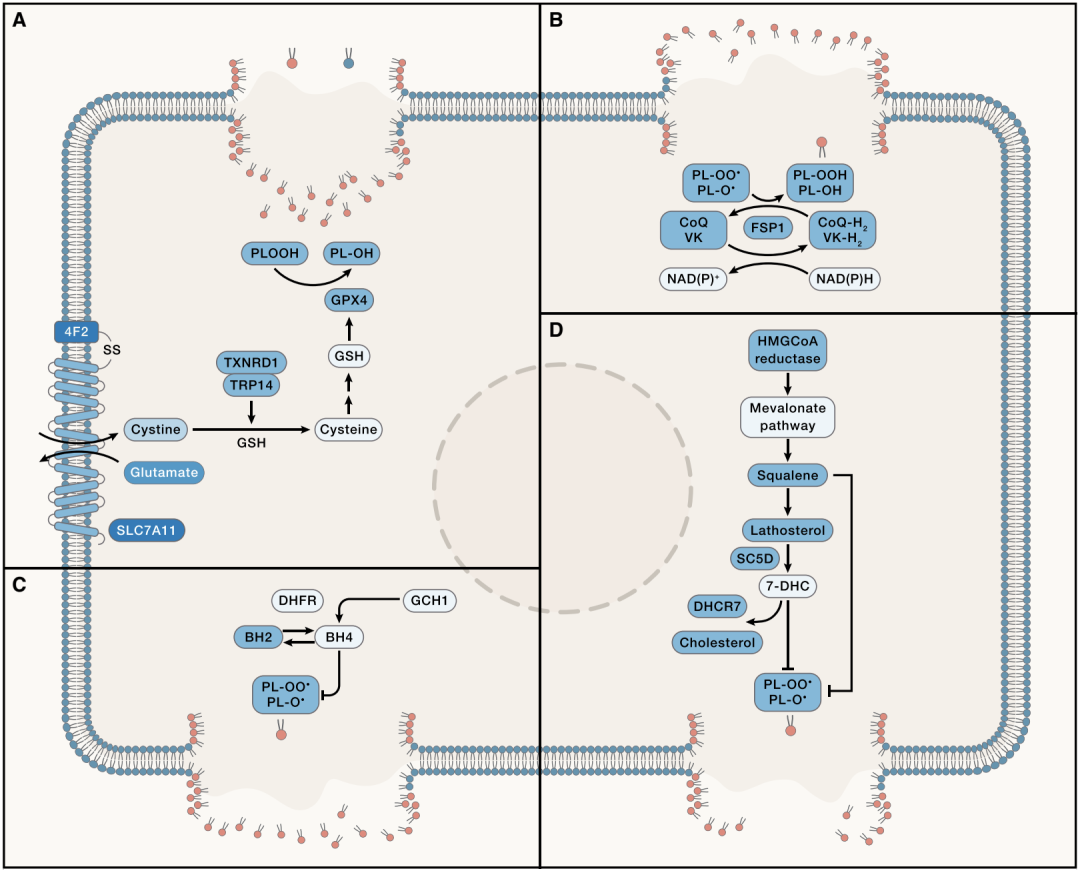
新兴的细胞死亡方式
除了上述几种主要方式,科学家们还发现了多种新兴的细胞死亡方式,每种都与特定的代谢紊乱相关。
铜死亡(Cuproptosis)由细胞内铜积累触发,铜与三羧酸循环中的脂酰化成分直接结合,导致蛋白质聚集和细胞死亡,某些肺癌细胞因高代谢活性而对铜死亡特别敏感。
NETosis 是中性粒细胞特有的细胞死亡方式,与中性粒细胞外诱捕网(NET)形成相关。在癌症中,过度的 NET 形成会促进血栓形成和转移,与患者不良预后相关。
双硫死亡(Disulfidptosis)在葡萄糖饥饿条件下由异常二硫键积累触发;碱死亡(Alkaliptosis)由细胞内碱化介导;氧化凋亡(Oxeiptosis)由高水平活性氧触发;Parthanatos 则由 PARP1 过度激活引起。这些新兴的细胞死亡方式虽然研究尚浅,但为理解癌症生物学提供了新维度。
实际上,新的细胞死亡方式还在源源不断地发现中,例如,泛凋亡(
癌症治疗策略的新思路
对细胞死亡机制的深入理解,已经催生了新的癌症治疗策略。最成功的例子是靶向 BCL-2 蛋白的 BH3 模拟物药物。
BCL-2 是一种抗凋亡蛋白,它的过表达会阻止癌细胞凋亡,BCL-2 抑制剂维奈托克(Venetoclax)已在慢性淋巴细胞白血病和急性髓系白血病治疗中显示出显著疗效,成为细胞死亡研究临床转化的里程碑。
然而,单一靶向凋亡途径往往面临耐药性问题。癌细胞非常“聪明”,当一条死亡通路被阻断时,它们会激活其他生存机制。因此,联合靶向不同细胞死亡途径成为新的研究方向。例如,铁死亡诱导剂与免疫疗法的联合使用,可能对传统治疗耐药的肿瘤产生更好效果。同样,针对铜死亡、NETosis 等新兴细胞死亡方式的治疗策略也在积极探索中。
免疫系统的双重角色
细胞死亡与免疫系统的相互作用复杂而微妙。一方面,免疫原性细胞死亡可以增强抗肿瘤免疫;另一方面,过度炎症可能创造有利于肿瘤生长的微环境。
某些细胞死亡方式会释放“危险信号”,激活免疫系统攻击肿瘤。这就是免疫原性细胞死亡的核心概念。然而,治疗策略如果过度强化对癌细胞的杀伤能力,也可能损害免疫细胞的功能,反而削弱免疫介导的癌症控制。
因此,理想的治疗策略应该选择性靶向癌细胞,同时保护甚至增强免疫功能。这需要精确理解不同细胞死亡方式对肿瘤微环境的影响,以及它们与免疫系统的相互作用。
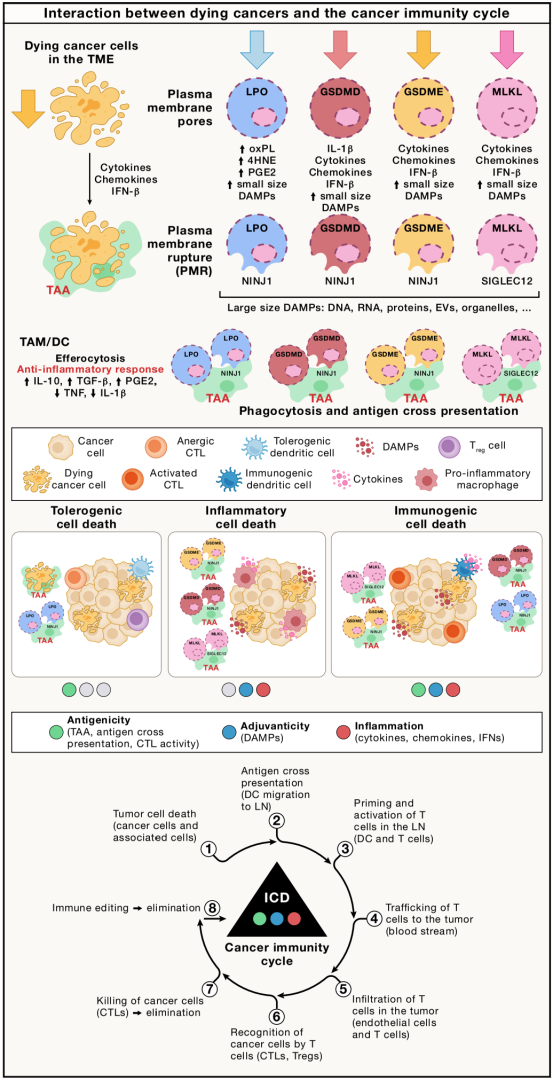
癌细胞死亡与癌症免疫循环之间的相互作用
维奈托克等靶向药物的成功已经证明,调控细胞死亡是有效的抗癌策略。随着对坏死性凋亡、焦亡、铁死亡等机制的理解不断深入,更多创新癌症疗法正在路上。
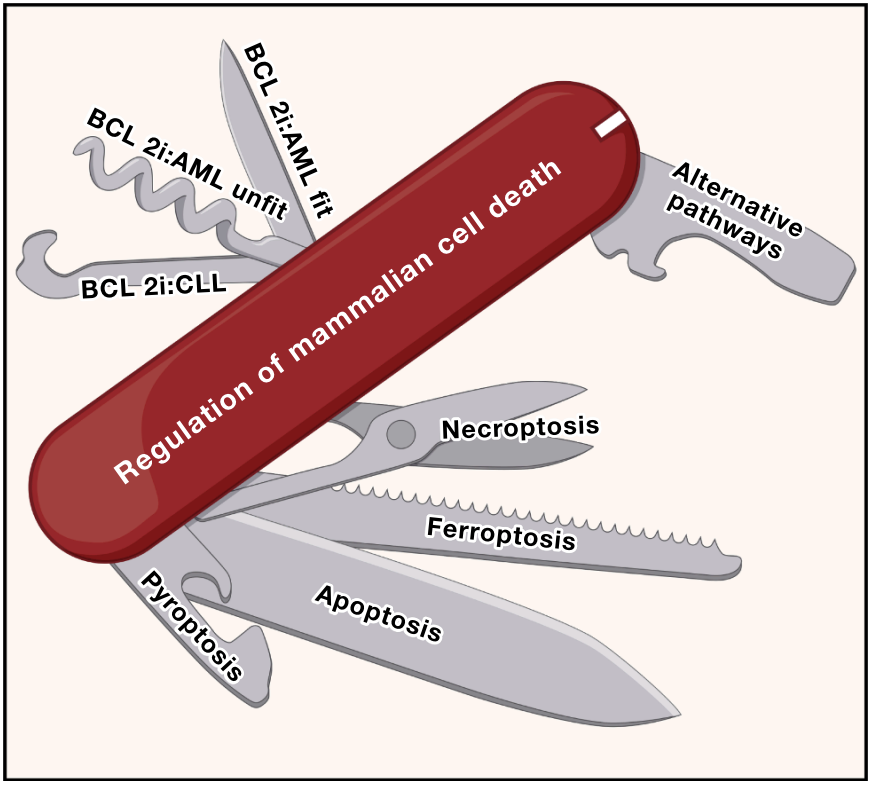
下图采用瑞士军刀作为类比来说明哺乳动物细胞如何部署一套模块化的受控细胞死亡(RCD)程序,这些程序可根据环境、应激压力和遗传线路选择性激活。不同的刀片或工具代表主要的死亡通路,包括凋亡、坏死性凋亡、焦亡和铁死亡,每种通路都针对特定的生物学挑战和免疫反应而设计。此外,这些工具还可能指示出替代或备用路径,当主要程序受阻时这些路径可以被激活。在癌症治疗中,选择性抑制抗凋亡 BCL-2 家族成员可能有效,但可能会留下其他“刀刃”可用,使癌细胞通过切换到非凋亡性死亡或生存策略来逃逸。相反,组合或情境感知的方法,针对刀具的多个“刀刃”,可能通过迫使恶性细胞也激活原本隐藏的死亡路径来克服耐药性。总体而言,该图强调了 RCD 是一个多功能、适应性强的系统,就像一把瑞士军刀,只有当其模块化设计被理解并策略性地加以利用时,其全部潜力才能得以实现。
因此,未来,癌症治疗可能不再依赖单一“杀手锏”,而是根据肿瘤类型和个体特征,精准组合不同细胞死亡通路的调节剂,形成多管齐下的治疗策略。这场生命与死亡的博弈,正因科学家的不懈探索而迎来新的转折点。
1. https://www.cell.com/cell/fulltext/S0092-8674(00)81683-9
2. https://www.cell.com/cell/fulltext/S0092-8674(25)01498-9
3. https://www.cell.com/cell/fulltext/S0092-8674(26)00325-9




点在看,传递你的品味




