IF=11.5 Journal of Controlled Release| 中国药科大学尹莉芳教授开发新型骨髓靶向脂质纳米粒,共递送地西他滨和siTNF-α治疗白血病
发布时间:2026-04-19来源:汇聚南药
尹莉芳教授
中国药科大学尹莉芳教授在国际权威期刊《Journal of Controlled Release》发表题为《Baiting-enhanced extravasation of lipid nanoparticles for targeted co-delivery of decitabine and siTNF-α to the bone marrow niche in leukemia therapy》的研究论文。该研究设计了一种具有“诱饵和增强外渗”功能的骨髓靶向脂质纳米粒(BIS‑LNPs@DCA‑siTNF),共递送缺氧/ROS双响应地西他滨前药和TNF‑α siRNA,通过主动跨越血‑骨髓屏障、靶向白血病细胞并重编程骨髓微环境,有效解决了急性髓系白血病(AML)治疗中药物生物利用度低、耐药性强以及骨髓保护微环境难以突破的关键问题,为AML的化学‑基因联合治疗提供了全新策略与技术支撑。🧬研究背景
急性髓系白血病(AML)是一种高度异质性的造血系统恶性肿瘤,预后极差。骨髓微环境为白血病干细胞(LSCs)提供低氧、免疫抑制的“保护伞”,导致化疗耐药和复发。目前一线药物地西他滨(Dacitabine,DCA)存在体内稳定性差、骨髓蓄积不足的缺陷;而TNF‑α siRNA虽可沉默白血病细胞中异常高表达的TNF‑α,从而阻断PI3K/AKT信号通路、削弱脂质代谢支持并恢复抗肿瘤免疫,但缺乏高效、骨髓特异性的递送载体。脂质纳米粒(LNPs)是核酸递送的金标准,然而如何实现肝外靶向、跨越血‑骨髓屏障并精准递送至骨髓龛内的白血病细胞,仍是重大挑战。受CXCR4/CXCL12趋化轴及CLL‑1在AML细胞表面高表达的启发,团队创新性地构建了双配体修饰、环境响应释放的LNP平台,实现了“诱饵趋化‑内皮松动‑主动摄取”的级联递送。🏆研究结果
1. 设计并合成骨髓靶向配体、响应性前药及脂质两亲物
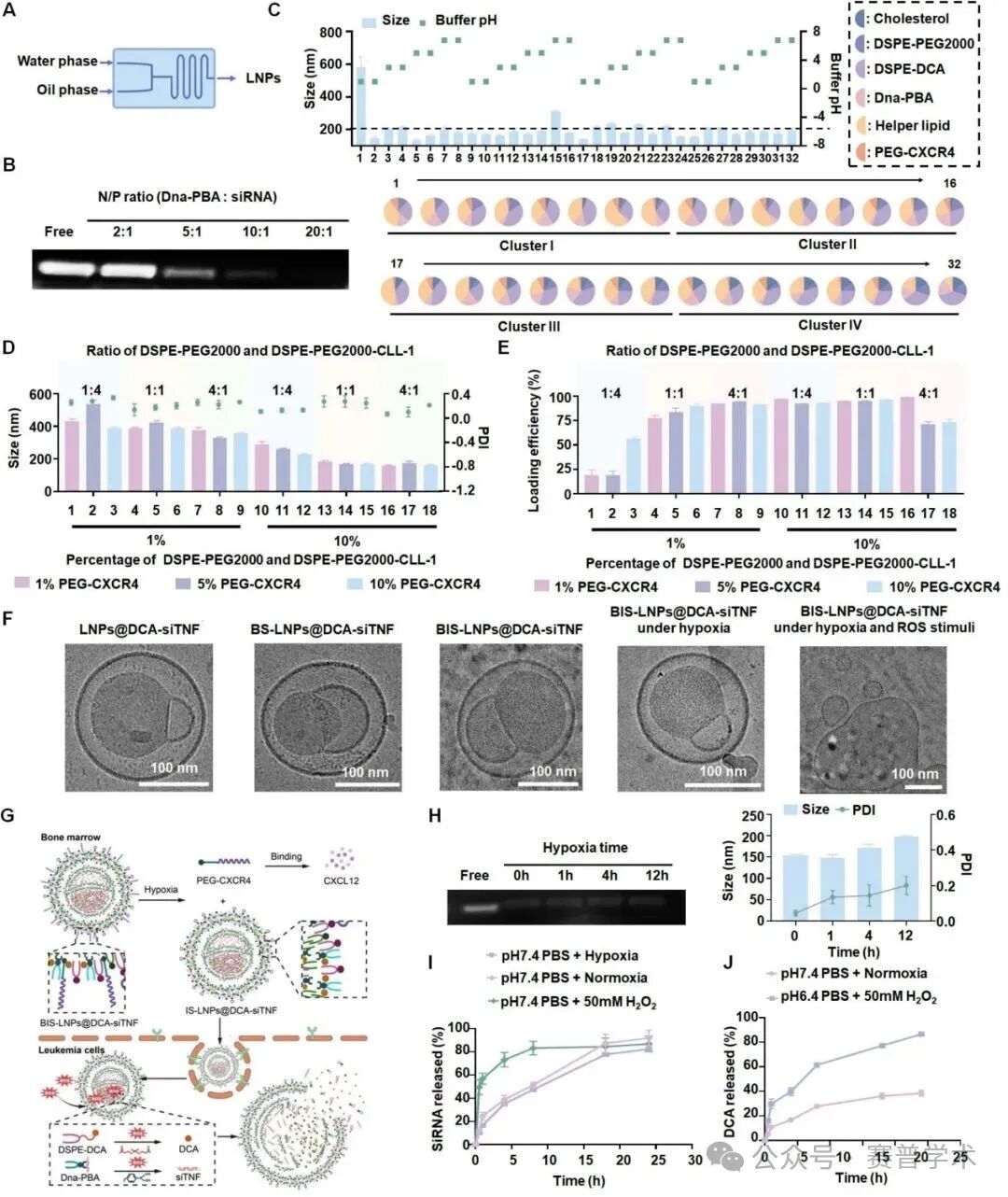
团队合成了PEG‑CXCR4(含缺氧可裂解的4‑硝基苄基连接子)和DSPE‑PEG2000‑CLL‑1(靶向AML标志物CLL‑1)两种功能脂质。同时,将地西他滨通过硫缩醛(TK) 连接子与DSPE偶联(DSPE‑TK‑DCA),实现ROS响应释放;并设计Dna‑PBA两亲分子,通过静电作用和氢键高效包载siRNA,同样赋予ROS敏感释放特性。核磁共振波谱(¹H NMR)证实各中间体及终产物成功合成。2. 微流控法制备BIS‑LNPs@DCA‑siTNF,系统优化处方并表征
采用微流控技术筛选32种处方,确定最佳配比(胆固醇/DSPE‑PEG2000/DSPE‑PEG2000‑CLL‑1/DSPE‑DCA/Dna‑PBA/DPPC/PEG‑CXCR4 = 2/1/1/6/4/4/2)。所得纳米粒粒径约160 nm,PDI<0.3,Zeta电位约‑10 mV,siRNA包封率高。Cryo‑TEM显示颗粒呈均匀脂质体囊泡内包含“泡状”结构,在缺氧+ROS条件下结构崩解,实现响应性释放。体外释放实验表明,在50 mM H₂O₂及缺氧条件下,siRNA和地西他滨的释放速率显著加快。3. CXCL12介导的趋化作用增强BIS‑LNPs跨内皮穿透能力
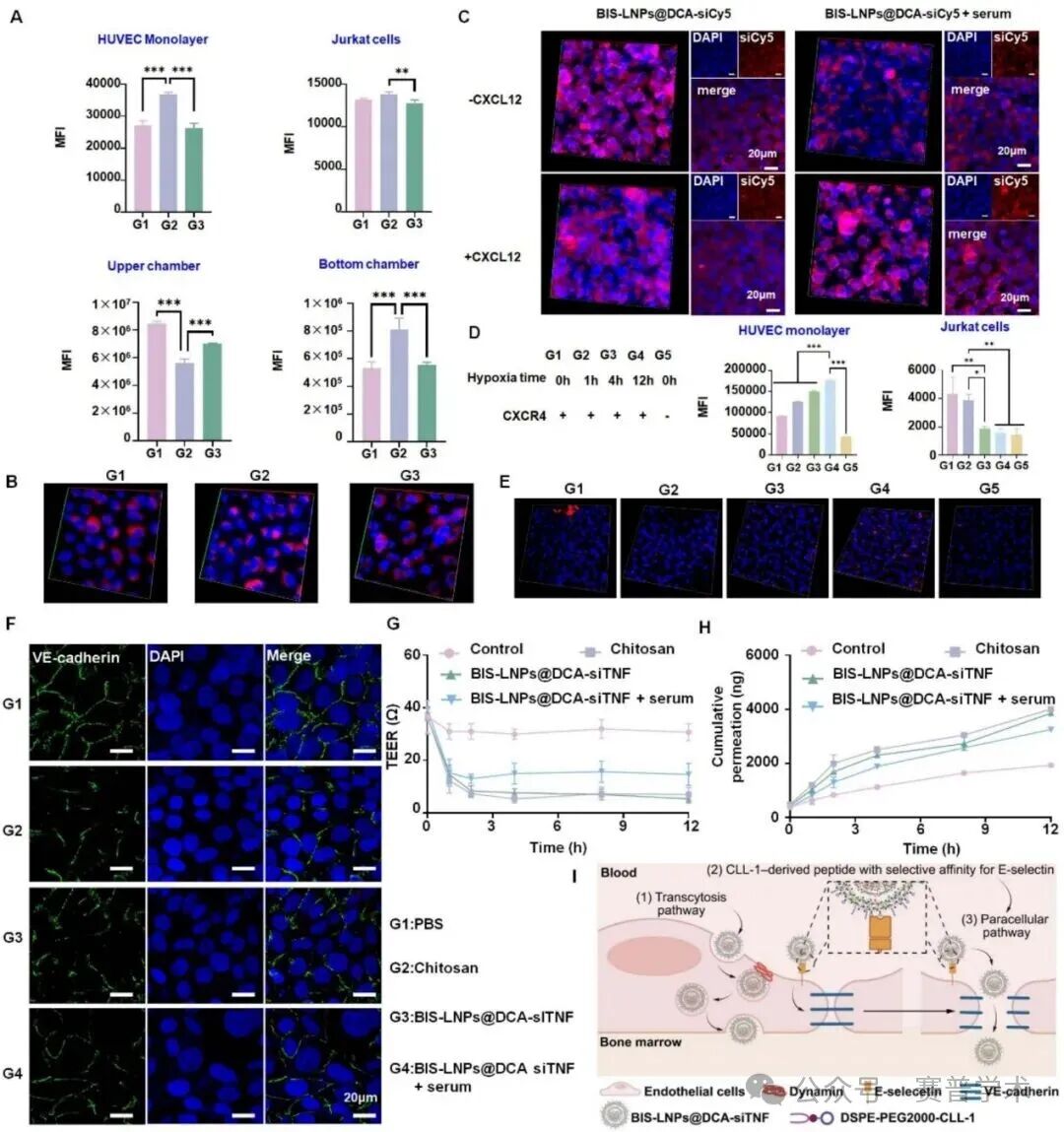
Transwell共培养模型(上室HUVEC,下室Jurkat细胞)显示:添加CXCL12后,Cy5标记的BIS‑LNPs在HUVEC和Jurkat细胞中的荧光强度显著升高;而CXCR4拮抗剂AMD3100预处理后穿透被抑制。蛋白冠形成不影响趋化性能。缺氧处理4 h后,PEG‑CXCR4逐渐脱离,LNP滞留于HUVEC内,而CLL‑1配体介导的旁细胞途径补偿性增强。VE‑cadherin免疫荧光染色及跨内皮电阻(TEER)下降证实CLL‑1配体可打开内皮细胞紧密连接,增强旁细胞通透性。4. Dynamin介导的外渗和转胞吞作用促进LNP跨越内皮屏障
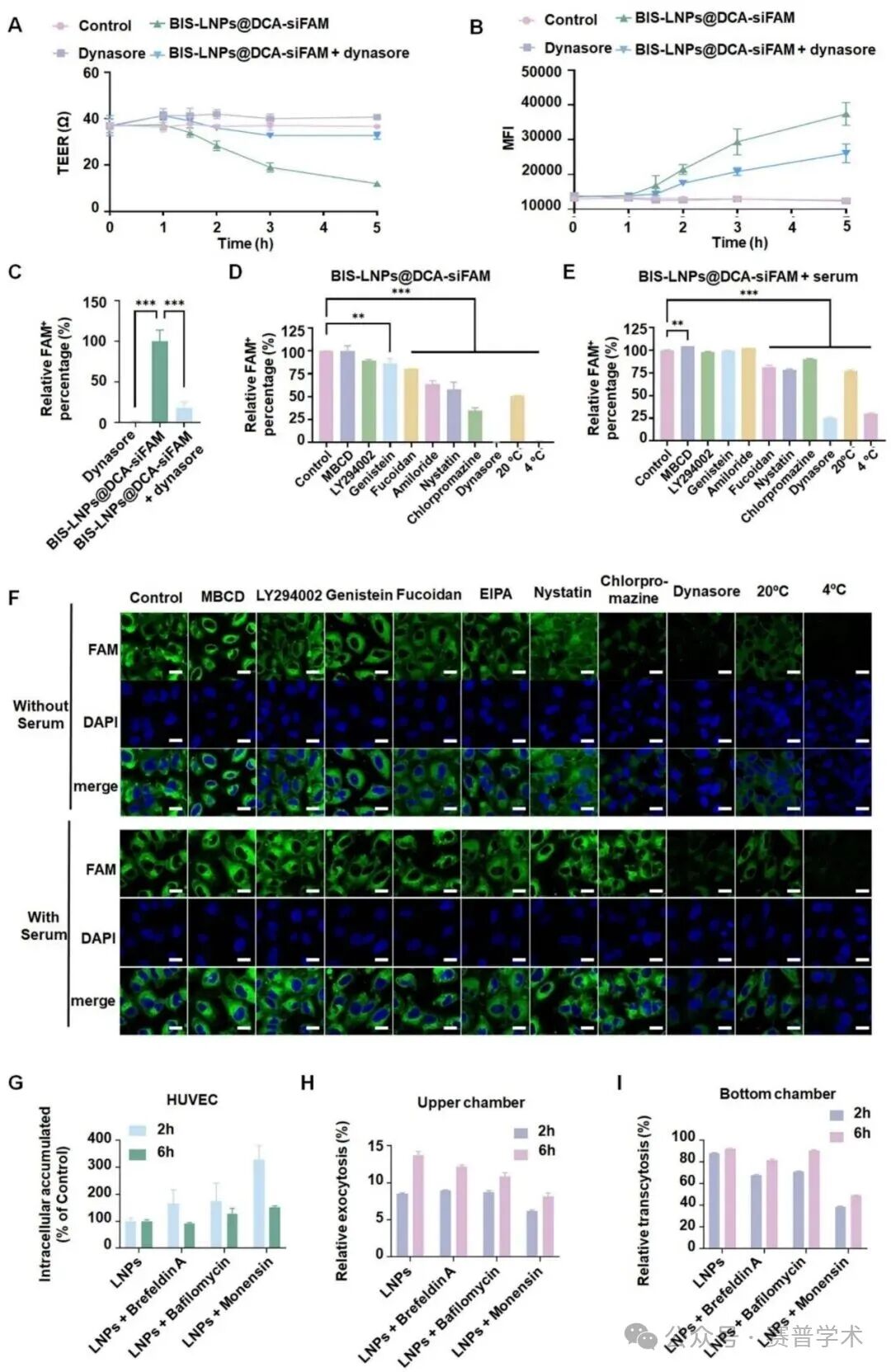
使用dynamin抑制剂dynasore可显著恢复TEER值、减少BIS‑LNPs的累积穿透量,并维持VE‑cadherin连续分布,表明dynamin依赖的旁细胞运输是CLL‑1介导的重要通路。内吞抑制剂筛选显示,氯丙嗪(clathrin途径)和dynasore分别抑制约60%和98%的细胞摄取,证明clathrin‑dynamin介导的内吞占主导。外排实验表明,莫能菌素(ER‑Golgi抑制剂)处理导致细胞内LNP滞留最高,提示ER‑Golgi途径是主要的外排路线。血清蛋白冠不影响内吞途径偏好。5. 体内骨髓龛靶向验证:双配体协同增强骨蓄积及内皮穿透
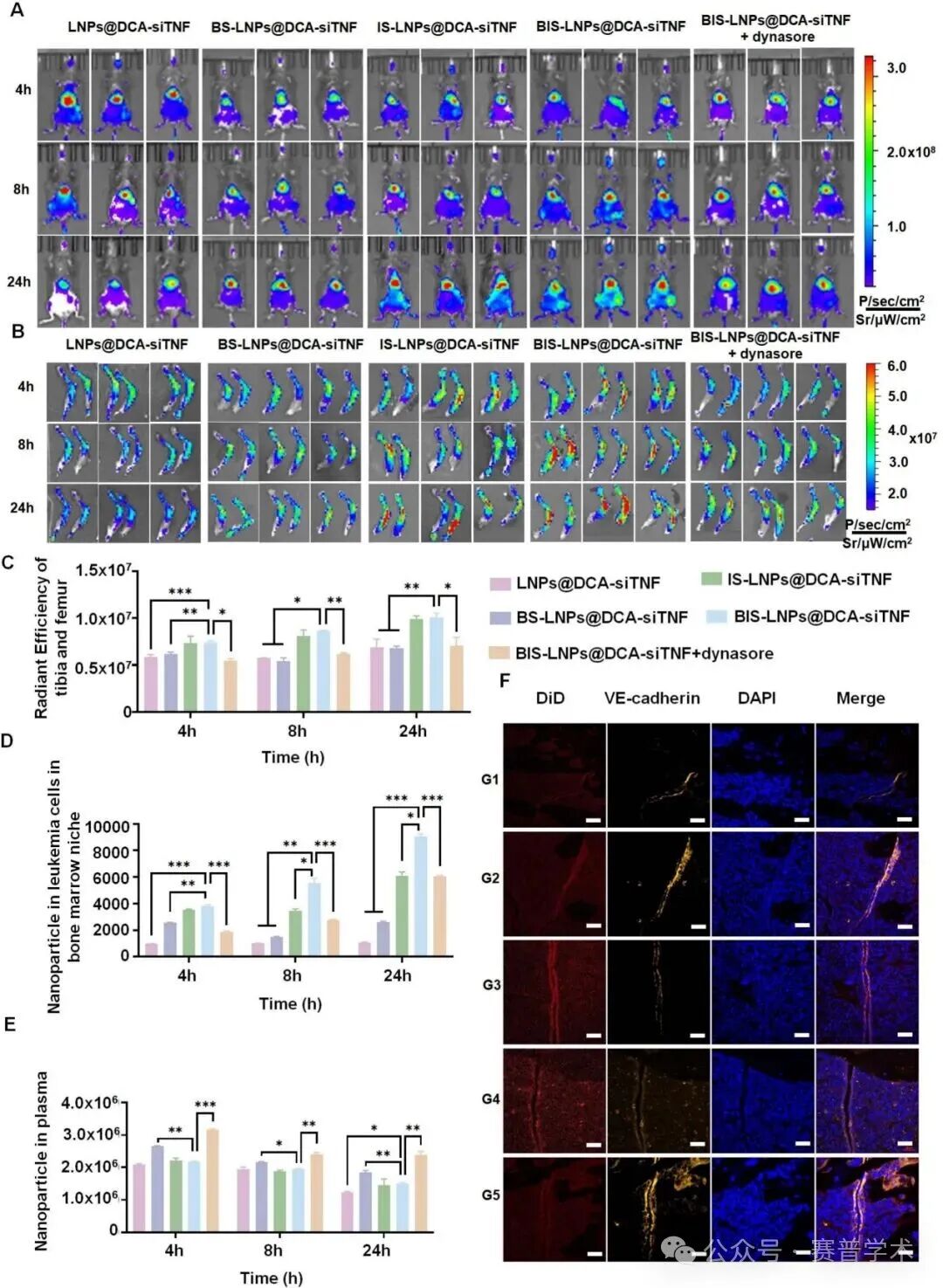
在C1498 AML小鼠模型中,DiD标记的BIS‑LNPs@DCA‑siTNF经尾静脉注射后,股骨荧光信号在4‑24 h持续强于单配体或非靶向组,且肝脾蓄积减少。dynasore联合给药显著抑制股骨荧光信号,同时增加血浆中纳米粒滞留,证实主动外渗过程依赖于dynamin。骨髓VE‑cadherin染色显示,IS‑LNPs(仅CLL‑1靶向)可降低VE‑cadherin信号,而BS‑LNPs(仅CXCR4靶向)无明显影响,证明CLL‑1配体直接参与紧密连接调控。6. 沉默TNF‑α破坏白血病‑脂肪细胞代谢支持
在低氧条件下,BIS‑LNPs@DCA‑siTNF处理C1498细胞后,Western blot显示TNF‑α、PI3K、p‑AKT、p‑NF‑κB显著下调。与脂肪细胞共培养模型中,BIS‑LNPs@DCA‑siTNF使脂肪细胞的ATGL、HSL、FABP4表达降低,油红O染色显示脂滴恢复,细胞外游离脂肪酸(FFA)水平下降,同时共培养的C1498细胞凋亡率升高。转录组测序(RNA‑seq)显示脂代谢相关基因(Fasn、Ldlr、Fabp4等)下调,KEGG富集分析表明脂肪细胞脂解、TNF信号通路、PPAR信号通路被抑制。7. 沉默TNF‑α调节破骨细胞分化,恢复骨稳态
白血病‑破骨细胞共培养模型中,BIS‑LNPs@DCA‑siTNF处理显著降低TRAP酶活性和TRAP阳性多核细胞数。RNA‑seq显示Wnt10a、Plcb2、Ccn4、Ptgs2、Tnf、Acp5等破骨相关基因下调,KEGG富集提示TNF信号通路、破骨细胞分化、NF‑κB信号通路被显著抑制。GSEA进一步证实PI3K‑AKT和NF‑κB通路负富集。细胞周期分析显示,处理组C1498细胞S期比例增加,从静止期进入活跃周期,增强对化疗的敏感性。8. 体内治疗效果:抑制白血病、激活免疫、改善运动功能并修复骨骼
在C1498原位AML模型中,BIS‑LNPs@DCA‑siTNF(G8)治疗组小鼠体重恢复、脾脏重量显著降低,骨髓和外周血中白血病负荷明显减轻(Wright‑Giemsa染色)。免疫组化显示HIF‑1α、FABP4和CXCL12表达下调。流式细胞术表明:骨髓中CD11b+Gr.1+ MDSCs减少约3倍,CD3+CD8+ T细胞增加14倍,外周血NK细胞(CD3−NK1.1+)和NKT细胞(CD3+NK1.1+)显著增多。行为学测试(转棒和旷场)显示运动协调和活动能力恢复。Micro‑CT和TRAP染色证实骨体积分数(BV/TV)增加约4倍,骨小梁结构恢复,破骨细胞活性被抑制。🌠图文鉴赏
Fig. 1. Fabrication and characterization of BIS-LNPs@DCA-siTNF.Fig. 2. Evaluation of BIS-LNPs@DCA-siTNF trans-endothelial penetration.Fig. 3. BIS-LNPs@DCA-siTNF utilizes dynamin-mediated Extravasation and transcytosis to traverse the endothelial barrier. The HUVEC monolayer was treated with PBS (Control), dynasore (a dynamin inhibitor), BIS-LNPs@DCA-siFAM and BIS-LNPs@DCA-siFAM+dynasore to evaluate the role of dynamin in nanoparticle transport.Fig. 4. In vivo evaluation of bone marrow niche targeting of BIS-LNPs@DCA-siTNF.原文链接:https://doi.org/10.1016/j.jconrel.2026.114874
信息来源:赛普学术



“汇聚南药”公众号所转载文章来源于其他公众号平台,主要目的在于分享行业相关知识,传递当前最新资讯。图片、文章版权均属于原作者所有,如有侵权,请在留言栏及时告知,我们会在24小时内删除相关信息。
本平台不对转载文章的观点负责,文章所包含内容的准确性、可靠性或完整性提供任何明示暗示的保证。
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。