告别传统药片,核酸药物引领精准医疗的新浪潮
发布时间:2026-04-17来源:药事纵横
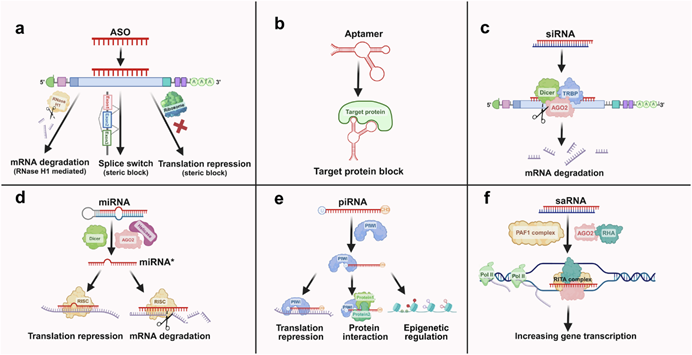
在现代医学漫长的发展历程中,人类对抗疾病的手段经历了从宏观到微观的深刻演变。传统的小分子药物和抗体药物主要致力于干预或阻断已经合成的蛋白质功能,这种方式在面对由基因异常引发的疾病时往往显得力不从心。随着生命科学的探索步入基因组与转录组时代,一种以脱氧核糖核酸或核糖核酸为药物主体的全新治疗模式应运而生。这类药物不再局限于对下游蛋白的物理干预,而是将治疗触角前移至生命信息的转录和翻译环节,通过对信使核糖核酸命运的精准干预,实现对蛋白表达的调控。这种从被动补充蛋白到主动调控生命的理念转变,标志着人类在疾病治疗领域取得了里程碑式的突破。图1. 不同类型小核酸的作用机制一、核酸药物的基本概况与代际演进
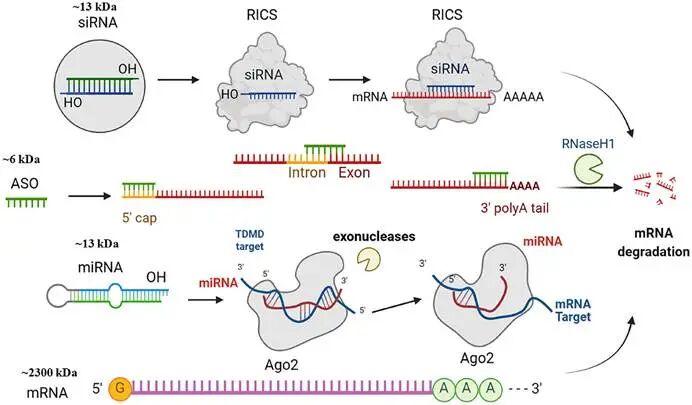
核酸药物在分子层面主要由十到五十个核苷酸通过磷酸二酯键连接而成,涵盖了核糖核酸、脱氧核糖核酸及其各类化学修饰衍生物。作为继小分子药物和抗体药物之后的第三大类药物,小核酸药物的核心优势在于遵循碱基互补配对原则,能够直接靶向疾病相关基因的信使核糖核酸或非编码核糖核酸。这种从基因源头进行调控的机制,成功破解了传统药物难以成药的靶点困境,展现出靶点特异性强、药效持续时间久、耐药风险低等显著特点。纵观全球核酸药物的发展轨迹,其技术演进呈现出清晰的代际更迭规律。核酸药物1.0时代(1990-2010年代),反义寡核苷酸技术确立了以阻断为核心的治疗策略。这类单链分子通过碱基互补配对结合靶标信使核糖核酸,进而阻断致病蛋白的翻译过程。随着化学修饰技术的日益成熟,反义寡核苷酸真正具备了成药属性。2016年诺西那生钠注射液获批治疗脊髓性肌萎缩症,该药物通过调节特定基因的剪接过程,显著改善了患儿的运动功能,成为反义寡核苷酸领域的划时代事件。2.0时代(2010年代至今)以“沉默”为核心,RNA干扰机制在细胞质中特异性降解靶标mRNA。小干扰核糖核酸进入细胞后与核糖核酸诱导沉默复合体结合,在细胞质中实现对靶标信使核糖核酸的特异性降解。2018年全球首款小干扰核糖核酸药物帕蒂斯兰获批用于治疗遗传性转甲状腺素蛋白淀粉样变性。随后靶向特定胆固醇调节蛋白的英克司兰于2021年获批,凭借每年仅需两次皮下注射即可持续降低低密度脂蛋白胆固醇的卓越表现,验证了小干扰核糖核酸高效的基因沉默能力。3.0时代(2020年代至今)以“表达”为核心,将编码蛋白的mRNA递送入细胞,利用人体自身核糖体实现治疗性蛋白的瞬时表达。这一阶段的代表性技术是将编码治疗性蛋白的信使核糖核酸递送入人体细胞,利用人体自身的核糖体实现治疗性蛋白的瞬时表达。二零二零年信使核糖核酸新冠疫苗的迅速问世与大规模应用,不仅验证了这一技术的颠覆性潜力,更向全球展示了核酸药物在应对突发公共卫生事件时的巨大价值。。图2.RNA治疗。包括siRNA、反义寡核苷酸(ASO)和microRNA(miRNA)二、多维视角下的作用机制与药物分类
不同类型的核酸药物在作用路径上存在显著差异,但均高度依赖碱基互补配对的分子识别特性。在基因沉默机制方面,小干扰核糖核酸主要介导靶标信使核糖核酸的切割降解,直接阻断异常蛋白的合成。反义寡核苷酸除了通过形成脱氧核糖核酸与核糖核酸杂合体招募酶类降解靶标外,还能通过阻断前体信使核糖核酸的剪接位点来调节蛋白表达模式,这为杜氏肌营养不良等因基因剪接异常导致的疾病提供了治疗可能。在基因激活层面,小激活核糖核酸能够通过招募特定的转录激活复合体,结合靶基因启动子或增强子区域,刺激基因转录的启动与延伸,为部分因基因功能缺失导致的遗传性代谢病开辟了新的干预途径。而在蛋白功能阻断方面,核酸适配体通过体外筛选技术获得独特的三维构象,能够像抗体一样特异性结合致病蛋白或病毒颗粒并阻断其生物学活性,同时具备热稳定性高和免疫原性低的优势。微小核糖核酸模拟物或抑制剂则通过模拟或抑制内源性微小核糖核酸的功能,实现对多个基因网络的宏观调控。这三大类技术在临床应用中各具优势。反义寡核苷酸能够穿透细胞核靶向核内的前体信使核糖核酸,在调节基因剪接方面具有不可替代的作用。核糖核酸干扰的优势在于其极高的基因沉默效率,在极低浓度下即可完成靶标降解,结合偶联技术实现的持久降脂作用正是基于这一机制。信使核糖核酸的最大优势则在于其瞬时表达特性,由于无需进入细胞核且不存在基因组整合风险,它在细胞质中翻译为蛋白质后即被降解,有效规避了基因治疗的长期安全性担忧,同时能够实现极为复杂的蛋白质功能。三、递送系统突破与给药途径演变
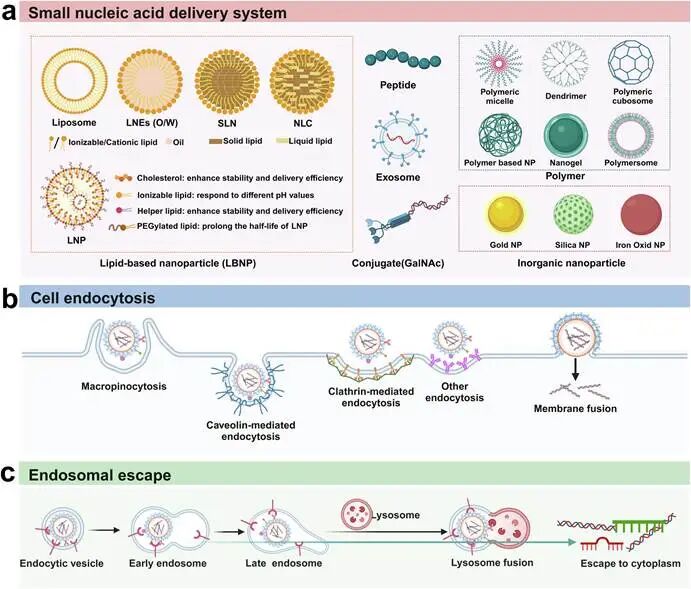
核酸药物的研发历程在很大程度上是一部递送技术的攻坚史。裸露的核酸分子在体内极易被核酸酶降解,且带有强负电荷,难以自主穿透细胞膜。因此,递送系统的持续突破成为了驱动核酸药物发展的核心力量。脂质纳米颗粒技术的成熟使得核酸药物能够高效靶向肝脏,而氮乙酰半乳糖胺偶联技术的出现则实现了肝细胞的特异性摄取。氮乙酰半乳糖胺能够与肝脏细胞表面高表达的特定受体特异性结合,这一技术拐点将人体代谢中枢肝脏变成了核酸药物能够系统性攻克的主战场。图3.用于递送小核酸的技术给药途径与递送系统密切相关,核心目标是突破细胞膜或血脑屏障等生物屏障并减少脱靶效应。皮下注射是目前最常用的全身给药方式,主要适用于偶联了靶向配体的药物,通过血液循环到达肝脏发挥作用。静脉注射则多用于核酸适配体类药物或需要快速起效的治疗场景。局部给药在突破特定生理屏障方面展现出独特价值,例如治疗脊髓性肌萎缩症的药物通过腰椎穿刺进行鞘内注射,直接将药物递送至脑脊液以靶向中枢神经系统。眼科疾病则广泛采用玻璃体内注射的方式。在剂量与给药频率方面,核酸药物因其长效性特点,给药间隔显著长于传统小分子或抗体药物。以治疗高胆固醇血症的药物为例,患者首次给药后三个月追加一次,此后每年仅需注射两次即可维持疗效。治疗遗传性疾病的药物在初始加载阶段可能需要较高频率的给药,进入维持阶段后也可将给药间隔延长至数月一次。这种超长效的给药范式极大提升了慢性病患者的用药依从性。四、从小分子到核酸序列的研发效率变革
核酸药物的核心特点在于其平台化与即用型的研发模式,这使得新药研发效率得到了质的飞跃。传统的的小分子药物和生物药从靶点发现到临床试验通常需要数年时间,而核酸药物在递送系统一旦验证成熟后,只需更换核糖核酸序列即可快速开发针对新靶点的药物。从序列设计到进入临床试验,整个周期可以缩短至数月。这种极高的研发敏捷性,使得核酸药物在应对快速变异的恶性肿瘤、开发个体化肿瘤疫苗以及应对突发传染病等方面具备了不可替代的战略优势。化学修饰技术的进步为核酸药物的研发效率提供了坚实保障。通过对核糖核酸骨架进行硫代修饰或在核糖环进行甲基化修饰,不仅大幅提升了核酸分子抵抗核酸酶降解的能力,还降低了免疫原性并改善了药代动力学特性。这些标准化的化学修饰模块与高通量序列筛选技术相结合,使得核酸药物的设计变得越来越像搭积木一样高效和模块化。五、从罕见病向慢性病的适应症空间拓展
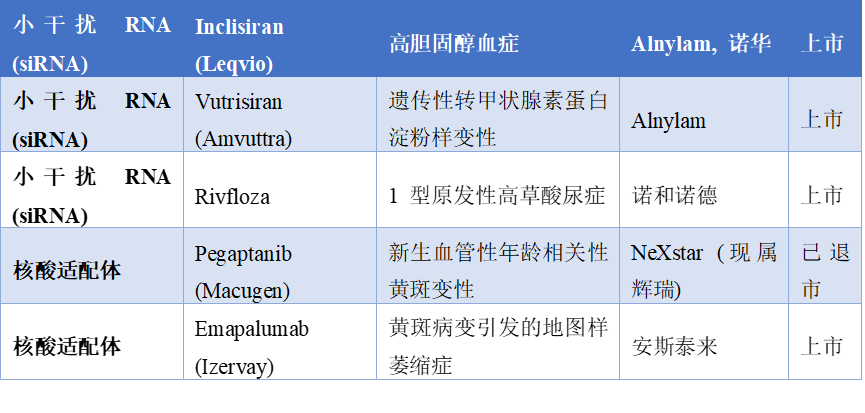
全球已获批上市的二十余款核酸药物在适应症选择上呈现出明显的演进轨迹。早期的研发主要集中在致病基因明确且未满足医疗需求迫切的罕见遗传病领域。这类由单个基因缺陷引起的疾病为核酸药物一对一的精准干预提供了理想场景,同时孤儿药认定等政策红利加速了上市进程,帮助企业快速完成了对技术平台安全性和有效性的初步验证。随着肝脏靶向递送技术的成熟,核酸药物的适应症空间迎来了爆发式拓展,成功从罕见病跨越至高胆固醇血症等常见慢病领域。靶向特定胆固醇调节蛋白的小干扰核糖核酸药物每年两次皮下注射即可强效降低低密度脂蛋白胆固醇,彻底打破了慢性病患者每日服药或频繁注射的传统模式。此后,针对高甘油三酯血症、血友病以及遗传性转甲状腺素蛋白淀粉样变性的多款核酸药物相继问世,展示了该领域在心血管代谢系统的巨大潜力。在传染病领域,针对慢性乙肝的小干扰核糖核酸药物通过沉默病毒共价闭合环状脱氧核糖核酸转录的信使核糖核酸,显著降低病毒载量,为功能性治愈乙肝提供了新思路。在肿瘤学领域,靶向特定癌基因的小干扰核糖核酸药物正在与免疫检查点抑制剂开展联合用药探索,旨在增强机体的抗肿瘤免疫反应。通过信使核糖核酸平台递送基因编辑工具,更为精准的基因修复提供了临床转化路径。六、结语
总的来说,核酸药物作为现代生物医药领域的第三大类药物,正以前所未有的速度和力度重塑着全球医药产业的格局。从最初通过阻断机制干预罕见遗传病,到利用沉默机制攻克心血管慢病,再到借助表达平台应对突发传染病,核酸药物完成了一场从补充蛋白到调控生命的壮丽跨越。其精准靶向基因的独特机制打破了传统药物的靶点限制,平台化研发模式则极大缩短了新药开发周期。当前,全球核酸药物市场正处于从罕见病治疗向常见病普及的历史性拐点。中国创新力量在这场浪潮中,正从早期的跟随者逐步转变为并跑者,并在部分前沿领域展现出领跑者的姿态。面向未来,随着肝外递送技术的逐一攻克、口服给药系统的成熟以及联合治疗策略的深入探索,核酸药物有望进一步扩大其治疗边界。随着技术的不断进步与临床数据的积累,小核酸药物有望成为慢性病领域、肿瘤领域等疾病精准治疗的重要突破口,从而为患者提供更有效、更安全、更个性化的治疗选择。[1] Sun D, Tan W, Zhao J, et al. Delivery of nucleic acid drugs for tumor therapy: Opportunities and challenges. Fundam Res. 2024 Jan 30;5(6):2948-2959. doi: 10.1016/j.fmre.2023.11.020.[2] Liu M, Wang Y, Zhang Y, et al. Landscape of small nucleic acid therapeutics: moving from the bench to the clinic as next-generation medicines. Signal Transduct Target Ther. 2025 Mar 10;10(1):73. doi: 10.1038/s41392-024-02112-8.[3] Bennett CF, Swayze EE. RNA targeting therapeutics: molecular mechanisms of antisense oligonucleotides as a therapeutic platform. Annu Rev Pharmacol Toxicol. 2010;50:259-93. doi: 10.1146/annurev.pharmtox.010909.105654.[4] Finkel RS, Mercuri E, Darras BT, et al. Nusinersen versus Sham Control in Infantile-Onset Spinal Muscular Atrophy. N Engl J Med. 2017 Nov 2;377(18):1723-1732. doi: 10.1056/NEJMoa1702752.[5] Springer AD, Dowdy SF. GalNAc-siRNA Conjugates: Leading the Way for Delivery of RNAi Therapeutics. Nucleic Acid Ther. 2018 Jun;28(3):109-118. doi: 10.1089/nat.2018.0736.
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。