保命与保乳不再二选一?浙江大学顾臻团队利用乳腺类器官,实现乳腺癌治疗与乳腺再生的统一


乳腺癌是女性最常见的癌症类型,对于广大乳腺癌患者而言,手术后的道路往往布满荆棘:切除不彻底,癌症可能卷土重来;切除过多,乳房的形态与功能又将永久受损。而传统的基于支架的填充方法,往往受限于其与人体天然组织的整合不足以及材料降解速度与组织发育速度不匹配。
因此,如何在根除肿瘤的同时,实现乳房(特别是乳腺)功能的完美重建,一直是横亘在外科医生和科学家们面前的巨大挑战。
该研究开发了一种工程化乳腺类器官(eMO),将乳腺类器官改造为一个集“抗癌”与“再生”于一体的智能微型“活细胞药物库”,小鼠术后乳腺癌模型中,其能够高效抑制肿瘤复发,同时能够自适应性地与乳腺整合以帮助重建,最终恢复泌乳能力,从而实现了抑制肿瘤复发与促进乳腺再生的双重奇迹。

传统疗法的“阿喀琉斯之踵”
目前的乳腺癌术后辅助治疗和重建手段各有局限:
全身化疗/放疗:“杀敌一千,自损八百”,副作用大,且对局部残留癌细胞的针对性不强;
人工填充材料:无论是硅胶假体还是生物支架,都可能引发排异、炎症,其降解速度也难以与人体组织生长同步。最关键的是,它们只是“填充物”,无法恢复“泌乳”这一核心生理功能。
脂肪移植:吸收率高,效果不稳定,且无法重建真正的乳腺腺体。
这些方法都无法从根本上解决 “治疗” 与 “再生” 之间的矛盾。
核心突破:让乳腺类器官变身“智能药厂”
这项研究的核心在于工程化乳腺类器官(engineered Mammary Organoid,eMO)。类器官(Organoid)是一类在体外培养的、能模拟真实器官复杂结构和功能的“迷你器官”。
研究团队的创新路径分为两步:
1、构建“泌乳车间”:研究团队先诱导乳腺类器官进入类似孕晚期的“泌乳状态”。此时,类器官的细胞内会产生大量脂质小滴——这原本是用来合成乳汁中脂肪的原料。
2、装载“智能导弹”:研究团队合成了一种新型前药 ATRA-DOX,它由抗癌药物阿霉素(DOX)和全反式维甲酸(ATRA)通过一个对酸极度敏感的化学键连接而成。这个前药能高效进入脂滴中,载药效率超过 85%。
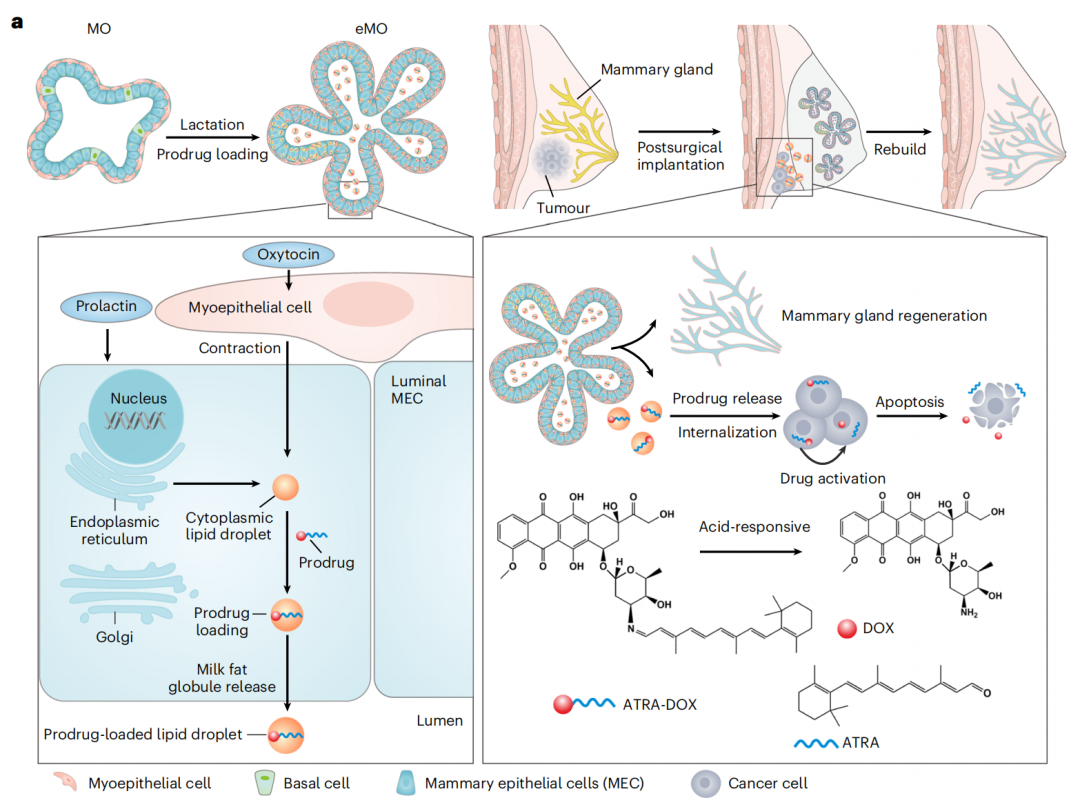
如何实现“一石二鸟”?
当载有 ATRA-DOX 前药的工程化乳腺类器官被植入手术切除肿瘤后的组织空腔时,一场精密的协同治疗与再生程序便启动了:
第一步:精准抗癌
定向分泌:类器官像正常乳腺一样,在肌上皮细胞收缩下,将满载前药的“脂滴胶囊”(模拟乳脂球)持续分泌到周围环境中。
精准引爆:残存的癌细胞会摄取这些脂滴,一旦进入酸性的肿瘤微环境,前药上的酸敏感化学键迅速断裂,释放出其中的阿霉素,从内部摧毁癌细胞。实验结果显示,该策略使小鼠模型肿瘤消退率达 96%,并有效激活了抗癌免疫反应。
第二步:原位再生
乳腺再生:在杀灭癌细胞的同时,这些植入的、具有活性的工程化乳腺类器官并未就此“躺平”。它们还能够自我适应,与宿主乳腺组织完美整合,促进新的乳腺导管和腺泡结构生长。
恢复泌乳:接受治疗的雌性小鼠,在愈后成功怀孕并分娩,其再生后的乳腺恢复了正常的泌乳能力。这证明了重建的不仅是外观,更是完整、有功能的生理单元。
从小鼠到人:临床转化的坚实一步
为了证明该策略的临床应用潜力,研究团队更进一步,利用人类诱导多能干细胞(hiPSC)成功培育出了“人源化乳腺类器官”,并重复了相同的工程化改造。在代表人类疾病的移植瘤模型上,人源化工程化乳腺类器官同样展现了强大的抑制肿瘤复发和促进组织再生的能力。
未来展望:通往个性化医疗的新范式
这项研究的深远意义在于,它提供了一种全新的“治疗即再生”的范式。与被动填充的异物不同,这种有生命的“类器官药物工厂”能与身体和谐共处,在完成任务后,其本身即转化为身体的一部分。
未来,通过使用患者自身细胞来构建类器官,我们有望实现完全个体化的术后治疗——不仅清除癌细胞,更能真正“还原”一个健康、完整的乳房结构和功能。
这不仅是一项科学技术的突破,更是献给乳腺癌患者的一份充满尊重与希望的未来礼物——战胜癌症,亦能保留完整与尊严。
值得一提的是,Nature Biomedical Engineering 期刊同期发表了题为:Living depots for breast cancer control and reconstruction 的评论文章,文章指出,顾臻团队开发的哺乳期诱导的乳腺类器官可作为自调控的活体药物库,在小鼠体内释放酸性激活的化疗药物,以抑制乳腺癌术后的肿瘤复发,同时促进乳腺组织再生。

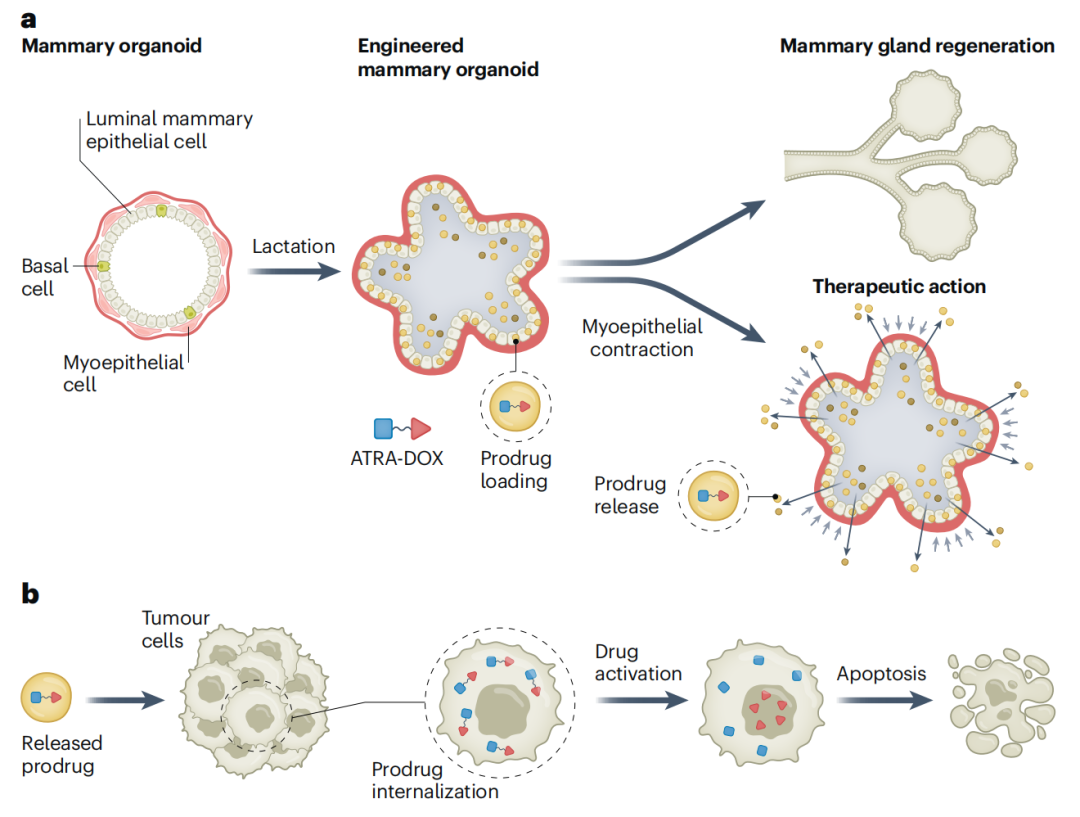
工程化乳腺类器官及其治疗作用的示意图
https://www.nature.com/articles/s41551-026-01655-1




点在看,传递你的品味




