确诊往往晚期,半数患者可能活不过5年!体检难查出,但依旧建议你这么做

卵巢癌,又被称为“妇癌之王”。因为它独特的生物学行为特点,常有患者在确诊时就已经是晚期了。
在中山大学肿瘤防治中心妇科的刘继红主任医师的诊室中,曾出现过这样的病例:有的患者,几个月前的超声还只有一个看起来是良性的小包块,没过多久,就迅速进展到了晚期。
“其实后来回头看,之前那个和子宫肌瘤难以区分的病变,可能已经是恶性的了。”
一篇2019年刊登在《柳叶刀-肿瘤学》(The Lancet Oncology)上的综述,将卵巢癌的特点总结为“七成活不过5年,七成患者复发,七成发现时已是晚期”。[1]
虽然随着治疗手段的发展,如今卵巢癌的5年生存率已有一些改善,但早诊断的困难,仍在很大程度上影响着它的预后。
超七成患者确诊即晚期
卵巢癌,是起源于卵巢或相关组织的恶性肿瘤,具有高度异质性和侵袭性。
总体而言,卵巢癌的发病率并不高。根据2022年的全球癌症统计,卵巢癌的标化发病率为每10万女性中6.7例,远低于更“知名”的乳腺癌、宫颈癌等。[2,3]
然而,因为具有“高复发率、低生存率”的特点,卵巢癌常被称为“妇癌之王”。
据2021年的统计数据,目前卵巢癌的总体5年生存率在50%左右。[4]对于这样一种癌症,早发现、早诊断、早治疗,自然是对预后极为关键的。但现实是,超七成的卵巢癌患者,在确诊时就已经是晚期了。[5]
刘继红就曾遇到过这样一个病人,3个月前的超声还并没有提示卵巢癌,仅仅3个月之后,就出现了大量腹水,最后病理提示为卵巢癌中最常见也是侵袭性最强的类型——高级别浆液性癌。
“这一类型的肿瘤最显著的特点就是突然发生、快速进展。这样的生物学特性也决定了,在早期往往难以识别。”
病理学研究表明,高级别浆液性癌在病灶非常微小的极早阶段,就可能已经在腹腔内完成播散,形成广泛的种植转移。[6]而这一时期,常用的影像学手段可能都无法探查到明确的病变。
在这样擅长“悄悄发育”的对手面前,许多筛查工具都显得有些一筹莫展。
例如,CA125是目前最常用的卵巢癌肿瘤标志物,也是浆液性癌的首选标志物。这项检查对于晚期卵巢癌及绝经后人群卵巢癌的预测价值较高,且其水平高低与疾病的进程有关,可以提示肿瘤的进展或消退。[2]
然而,CA125在卵巢癌中的表现受到肿瘤生物学异质性的影响。在临床上被诊断为早期的病例中,仅约50%的患者会出现CA125升高;同时,在健康人群及部分良性疾病中,也可能出现CA125升高。[7]这些情况,都会影响CA125对卵巢癌的诊断价值。
2011年发表在JAMA上的PLCO研究是一项涉及78216名女性的卵巢癌筛查RCT,结果显示,采用CA125联合经阴道超声筛查,并未降低卵巢癌死亡率,反而带来了不必要的手术风险。[8]
2016年发表在《柳叶刀》(The Lancet)上的UKCTOCS研究则纳入了超20万名女性,而这项更大规模的RCT也表明,不论是单独阴道超声筛查、还是阴道超声结合CA125筛查,都没有显著降低卵巢癌死亡率。[9]
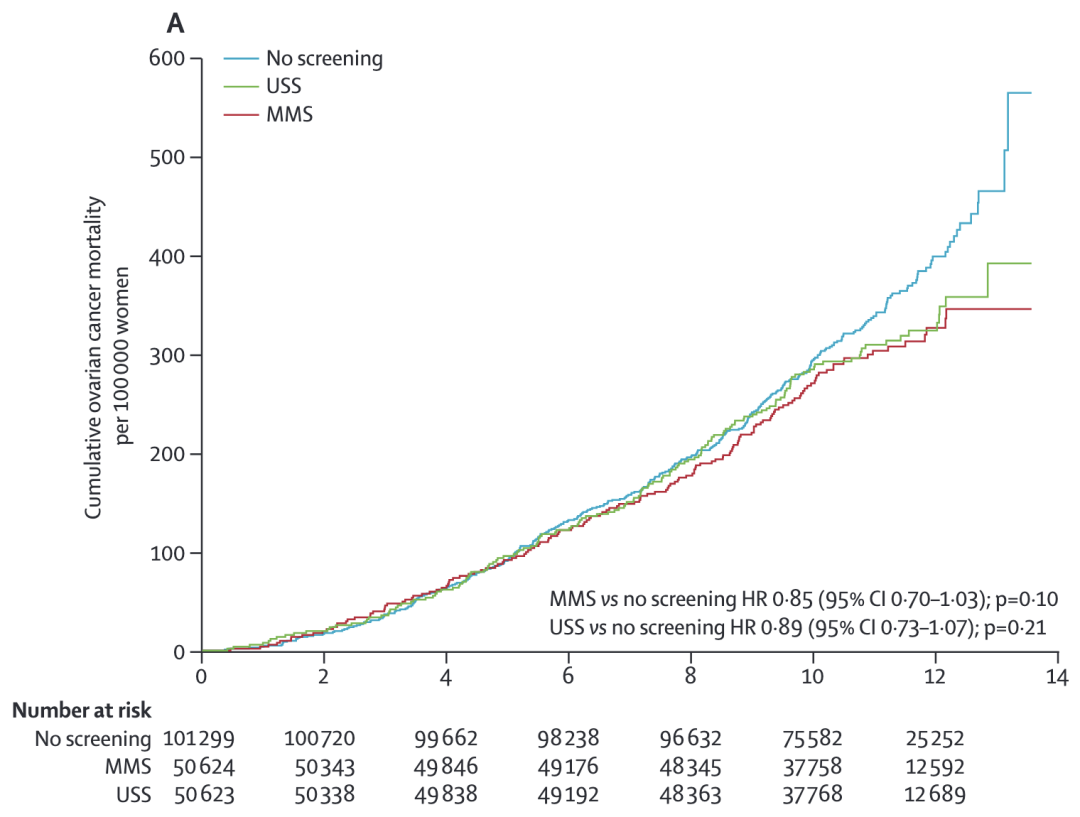
图源:参考资料8
也因此,目前学界普遍认为,在非高危人群中,无论是CA125、经阴道超声,还是二者联合,对卵巢癌的筛查效果都并不理想。
“妇癌之王”,其实也能预防
不过,对于这样一位隐匿的“杀手”,也并不是完全没有办法将它扼杀在摇篮中。
其中一个办法是,对于一些已经完成生育计划的女性,在她们因其他良性疾病(如子宫肌瘤、异常子宫出血)或为绝育而接受盆腔或腹部手术时,同时进行“机会性输卵管切除术”。
目前,国际妇产科学联盟(FIGO)、欧洲妇科肿瘤学会(ESGO)、美国妇产科医师协会(ACOG)等主流妇产科学术机构,都已将机会性输卵管切除术都已被视作一种低成本、低额外风险的卵巢癌一级预防策略。[10-12]
已有不少研究表明,在子宫切除术或绝育手术的同时进行输卵管切除术,并不会增加手术风险,也不影响卵巢功能,[11]但能显著降低普通人群的卵巢癌风险。
加拿大的一项队列研究显示,接受机会性输卵管切除的女性中未观察到浆液性卵巢癌病例,而根据对照组发病率推算的预期病例数为5.27例;[13]
另一项瑞典的队列研究显示,因良性疾病手术的同时进行双侧输卵管切除术,可使卵巢癌风险显著降低(HR=0.65,95% CI = 0.52~0.81);[14]
一项综合了77个原始研究的Meta分析显示,双侧输卵管切除术可以显著降低卵巢癌的发生率(OR=0.51)。[15]
为什么只切除输卵管,就能有这么好的卵巢癌预防效果呢?原理来自于病理学研究。
在“卵巢癌”这个名字下,包括了许多不同组织来源和分子特征的恶性肿瘤。比如最常见的“高级别浆液性卵巢癌”,其实通常是起源于输卵管的,最初表现为“输卵管上皮内癌”。[6]
另外,还有一部分卵巢癌起源于子宫内膜异位症,而真正起源于卵巢的卵巢癌,占比可能并不高。[6]
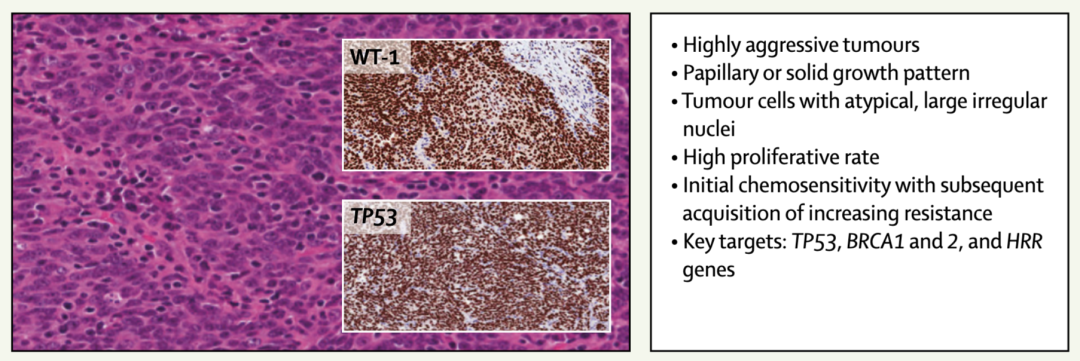
高级别浆液性卵巢癌的特点 图源:参考资料16
另一个问题是,这样一种对普通人群有效的一级预防方式,对高危人群来说可能并不足够。
“卵巢癌高危人群”,主要指携带BRCA1或BRCA2基因胚系突变的女性。研究显示,BRCA1和BRCA2胚系突变携带者一生中发生卵巢癌的累积风险分别可达54%和23%。[2]
对于这些人群,国内外指南推荐在一定年龄之后,考虑进行“降低风险的输卵管卵巢切除术”,也就是将输卵管和卵巢同时切除,更大程度预防卵巢癌的发生。[2,17,18]
研究显示,预防性输卵管卵巢切除术可使携带BRCA1/2变异女性的卵巢癌发病率降低80~90%,并使全因死亡率降低77%。[17]
目前指南普遍推荐,所有卵巢癌、输卵管癌、原发性腹膜癌患者进行BRCA1/2胚系突变检测,[18,19]并推荐特定乳腺癌患者也进行基因检测。[20]
然而,在一项针对中国妇科医生的全国性调查中,有69.7%的受访妇科医生表示,他们的患者中接受基因筛查的比例低于30%。[21]
“其实基因检测技术在国内已经非常成熟,可及性也很高。”刘继红指出,“但国内很多医生还没有形成主动向符合条件的患者推荐基因检测的意识,也没有预防性切除的概念。”
刘继红还记得自己曾遇到过一名患者,之前已经确诊过乳腺癌,并且也通过基因检测发现了BRCA变异,“但当时医生没有建议她做预防性切除,最终患者发展成晚期卵巢癌。这样的案例就很可惜。”
体检对个体仍然意义重大
一个好消息是,对于非高危人群来说,一生中发生卵巢癌的几率只有1~2%。与此同时,新的检测方法,也在给这个疾病的早诊断带来希望。
例如,已有一些研究证实,生物标志物HE4(人附睾蛋白4)在部分卵巢癌中具有更高的特异性。[22-24]HE4和CA125的联合检测,也已经在国内获得了较多的实践。
2024年,刘继红团队研究登上《柳叶刀-数字医疗》(The Lancet Digital Health),这项研究发现,基于人工智能模型的集成模型,能够辅助卵巢癌的精准诊断。[25]
不过,目前来说,一些新的诊断方法距离临床应用还有一些距离,卵巢癌的早诊断问题仍然存在。在缺乏有效人群筛查工具的情况下,仅依赖症状识别往往也不够敏感。
对于普通人而言,更现实的做法是,一方面提高对相关症状的警惕,在症状持续或反复出现时及时就医评估;另一方面,在医生指导下,根据个体情况合理选择相关检查手段,以尽可能在疾病负荷较低时获得线索。
“CA125和超声,作为大规模人群筛查时,可能整体效果并不理想。但对于一个个体而言,仍然很有价值。”刘继红表示。END
特别致谢:中山大学肿瘤防治中心妇科主任医师 刘继红
题图 Copyright © Elizabeth Sanduvete Chaves
本文由丁香园江子艺撰稿
推荐阅读
乳腺癌仍是女性过早死亡的主要原因,但许多患者感觉“被抛弃”
全球唯一可预防的癌症,每年夺走6万中国女性的生命
确诊往往已是晚期,很多人还不知道自己可能病了
点击阅读原文,访问柳叶刀主页
关注柳叶刀服务号,探索更多科研服务!
