指南解读|2026年版巴塞罗那临床肝细胞癌分期更新解读

2026年版巴塞罗那临床肝细胞癌(BCLC)分期继续保持分期、预后与治疗三位一体框架的简洁性,同时纳入了治疗领域的最新进展。此次更新的亮点在于引入复杂性、不确定性、主观性与情感因素(CUSE)临床决策框架,即通过综合现有循证医学证据,系统评估复杂性、不确定性、主观性及情感因素4个维度,指导多学科团队以病人为中心作出更加科学的个体化治疗决策。在具体治疗推荐方面,BCLC 0/A期肝细胞癌新增立体定向放疗和经动脉放射栓塞,作为手术治疗及消融治疗之外的重要根治性治疗选择;BCLC B期肝细胞癌强调现有证据尚不足以支持介入治疗联合系统治疗的常规应用;BCLC C期肝细胞癌则进一步巩固了免疫联合治疗方案作为一线首选方案的地位。
基金项目:国家自然科学基金项目(No.92574302)
作者单位:复旦大学附属中山医院 a.肝胆肿瘤与肝移植外科 b.介入治疗与肝胆肿瘤内科,上海 200032
通信作者:高强,E-mail:gao.qiang@zs-hospital.sh.cn
巴塞罗那临床肝细胞癌(Barcelona clinic liver cancer,BCLC)分期是目前国际应用最广泛的肝细胞癌(hepatocellular carcinoma,HCC)分期系统,由Llovet等[1]于1999年首次提出。相较于聚焦肿瘤解剖学分期的TNM分期系统,BCLC分期系统的核心创新在于整合病人的肿瘤负荷、肝功能储备及全身状况,构建预后分期,并将分期与治疗策略直接关联,形成分期、预后与治疗三位一体的框架。
BCLC分期自首次发布以来,已历经5次重大更新。2005年更新将直径<2 cm的孤立病灶细化为0期,最终形成由极早期0期至晚期D期的5期分期系统[2];2010年更新强化了局部消融治疗在早期肝细胞癌中的应用推荐[3];2016年更新强调了多学科诊疗模式在HCC管理中的重要性[4];2022年更新将中期肝细胞癌进一步细化为3个亚组,并引入“治疗阶段迁移”(treatment stage migration,TSM)和“无法治疗性进展”(untreatable progression,UTP)等新概念[5];2026年版更新则重点提出了全新的、以病人为中心的复杂性、不确定性、主观性及情感因素(CUSE)决策框架[6]。CUSE决策框架是指整合复杂性、多因素疾病及多种治疗方案,不确定性、预后模糊性及证据持续迭代,主观性、医务人员与病人对治疗方案选择的个体差异及偏好,以及情感因素、医务人员和病人的既往经历、期望与个人信念4个维度,并结合个人价值观、法律法规及卫生系统承载能力等情境因素,最终制定肝细胞癌治疗方案的过程。2026年版BCLC分期(图1)[6]与2022年版[5]相比,在肝细胞癌具体分期及预后方面变动不大,但进一步明确了BCLC B期的定义,即由原来的“多灶性”明确为“>3个肿瘤,或≤3个且至少1个肿瘤直径>3 cm”。
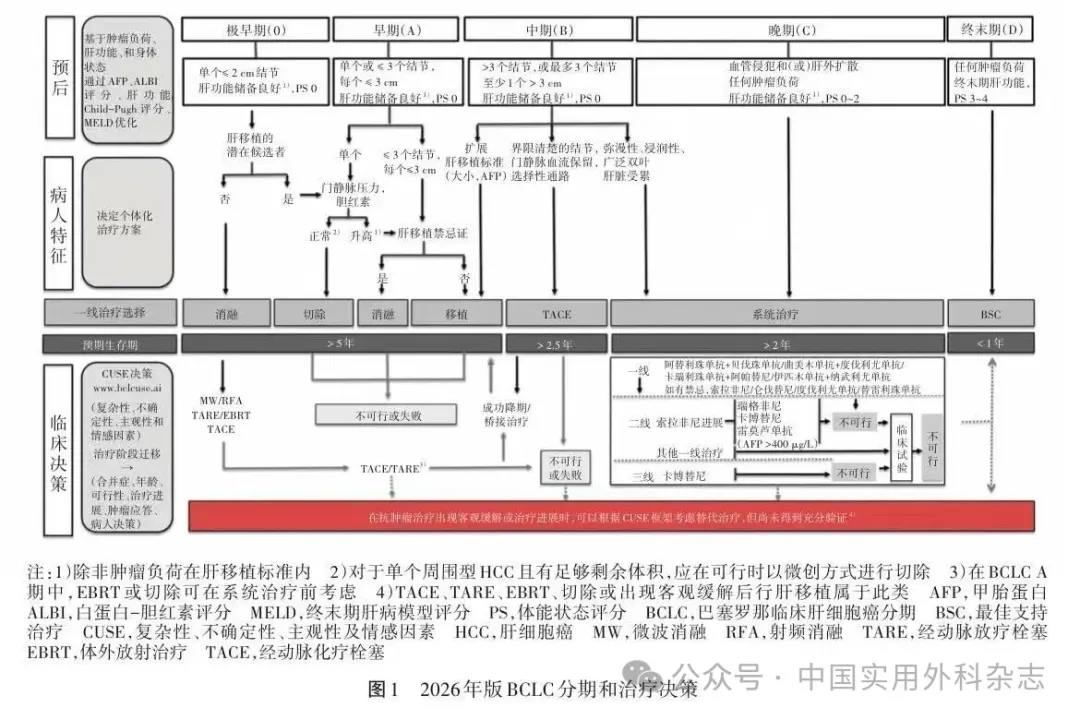
1 |以病人为中心的CUSE决策框架
CUSE框架的构建主要旨在解决两类常见的循证医学证据空白:一是缺乏总生存期(overall survival,OS)获益证据的治疗方案;二是不同治疗方案均具有OS获益证据,但缺乏头对头比较。前者包括两种情况:其一,虽有前瞻性Ⅲ期随机对照研究结果,但OS数据尚未成熟;其二,虽有无进展生存期(progression-free survival,PFS)获益证据,但缺乏OS结果。对于OS数据尚未成熟的方案,2026年版BCLC建议,在正式OS结果公布后,再于个体病人中启动相应治疗。例如,在IMbrave050研究中,尽管中期分析提示贝伐珠单抗联合阿替利珠单抗能够显著延长病人的术后复发时间,但最终研究结果显示OS为阴性,使系统治疗在肝细胞癌术后辅助治疗中的探索再次受挫[7]。
肿瘤局部控制所带来的PFS获益,可能伴随肝功能储备下降及治疗相关不良事件的发生,最终未必能够转化为OS获益。目前,在介入治疗联合系统治疗对比单纯介入治疗用于中期肝细胞癌的3项随机对照试验(randomized controlled trial,RCT)中,EMERALD-1[8]、LEAP-012[9]和TALENTACE[10]均以PFS为主要研究终点,并获得阳性结果。由于尚未获得OS阳性结果,LEAP-012研究近期已宣布提前终止。2026年版BCLC分期在CUSE决策框架中罗列治疗证据时,仍将包含OS终点的研究作为高级别证据,认为PFS作为相对脆弱的研究终点,仍不能替代OS。另一方面,2026年版BCLC分期亦指出,若某种能够带来PFS获益的治疗方案可明确增加病人获得根治性治疗的机会,亦可作为推荐方案。这也是目前国内局部治疗联合系统治疗作为多项转化治疗方案应用的基础之一。对于已有多项RCT证实具有OS获益的方案,可参考限制性平均生存时间、PFS、至治疗失败时间、缓解持续时间、质量调整寿命年,以及肝功能衰竭、肝移植、静脉曲张破裂出血等临床相关事件的累积发生率,作出具体治疗决策。
CUSE决策的实施包括6个环节(图2):(1)确立治疗目标。(2)评估肝功能储备、体能状态、合并症、治疗可实施性、经济承受能力及照护者支持能力等复杂因素。(3)根据证据的确定性与适用性进行分级评估,2026年版BCLC在补充材料中列出了对应BCLC 0~D期各期不同治疗方案的研究证据,未来将上线BCLC.CUSE.AI,以提供定制化、针对具体病例的循证依据评估。(4)开展多学科讨论。(5)形成具有决策依据及知情同意内容的文书。(6)根据治疗目标、病情变化及证据更新,对方案进行动态调整。
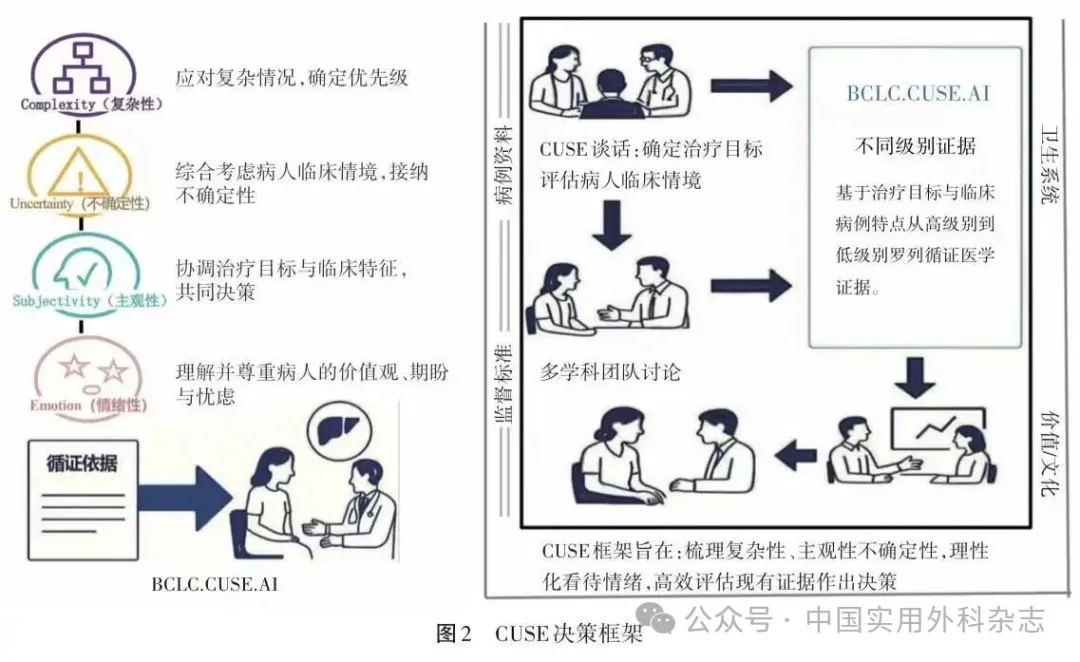
CUSE框架的提出标志着BCLC分期系统由单纯生物医学模型向整合生物-心理-社会医学模式的综合决策工具演进。然而,在具体临床实践中,CUSE的有效执行仍将面临多重挑战。一方面,决策制定依赖于大型医疗中心成熟、高效、定期运作且权责分明的多学科诊疗团队,对具体病例进行系统评估、多维权衡及深入沟通;在我国肝细胞癌病人基数庞大的背景下,可能面临诊疗效率下降的问题。另一方面,决策的最终确定需要病人及陪护人员深度参与。受教育水平、文化背景及对疾病认知程度等因素限制,并非所有病人均有意愿或能力参与复杂决策,反而可能加重诊疗过程中医患双方的无力感。
2 |不同分期肝细胞癌治疗推荐的更新
2.1 BCLC 0/A期肝细胞癌 2026年版BCLC分期对不同分期肝细胞癌的首选推荐方案与2022年版基本一致。对于多灶性BCLC A期、合并临床显著性门静脉高压(clinical significant portal hypertension,CSPH)的BCLC 0/A期,以及降期后满足移植条件的BCLC B期肝细胞癌,首选治疗为肝移植。对于无CSPH的BCLC 0/A期单发肝细胞癌,首选手术切除。与2025年EASL指南一致,欧美对于手术切除的指征仍较为严格。基于我国肝细胞癌病人基数庞大及肝源有限的现实情况,依据中国肝癌分期(China liver cancer staging,CNLC)指南,手术切除的适应证不仅包括多灶性BCLC A期肝细胞癌,还包括部分BCLC B期,即CNLC Ⅰb~Ⅱb期肝细胞癌;同时,局部治疗联合系统治疗作为有效的转化手段,进一步使部分BCLC C期,即局部晚期CNLC Ⅲa期肝细胞癌获得根治机会[11]。这亦体现了CUSE决策的地域差异性。对于不适合首选治疗的BCLC 0/A期病人,2026年版BCLC指南推荐采用CUSE决策。对于适合消融的病人,优选经皮消融术;对于肿瘤位置不适合经皮消融的病人,可行腹腔镜下消融;对于不适合消融术的病人,可选择经导管动脉化疗栓塞(trans-arterial chemoembolization,TACE)。经导管肝动脉放射栓塞术(trans-arterial radioembolization,TARE)与消融治疗疗效相当[12];外放射治疗(external beam radiation therapy,EBRT)中位OS可达5年[13],亦可作为补充选择。
2.2 BCLC B期肝细胞癌 对于不满足肝移植条件的BCLC B期病人,首选TACE。对于不适合TACE的病人,可考虑TARE[14-15]或EBRT[16]。尽管TARE在总体缓解率方面优于TACE,但两者OS获益相当,因此,TARE不作为中期肝细胞癌的首选推荐[14]。基于目前3项TACE联合免疫治疗及靶向治疗用于中期肝细胞癌的随机对照试验(randomized controlled trial,RCT),即LEAP-012[9]、EMERALD-1[8]和TALENTACE[10],仅显示PFS获益,尚缺乏OS获益数据,故2026年版BCLC分期及EASL指南均不推荐TACE联合系统治疗。尽管TACE+仑伐替尼[17]、TACE+阿帕替尼[18]及DEB-TACE+阿帕替尼[19]对比单纯TACE治疗中期肝细胞癌显示出显著的PFS和OS获益,但由于上述研究仅纳入我国病人,缺乏跨人群验证,因此,未被更新版指南推荐。对于弥漫性、浸润性及累及左右半肝的BCLC B期肝细胞癌,2026年版分期仍推荐将治疗阶段迁移至系统治疗。
2.3 BCLC C期肝细胞癌 对于BCLC C期肝细胞癌,2026年版分期在2022年版所推荐的阿替利珠单抗联合贝伐珠单抗[20]以及曲美木单抗联合度伐利尤单抗基础上,新增伊匹木单抗联合纳武利尤单抗[21]、卡瑞利珠单抗联合阿帕替尼[22]作为首选一线方案,后者纳入了17%的非亚洲地区病人。对于存在免疫治疗禁忌证的病人,可选择索拉非尼或仑伐替尼;对于存在靶向治疗禁忌证的病人,可选择度伐利尤单抗或替雷利珠单抗。尽管安罗替尼联合派安普利单抗[23]、经导管肝动脉灌注化疗[24]、多纳非尼[25]、信迪利单抗联合贝伐珠单抗生物类似药[26]以及特瑞普利单抗联合贝伐珠单抗[27]治疗晚期肝细胞癌,相较于索拉非尼或仑伐替尼亦显示出更显著的OS获益,但由于纳入病人主要局限于亚洲地区,且以中国人群为主,缺乏地域普适性,因此,在2026年更新版中未被推荐。对于不适合全身系统治疗的局部晚期病人,在CUSE决策框架下可选择TARE[28]或EBRT[29]。目前二线治疗的循证医学依据主要来源于索拉非尼治疗失败后的RCT研究,而在真实世界中,仅有极少数存在免疫治疗禁忌证或合并蛋白尿等无法耐受仑伐替尼的病人,于一线接受索拉非尼单药治疗。对于绝大多数一线接受以免疫治疗为基础的联合方案后进展病人的二线及后线治疗,目前尚缺乏高质量研究证据,因而推荐进入临床研究。
3 |结语
总体而言,2026年版BCLC分期在保持BCLC分期系统简洁性的同时,通过CUSE框架赋予临床决策更大的灵活性,以满足个体化治疗需求。由于BCLC分期作为西方主流指南,其循证医学证据的采纳更注重是否纳入足够数量的非亚洲,尤其是欧美人群,因此,在为我国肝细胞癌病人制定治疗方案时可作为重要参考,但仍存在一定局限性。事实上,我国在肝细胞癌新辅助治疗[30]、术后辅助治疗[31-32]、转化治疗[33]、中期肝细胞癌联合治疗[17-19,34]及晚期肝细胞癌系统治疗等方面[22-23,25-27],均已有高质量临床研究结果发表。相较于BCLC分期,更适用于我国肝细胞癌病人的CNLC分期及《原发性肝癌诊疗指南(2024版)》[11]具有更强的实用性。2025年,中国肝癌研究团队在ESMO公布的研究结果,包括卡瑞利珠单抗联合阿帕替尼围手术期治疗降低可切除肝细胞癌术后复发风险[30],以及转化切除显著改善阿替利珠单抗联合贝伐珠单抗治疗肝细胞癌总体生存预后[33],均为CNLC分期的进一步更新提供了新的高质量循证医学依据。当然,随着循证医学证据不断积累,多学科团队辅助CUSE决策实施亦将成为未来肝细胞癌治疗方案制定的重要趋势。人工智能时代信息整合能力的提升,也为治疗决策带来了新的机遇与挑战。
利益冲突 所有作者均声明不存在利益冲突
作者贡献声明 谢迪杨负责文献查询及初稿撰写;高强负责文章结构构思及全文审校
参考文献
(在框内滑动手指即可浏览)
[1] Llovet JM, Brú C,Bruix J. Prognosis of hepatocellular carcinoma: The BCLC staging classification[J].Semin Liver Dis,1999,19(3):329-338.DOI:10.1055/s-2007-1007122.
[2] Bruix J,Sherman M. Management of hepatocellular carcinoma[J].Hepatology,2005,42(5):1208-1236.DOI:10.1002/hep.20933.
[3] Forner A,Reig ME, de Lope CR, et al.Current strategy for staging and treatment: The BCLC update and future prospects[J]. Semin Liver Dis, 2010, 30(1):61-74.DOI:10.1055/s-0030-1247133.
[4] Bruix J,Reig M,Sherman M. Evidence-based diagnosis,staging, and treatment of patients with hepatocellular carcinoma[J]. Gastroenterology,2016, 150(4):835-853. DOI:10.1053/j.gastro.2015.12.041.
[5] Reig M,Forner A,Rimola J,et al.BCLC strategy for prognosis prediction and treatment recommendation: The 2022 update[J].J Hepatol,2022,76(3):681-693. DOI:10.1016/j.jhep.2021.11.018.
[6] Reig M,Sanduzzi-Zamparelli M,Forner A,et al. BCLC strategy for prognosis prediction and treatment recommendations: The 2026 update[J]. J Hepatol,2026, 84(3):631-654.DOI:10.1016/j.jhep.2025.10.020.
[7] Qin S, Chen M, Cheng AL, et al. Atezolizumab plus bevacizumab versus active surveillance in patients with resected or ablated high-risk hepatocellular carcinoma(IMbrave050):A randomised, open-label, multicentre,phase 3 trial[J]. Lancet,2023,402(10415):1835-1847. DOI:10.1016/S0140-6736(23)01796-8.
[8] Sangro B,Kudo M,Erinjeri JP, et al. Durvalumab with or without bevacizumab with transarterial chemoembolisation in hepatocellular carcinoma(EMERALD-1):A multiregional, randomised, double-blind,placebo-controlled,phase 3 study[J].Lancet, 2025,405(10474):216-232.DOI:10.1016/S0140-6736(24)02551-0.
[9] Kudo M,Ren Z,Guo Y,et al.Transarterial chemoembolisation combined with lenvatinib plus pembrolizumab versus dual placebo for unresectable,non-metastatic hepatocellular carcinoma(LEAP-012):A multicentre,randomised, double-blind,phase 3 study[J]. Lancet,2025,405(10474):203-215.DOI:10.1016/S0140-6736(24)02575-3.
[10] Dong J,Han G, Ogasawara S,et al. TALENTACE: A phase Ⅲ,open-label, randomized study of on-demand transarterial chemoembolization combined with atezolizumab + bevacizumab or on-demand transarterial chemoembolization alone in patients with systemically untreated, intermediate-to-high burden unresectable hepatocellular carcinoma[J]. Ann Oncol,2025,36(suppl):62.
[11] 中华人民共和国国家卫生健康委员会医政司.原发性肝癌诊疗指南(2024年版)[J].中国实用外科杂志,2024,44(4):361-386.DOI:10.19538/j.cjps.issn1005-2208.2024.04.01.
[12] Salem R,Johnson GE,Kim E,et al.Yttrium-90 radioembolization for the treatment of solitary,unresectable HCC: The LEGACY study[J].Hepatology,2021, 74(5):2342-2352.DOI:10.1002/hep.31819.
[13] Takeda A,Sanuki N, Tsurugai Y,et al.Phase 2 study of stereotactic body radiotherapy and optional transarterial chemoembolization for solitary hepatocellular carcinoma not amenable to resection and radiofrequency ablation[J]. Cancer,2016, 122(13):2041-2049.DOI:10.1002/cncr.30008.
[14] Ranganathan S, Gabr A, Entezari P,et al.Radioembolization for intermediate-stage hepatocellular carcinoma maintains liver function and permits systemic therapy at progression[J]. J Vasc Interv Radiol,2023, 34(6):968-975. DOI:10.1016/j.jvir.2022.11.036.
[15] Dhondt E,Lambert B,Hermie L, et al. Y-90 radioembolization versus drug-eluting bead chemoembolization for unresectable hepatocellular carcinoma: Results from the TRACE phase Ⅱ randomized controlled trial[J].Radiology,2022,303(3):699-710. DOI:10.1148/radiol.211806.
[16] Comito T,Loi M,Franzese C,et al.Stereotactic radiotherapy after incomplete transarterial(chemo-)embolization(TAE\TACE)versus exclusive TAE or TACE for treatment of inoperable HCC: A phase Ⅲ trial(NCT02323360)[J]. Curr Oncol,2022,29(11):8802-8813. DOI:10.3390/curroncol29110692.
[17] Peng Z,Fan W,Zhu B,et al.Lenvatinib combined with transarterial chemoembolization as first-line treatment for advanced hepatocellular carcinoma: A phase Ⅲ,randomized clinical trial(LAUNCH)[J]. J Clin Oncol, 2023,41(1):117-127. DOI:10.1200/JCO.22.00392.
[18] Kan XF, Liang B,Zhang XL,et al.Transarterial chemoembolization plus apatinib for unresectable hepatocellular carcinoma: A multicenter, randomized,open-label,phase Ⅲ trial[J]. BMC Med, 2025, 23(1):313. DOI:10.1186/s12916-025-04159-y.
[19] Duan X,Li H,Kuang D,et al. Comparison of drug-eluting bead transarterial chemoembolization combined with apatinib versus drug-eluting bead transarterial chemoembolization for the treatment of unresectable hepatocellular carcinoma: A randomized,prospective,multicenter phase Ⅲ trial[J].Signal Transduct Target Ther,2024, 9(1):304.DOI:10.1038/s41392-024-02012-x.
[20] Finn RS, Qin S, Ikeda M, et al.Atezolizumab plus bevacizumab in unresectable hepatocellular carcinoma[J].N Engl J Med,2020, 382(20):1894-1905.DOI:10.1056/NEJMoa1915745.
[21] Yau T,Galle PR,Decaens T,et al. Nivolumab plus ipilimumab versus lenvatinib or sorafenib as first-line treatment for unresectable hepatocellular carcinoma(CheckMate 9DW):An open-label,randomised, phase 3 trial[J].Lancet, 2025,405(10492):1851-1864.DOI:10.1016/S0140-6736(25)00403-9.
[22] Qin S, Chan SL,Gu S,et al. Camrelizumab plus rivoceranib versus sorafenib as first-line therapy for unresectable hepatocellular carcinoma(CARES-310):A randomised,open-label,international phase 3 study[J].Lancet,2023,402(10408):1133-1146. DOI:10.1016/S0140-6736(23)00961-3.
[23] Zhou J,Luo J, Bai Y,et al. Anlotinib plus penpulimab versus sorafenib in the first-line treatment of unresectable hepatocellular carcinoma(APOLLO):A randomised, controlled,phase 3 trial[J]. Lancet Oncol, 2025, 26(6):719-731. DOI:10.1016/S1470-2045(25)00190-1.
[24] Lyu N,Wang X,Li JB,et al.Arterial chemotherapy of oxaliplatin plus fluorouracil versus sorafenib in advanced hepatocellular carcinoma: A biomolecular exploratory, randomized,phase Ⅲ trial(FOHAIC-1)[J]. J Clin Oncol,2022,40(5):468-480. DOI:10.1200/JCO.21.01963.
[25] Qin S, Bi F,Gu S, et al. Donafenib versus sorafenib in first-line treatment of unresectable or metastatic hepatocellular carcinoma: A randomized,open-label,parallel-controlled phase Ⅱ-Ⅲ trial[J]. J Clin Oncol, 2021,39(27):3002-3011. DOI:10.1200/JCO.21.00163.
[26] Ren Z,Xu J, Bai Y,et al. Sintilimab plus a bevacizumab biosimilar(IBI305)versus sorafenib in unresectable hepatocellular carcinoma(ORIENT-32):A randomised,open-label,phase 2-3 study[J]. Lancet Oncol,2021,22(7):977-990. DOI:10.1016/S1470-2045(21)00252-7.
[27] Shi Y,Han G, Zhou J,et al.Toripalimab plus bevacizumab versus sorafenib as first-line treatment for advanced hepatocellular carcinoma(HEPATORCH):A randomised,open-label,phase 3 trial[J]. Lancet Gastroenterol Hepatol, 2025,10(7):658-670.DOI:10.1016/S2468-1253(25)00059-7.
[28] Garin E,Tselikas L, Guiu B,et al.Personalised versus standard dosimetry approach of selective internal radiation therapy in patients with locally advanced hepatocellular carcinoma(DOSISPHERE-01):A randomised,multicentre,open-label phase 2 trial[J].Lancet Gastroenterol Hepatol,2021, 6(1):17-29.DOI:10.1016/S2468-1253(20)30290-9.
[29] Dawson LA,Winter KA,Knox JJ, et al. Stereotactic body radiotherapy vs sorafenib alone in hepatocellular carcinoma: The NRG Oncology/RTOG 1112 phase 3 randomized clinical trial[J]. JAMA Oncol,2025, 11(2):136-144. DOI:10.1001/jamaoncol.2024.5403.
[30] Zhou J, Fan J, Wang Z, et al. Perioperative camrelizumab plus rivoceranib in resectable hepatocellular carcinoma (CARES-009): A randomized, multicenter, phase Ⅲ trial[J]. Ann Oncol, 2025, 36(suppl 2):821.DOI:10.1016/j.annonc.2025.08.2100.
[31] Li SH, Mei J, Cheng Y,et al. Postoperative adjuvant hepatic arterial infusion chemotherapy with FOLFOX in hepatocellular carcinoma with microvascular invasion: A multicenter, phase Ⅲ, randomized study[J].J Clin Oncol, 2023,41(10):1898-1908.DOI:10.1200/JCO.22.01142.
[32] Wang Z, Ren Z,Chen Y,et al.Adjuvant transarterial chemoembolization for HBV-related hepatocellular carcinoma after resection: A randomized controlled study[J]. Clin Cancer Res, 2018,24(9):2074-2081.DOI:10.1158/1078-0432.CCR-17-2899.
[33] Sun HC, Fan J, Shen F, et al. Liver resection versus continued atezolizumab plus bevacizumab in locally advanced hepatocellular carcinoma after atezolizumab plus bevacizumab treatment (TALENTop): A multicenter, open-label, randomized phase Ⅲ trial[J]. Ann Oncol, 2025, 36(suppl 2):821. DOI:10.1016/j.annonc.2025.08.2099.
[34] Li L,Xu X, Wang W,et al.Safety and efficacy of PD-1 inhibitor(sintilimab)combined with transarterial chemoembolization as the initial treatment in patients with intermediate-stage hepatocellular carcinoma beyond up-to-seven criteria[J].J Immunother Cancer,2025,13(1):e010035. DOI:10.1136/jitc-2024-010035.
【引用本文】高 强,谢迪杨. 2026年版巴塞罗那临床肝细胞癌分期更新解读[J]. 中国实用外科杂志,2026,46(3):338-342.
DOI:10.19538/j.cjps.issn1005-2208.2026.03.11


