Cell:高璞/高昂合作揭示细胞膜损伤的全新模式——纵向膜剪切,启动自毁程序,抵抗病毒传播


撰文丨王聪
编辑丨王多鱼
排版丨水成文
在微生物世界中,细菌与噬菌体(感染细菌的病毒)之间的攻防战从未停歇。为了生存,细菌进化出了多种精妙的免疫防御系统。其中,CBASS(基于环状寡核苷酸的抗噬菌体信号系统)是细菌和古菌中广泛存在的一种核心抗病毒策略,它被认为是哺乳动物 cGAS-STING 先天免疫通路的进化祖先。
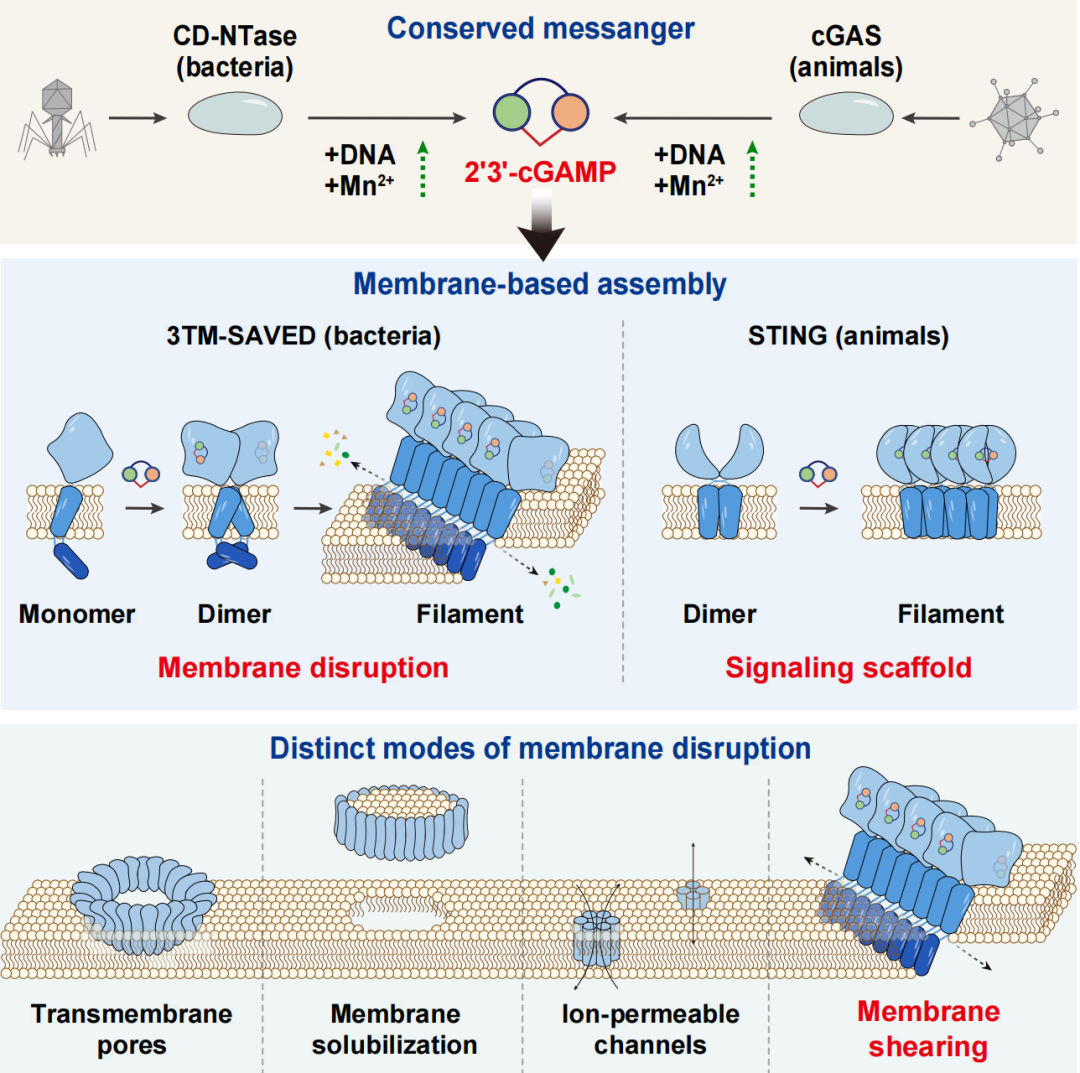
该研究系统揭示了原核生物中 2'3'-cGAMP 的生成方式、其特异性驱动下游跨膜效应蛋白发生聚集变构和高阶装配的机制,以及由此触发的一种此前未被认识的全新的膜损伤模式——纵向膜剪切,从而破坏细菌自身细胞膜,触发细胞死亡,与入侵的噬菌体“同归于尽”,阻止其进一步传播。

从信号到死亡:一条精密的防御流水线
CBASS 系统的运作就像一条精密的防御流水线。当噬菌体入侵时,细菌内的 CD-NTase 酶(类似于哺乳动物的 cGAS 酶)会检测到异常,并合成一种名为 2'3'-cGAMP 的环状二核苷酸信号分子。这个信号分子随后被下游的效应蛋白识别,最终触发细胞的“自毁”程序,与入侵的噬菌体“同归于尽”。
在众多效应蛋白中,跨膜蛋白是最主要的一类,存在于超过 40% 的 CBASS 系统中。它们被预测能够破坏细胞膜,但具体机制一直是个谜。
关键发现:逐步组装与纵向膜剪切
在这项最新研究中,研究团队聚焦于其中一种代表性蛋白——来自苏云金芽孢杆菌的 3TM-SAVED 效应蛋白。
研究团队利用冷冻电镜技术,首次完整解析了 3TM-SAVED 效应蛋白从“待机”到“激活”的全过程,并发现了一种全新的膜破坏机制。
1、高度特异性的激活
该研究发现,上游的 CD-NTase 酶能合成与哺乳动物 cGAS 酶产物完全相同的 2'3'-cGAMP。这个信号分子就像一把特制的钥匙,能精准地打开 3TM-SAVED 这把“锁”。其他结构类似的环状二核苷酸则无法有效激活它。
2、逐步的“变形记”
在没有信号分子时,3TM-SAVED 以稳定的单体形式存在。一旦结合 2'3'-cGAMP,它便开启了一场快速的形态剧变——
第一步:形成瞬态二聚体。两个单体蛋白通过跨膜区和胞内的 SAVED 结构域相互结合,形成一个对称的二聚体中间体。这个二聚体结构清晰展示了信号分子如何像“分子胶水”一样,桥接并稳定两个 SAVED 结构域。
第二步:组装成高阶丝状体。二聚体并不稳定,它们会进一步首尾相连,组装成延伸的丝状结构。这是实现膜破坏功能的关键形态。
3、前所未有的破坏机制:纵向膜剪切
最令人惊讶的发现在于丝状体如何破坏细胞膜,传统的膜破坏蛋白通常通过膜打孔或膜溶解实现。而 3TM-SAVED 丝状体采用了一种截然不同的策略——纵向膜剪切。
在丝状体结构中,蛋白的跨膜结构域和两亲性发夹结构发生了重排,它们排列成两列具有相反疏水/亲水面的垂直偏移阵列。当这个丝状体在膜上组装时,就像一把“分子犁”插入脂质双层,沿着丝状体组装轴,将细胞膜垂直“剪切”,导致细胞膜被分裂成两个错位的脂质层(上下错位的脂质层并未完全分离,而是仍由蛋白纤维以一定方式松散连接),从而形成线性排列的孔洞,这些孔洞能够允许水、离子和小分子通过,最终导致膜通透性增加并触发细胞死亡。
意义与展望:连接两域的免疫桥梁
这项研究的突破性意义在于:
揭秘了长期未知的机制:首次阐明了 CBASS 系统中最主要的效应蛋白——跨膜蛋白是如何将信号识别转化为膜破坏和免疫激活,填补了该领域的知识空白。
定义了一种全新的膜破坏范式:“纵向膜剪切”机制的发现,为理解跨生命域的膜破坏的原理增添了全新章节,其可能广泛存在于其他跨膜防御蛋白中。
揭示了深刻的进化联系:细菌合成 2'3'-cGAMP 的机制与哺乳动物 cGAS 酶高度相似,而跨膜效应蛋白的激活也可能为理解更复杂的真核免疫系统(例如 cGAS-STING 通路下游的膜重塑事件)提供线索。
此外,理解细菌这种“自毁式”防御的精细调控机制,不仅加深了我们对生命进化史上免疫系统起源的认识,也可能为未来开发新型抗菌或抗病毒策略提供灵感。
https://www.cell.com/cell/abstract/S0092-8674(26)00344-2




点在看,传递你的品味




