国际关注 | JAMA 发表耶鲁学者研究结果:基于替代终点获批的突破性治疗药品往往缺乏上市后研究要求
发布时间:2026-04-20来源:中国食品药品监管杂志
JAMA发表耶鲁学者研究结果:基于替代终点获批的突破性治疗药品往往缺乏上市后研究要求
根据2024 年8 月27 日在线发表在《美国医学会杂志》(JAMA)的一项研究结果,使用替代终点支持药品审批而不要求上市后研究,可能“妨碍患者和临床医生做出准确和知情的决策”。
获得突破性治疗药品认定的药品,可继续获得加速审批或传统审批;尽管FDA 要求对获得加速审批的药品开展上市后研究,但对获得传统审批的突破性药品,通常不要求进行上市后研究,即便主要终点采用替代指标。
耶鲁大学结局研究与评价中心研究员Maryam Mooghali 及其同事在发表于JAMA Network Open 上的一项研究中表示:尽管如此,先前的研究还是对肿瘤和非肿瘤治疗用药的替代指标与其预测的临床结局之间的关联提出质疑,研究结果表明,用于为FDA 批准这些适应症提供信息的替代指标与临床结局(如总生存期或生活质量)并不一致。
Mooghali 及其同事评估了自2012 年突破性药品认定计划启动以来至2023 年12 月31 日之间所有FDA 通过突破性治疗药品认定通道批准的关键临床试验中所采用的主要终点。还调查了FDA 是否要求或请求进行额外的上市后研究,以确认根据替代指标获批药品的临床疗效。
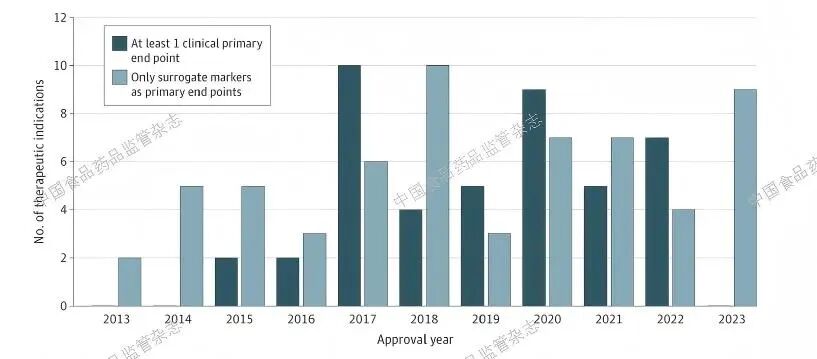
获得FDA 批准的药品中,越来越多地以替代指标为主要疗效终点,而不是以临床结局为主要疗效终点。临床结局衡量的是治疗效果,例如评估患者的感觉、功能或存活情况,而替代指标使用的是实验室测量结果或成像结果,在衡量临床结局时,采用了这些替代指标。
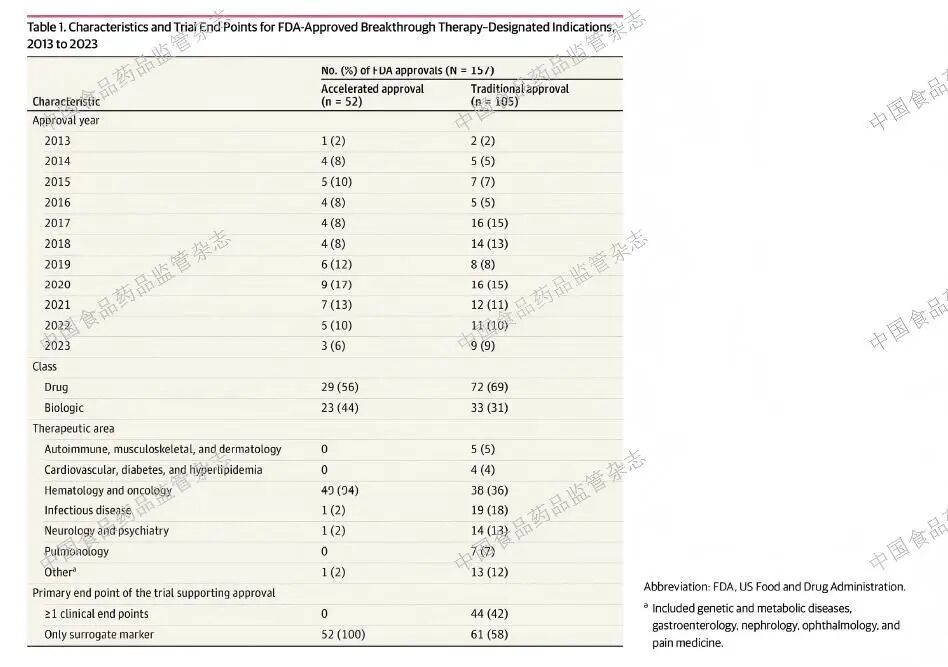
2013~2023 年,FDA 批准了157 种获得突破性治疗药品认定的疗法,其中52 种(33%)获得加速批准,105 种(67%)获得传统批准。
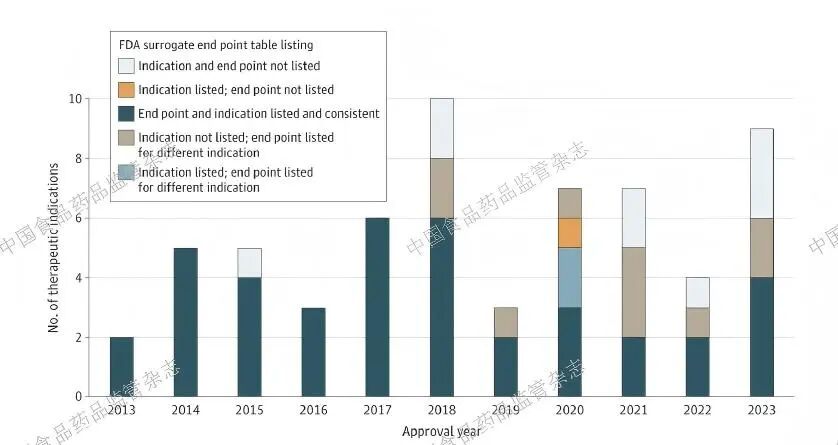
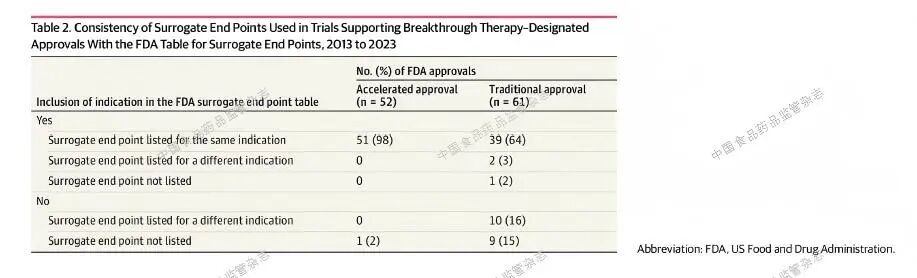
所有加速审批均基于以替代指标为主要终点的关键性试验,FDA要求对这些药品开展上市后研究以确认疗效。半数以上的传统获批药品(58%)基于依赖替代终点的关键性试验,其中只有4 种药品(7%)被要求完成上市后研究以确认疗效。在获得传统批准的突破性治疗药品中,近三分之二(64%)依赖于FDA 认可的用于相同适应症的替代标志物。
文章作者表示,在加速审批中,FDA 要求开展上市后研究,以确认所有突破性治疗药品所针对的适应症的预期临床疗效,而基于替代标记物的传统审批则不同,FDA 一般不要求开展上市后疗效研究。
尽管最近的研究显示,与通过其他通道获批的药品相比,通过突破性治疗药品认定通道获批的药品,总生存期更高,但有人士担心,这种认定可能意味着临床获益的特殊程度,从而在公众和临床医生中造成一种错误观念,错误地认为这些药品通过治愈严重疾病或改善患者的生活质量或生存率,大幅改善患者的预后。
作者得出结论认为,证据表明,相当一部分医生曲解了突破性治疗药品认定在证据标准方面的含义,包括该认定自动赋予了获得加速审批的资质。因此,当突破性治疗药品认定所针对的适应症的获批,是基于替代终点而非临床结局,同时没有一致的上市后要求来确认获益时,这可能会阻碍患者和临床医生做出准确、知情的决策。
①Mooghali M, Wallach JD, Ross JS, Ramachandran R. Premarket Pivotal Trial End Points and Postmarketing Requirements for FDA Breakthrough Therapies. JAMA Netw Open.2024;7(8):e2430486.doi:10.1001/jamanetworkopen.2024.30486.
Welcome Everyone To Subscribe
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。