CTLA-4抗体如何重塑抗肿瘤免疫应答?
一、CTLA-4在T细胞活化中扮演什么角色?
CTLA-4又名CD152,是表达于活化T细胞表面的免疫球蛋白超家族成员,与共刺激分子CD28高度同源,共享CD80及CD86配体。CD28与配体结合后传递共刺激信号,促进IL-2产生、T细胞存活、增殖及分化,是T细胞完全活化的关键第二信号。与之相反,CTLA-4通过与CD28竞争性结合CD80/CD86,阻断共刺激信号,同时通过胞内结构域传递负性调控信号,抑制T细胞活化。在免疫应答初期,CTLA-4表达水平有限,CD28信号占优势,T细胞被激活并扩增;随着T细胞活化,CTLA-4表达上调,在免疫应答后期竞争性抑制CD28信号,下调或终止T细胞反应。这一负反馈机制维持免疫稳态,防止过度免疫损伤。此外,表达于调节性T细胞表面的CTLA-4对驱动调节性T细胞抑制功能至关重要,聚集于肿瘤组织中抑制抗肿瘤免疫。CTLA-4表达受到严格调控,活化后迅速内吞从细胞表面去除,以避免对快速T细胞激活反应的过度抑制。
二、CTLA-4如何通过多种机制抑制T细胞功能?
CTLA-4通过至少三种机制抑制T细胞活化。第一,竞争性拮抗B7-CD28共刺激信号。CTLA-4与CD80/CD86的亲和力远高于CD28,可通过占据配体阻止CD28获得共刺激信号。第二,直接传递抑制信号。CTLA-4与TCR-CD3复合物上的ITAM相互作用,破坏T细胞激活所需的生化信号级联。T细胞激活的起始由Lck和Fyn对TCR-CD3复合物ITAM的磷酸化介导,磷酸化的ITAM结合ZAP70的SH2结构域,进而通过激活衔接蛋白和酶效应物触发免疫反应。CTLA-4与ITAM的相互作用从本质上破坏了这一信号传导,ZAP70、SYK和Fyn也是CTLA-4直接抑制的潜在靶点。第三,CTLA-4还可在免疫突触处与TCR-CD3复合物直接相互作用,干扰T细胞受体信号的起始放大。阻断CTLA-4后,肿瘤浸润的调节性T细胞功能被钝化,从而增强瘤内免疫应答。
三、CTLA-4抗体如何发挥抗肿瘤作用?
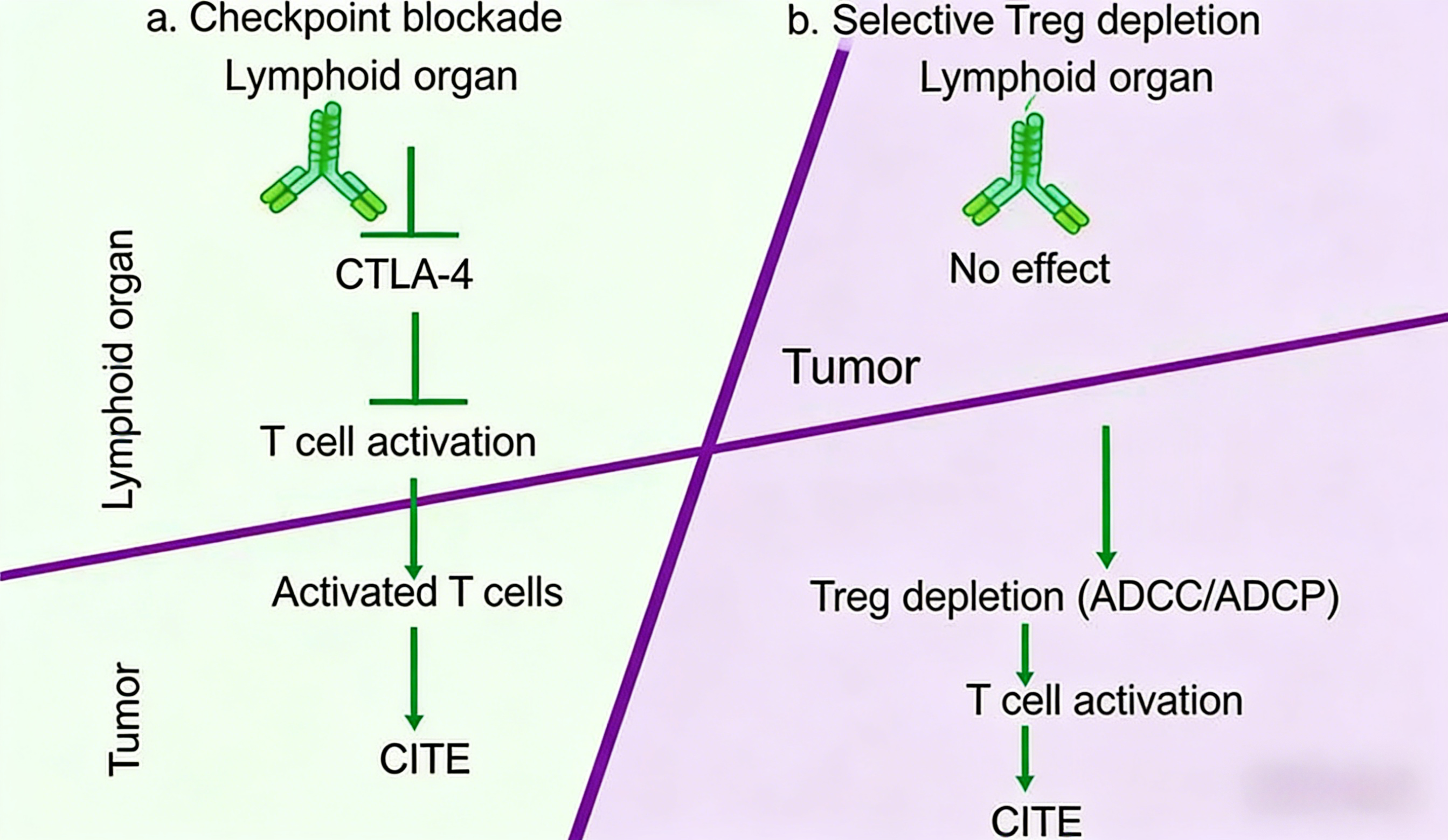
CTLA-4抗体作为首个获批的免疫检查点抑制剂,通过双重机制增强抗肿瘤免疫。一方面,抗体阻断CTLA-4与CD80/CD86的相互作用,解除对CD28共刺激信号的竞争性抑制,恢复T细胞活化信号。另一方面,CTLA-4抗体通过Fc段介导的抗体依赖的细胞介导的细胞毒作用,选择性清除肿瘤微环境中高表达CTLA-4的调节性T细胞,解除其免疫抑制效应。阻断CTLA-4后,肿瘤浸润调节性T细胞功能被钝化,效应T细胞活性增强,瘤内免疫应答显著改善。这一机制使CTLA-4抗体在黑色素瘤等肿瘤中展现出持久疗效,部分患者成为长期幸存者。机体对肿瘤细胞的免疫应答始于肿瘤特异性抗原的暴露和释放,抗原提呈细胞吞噬肿瘤抗原后呈递给T细胞,在淋巴结形成致敏的效应T细胞,随后T细胞浸润肿瘤释放更多抗原。CTLA-4抗体在这一全过程中解除抑制,放大抗肿瘤免疫循环。
四、CTLA-4抗体在自身免疫病及移植免疫中有何应用?
CTLA-4参与维持自身免疫耐受,其功能缺陷与多种自身免疫病易感性相关。CTLA-4外显子1中的单核苷酸多态性与多发性硬化症、糖尿病、甲状腺炎等自身免疫疾病及自然流产倾向有关。抗体介导的CTLA-4阻断可阻止耐受性发展,增强抗肿瘤反应,但可能加剧自身免疫疾病,因此在应用时需权衡疗效与安全性。在移植免疫中,CTLA-4信号通路是诱导移植物耐受的重要靶点。CTLA-4融合蛋白通过结合CD80/CD86,阻断CD28共刺激信号,已获批用于类风湿关节炎等自身免疫病的治疗。
五、CTLA-4抗体开发面临哪些挑战与机遇?
CTLA-4抗体的临床应用面临疗效与安全性的双重挑战。单药治疗在多数实体瘤中疗效有限,仅黑色素瘤等少数肿瘤显示出显著获益。免疫相关不良反应发生率较高,包括腹泻、皮疹、结肠炎及垂体炎等,严重时可危及生命。联合治疗是CTLA-4抗体的主要发展方向,与PD-1/PD-L1抗体联用可同时阻断T细胞活化早期及效应阶段的抑制信号,在黑色素瘤、肾细胞癌等瘤种中展现出协同增效。新型CTLA-4抗体通过Fc段工程化改造,增强调节性T细胞清除活性,同时减少对效应T细胞的非特异性消耗,有望优化疗效与安全性平衡。
六、小结
CTLA-4作为T细胞活化的负调控分子,通过竞争性拮抗B7-CD28信号、直接传递抑制信号及调节调节性T细胞功能,在维持免疫稳态中发挥核心作用。CTLA-4抗体通过阻断抑制信号及清除调节性T细胞,增强抗肿瘤免疫,开创了肿瘤免疫治疗的新纪元。尽管面临疗效与安全性的挑战,CTLA-4抗体与PD-1/PD-L1抗体的联合策略及新一代抗体的工程化改造,正推动其在精准肿瘤免疫治疗中发挥更重要的作用。
