VEGFR抗体如何切断肿瘤营养供给?
一、VEGFR2在血管生成中扮演什么角色?
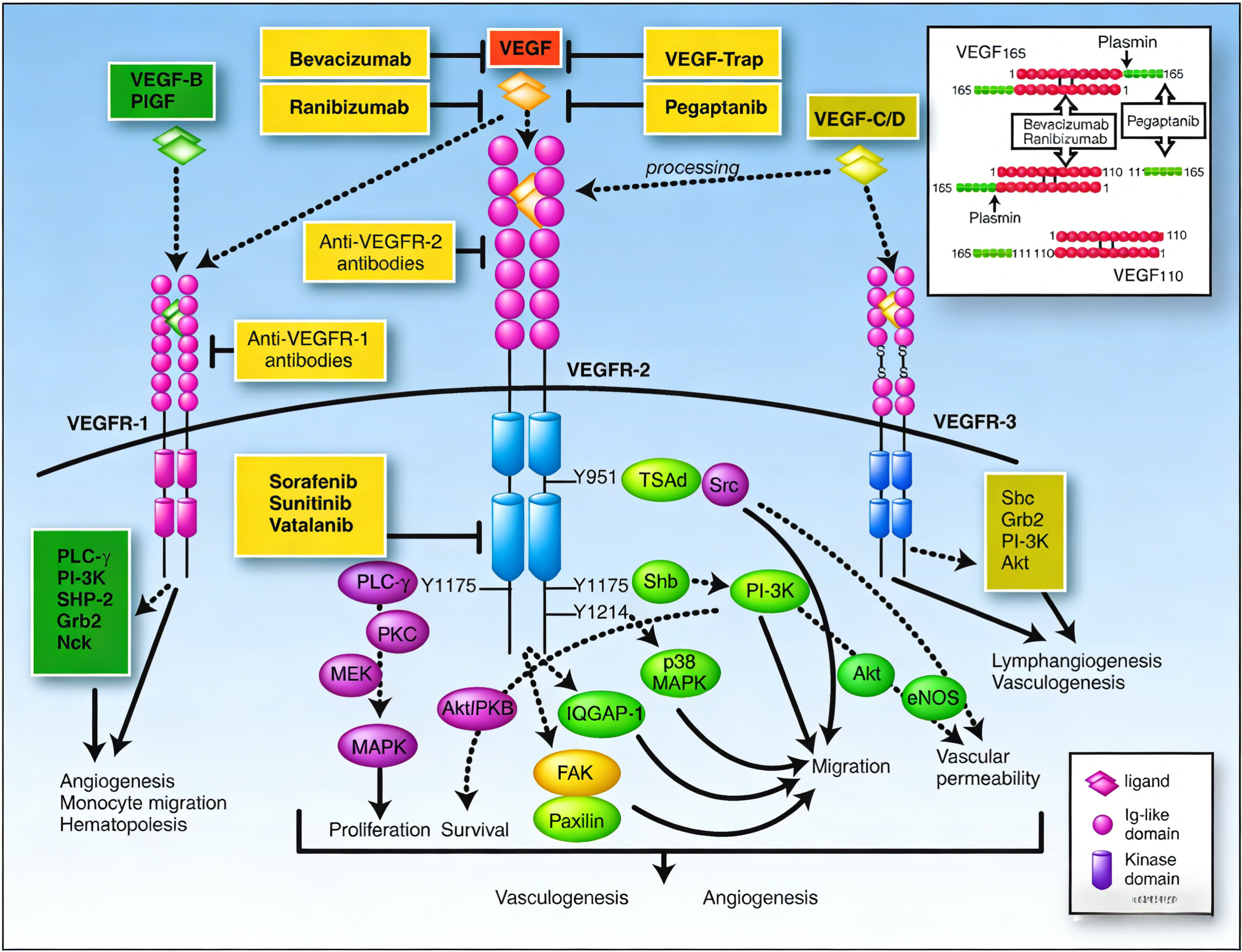
VEGFR2是血管内皮生长因子的主要细胞表面受体,在血管生成、血管发育、血管通透性调节及胚胎造血中发挥核心作用。VEGF家族包括五个成员:VEGF-A、VEGF-B、VEGF-C、VEGF-D及胎盘生长因子,其中VEGF-A与VEGFR2的亲和力最高,是驱动血管生成的关键配体。当VEGF与VEGFR2结合后,受体发生二聚化并激活下游信号通路,包括RAS/RAF/MEK/ERK通路促进内皮细胞增殖,PI3K/AKT通路促进内皮细胞存活及迁移。VEGFR2胞外区由七个类免疫球蛋白亚基组成,跨膜区锚定于细胞膜,胞内区包含催化酪氨酸激酶结构域。在肿瘤微环境中,肿瘤细胞分泌大量VEGF,通过旁分泌方式激活内皮细胞VEGFR2,诱导新生血管形成,为肿瘤生长提供氧气和营养。因此,阻断VEGFR2信号通路已成为抗血管生成治疗的核心策略。
二、靶向VEGF-VEGFR2通路的策略有哪些?
目前针对VEGF-VEGFR2通路的干预策略主要分为三类。第一类是靶向配体的药物,包括抗VEGF单克隆抗体,通过中和VEGF阻断其与受体的结合;VEGF-Trap可溶性受体融合蛋白,同时结合VEGF-A、VEGF-B及胎盘生长因子;还有靶向VEGF的siRNA药物。第二类是靶向受体胞内酪氨酸激酶的小分子抑制剂,如索拉非尼、舒尼替尼等,通过阻断激酶活性抑制下游信号传导。这些药物已广泛应用于多种实体瘤的治疗。第三类是靶向VEGFR2胞外区的单克隆抗体,通过竞争性结合VEGFR2,阻断配体与受体的相互作用。与靶向配体的策略相比,VEGFR2抗体可同时阻断所有VEGF家族成员通过该受体介导的信号,理论上具有更全面的抗血管生成效应。
三、VEGFR2抗体如何发挥抗肿瘤作用?
VEGFR2抗体通过特异性结合VEGFR2的胞外区,竞争性阻断VEGF与受体的结合,从而抑制受体二聚化及下游信号通路活化。这一干预导致多重抗肿瘤效应:抑制内皮细胞增殖与迁移,减少肿瘤新生血管形成;促进现有血管正常化,改善肿瘤微环境缺氧状态;增加化疗及免疫治疗药物的肿瘤渗透;协同增强抗肿瘤免疫应答。临床前研究显示,VEGFR2抗体单药可抑制多种肿瘤模型生长,与化疗、放疗或免疫检查点抑制剂联用时疗效进一步增强。目前,VEGFR2抗体已在胃癌、非小细胞肺癌、结直肠癌等多种实体瘤中展现出临床价值。
四、VEGFR2抗体与VEGF抗体有何异同?
VEGFR2抗体与VEGF抗体虽同属抗血管生成药物,但作用靶点及机制存在差异。VEGF抗体中和可溶性配体,仅阻断VEGF-A,而VEGFR2抗体阻断受体,可同时阻断VEGF-A、VEGF-C、VEGF-D等多种配体通过VEGFR2介导的信号。VEGFR2抗体还可能通过抗体依赖的细胞介导的细胞毒作用清除表达VEGFR2的肿瘤血管内皮细胞,产生直接细胞毒效应。在临床应用上,两者适应症有所重叠但不完全相同,VEGFR2抗体在胃癌中的疗效尤为突出。VEGFR2抗体的使用不依赖于肿瘤组织VEGF表达水平,而VEGF抗体在VEGF高表达肿瘤中可能更有效。
五、VEGFR2抗体开发面临哪些挑战?
VEGFR2抗体的临床开发面临多重挑战。首先,抗血管生成治疗易产生耐药,肿瘤可通过上调替代促血管生成因子如FGF、PDGF等逃逸VEGFR2阻断。其次,VEGFR2在正常组织血管中也有表达,长期阻断可能导致高血压、蛋白尿、出血等血管相关副作用。第三,VEGFR2抗体的最佳联合策略尚未统一,与化疗、靶向治疗或免疫治疗的时序及剂量需精细优化。此外,预测疗效的生物标志物缺乏,限制了优势人群的筛选。目前仅有少数VEGFR2抗体获批上市,多数在研药物仍处于临床前或早期临床阶段,竞争激烈。
六、VEGFR2抗体的未来发展方向是什么?
新一代VEGFR2抗体的开发正朝着多靶点协同方向演进。双特异性抗体将VEGFR2与PD-1、PD-L1或TGF-β等靶点结合,可同时阻断血管生成与免疫抑制,协同增强抗肿瘤效应。抗体偶联药物将细胞毒性载荷精准递送至肿瘤血管内皮细胞,实现靶向杀伤。联合治疗策略的优化是提升疗效的关键,VEGFR2抗体与免疫检查点抑制剂联用可重塑肿瘤微环境,促进T细胞浸润与功能恢复。生物标志物的开发将助力患者筛选,VEGFR2表达水平、肿瘤血管密度及循环VEGF水平等可能预测治疗反应。随着对抗血管生成机制理解的深化,VEGFR2抗体有望在精准肿瘤治疗中发挥更重要的作用。
