囊性听神经瘤手术难度更大吗?聚焦肿瘤全切与面神经保护困局
囊性听神经瘤因其与面神经关系密切,对外科手术构成挑战。虽然全切是首要目标,但考虑到对患者生活质量的影响,保护面神经功能至关重要。一个标志性的挑战是蛛网膜平面的消失,尤其是在靠近脑干和面神经的区域。有时,结构不稳定和粘连导致的解剖平面缺失,使得全切缺乏安全的操作通道。囊性变性、反复的微出血以及促进瘤周纤维化的慢性炎症,可能破坏自然的分离界限。
囊性听神经瘤手术为何具有挑战?个体化手术决策是关键
囊性听神经瘤的研究主要强调与肿瘤大小和粘连程度相关的手术复杂性,而非入路依赖性的预后结果,这支持了基于听力状况、解剖特点和术者经验的个体化手术决策。
术者理解面神经在后颅窝和内听道内的解剖是基础。我们知道面神经起自脑干,位于前庭蜗神经的前上方,穿过桥小脑角池后进入内听道。听神经瘤由于肿瘤生长时常把面神经向前或前上方推移,故可出现神经拉伸成薄带状的情况,但也有相反的情况,即神经被推向后方、下方,甚至分散穿入肿瘤内。面神经有明确的蛛网膜鞘,因此其蛛网膜鞘是极好的分离平面,务必保护神经的血供。
经迷路入路有利于显露桥小脑角、内听道及脑干界面,因而有利于早期颅神经的识别,但毋庸讳言,经迷路入路在解剖上有明确而重要的限制,直接限制了其应用。小乳突或气化不良的乳突、高位或前移的颈静脉球、前移的乙状窦,以及既往乳突手术史,均可能限制手术通道,增大手术难度,同时影响内听道及桥小脑角的安全暴露,故宜根据具体情况选择替代入路。因此,系统、细致的术前影像学评估对入路选择有决定意义。
囊性听神经瘤成功手术案例一则
一名59岁男性,出现为进行性、严重的左侧听力下降。MRI显示左侧内听道和桥小脑角有一大小约2.9厘米的部分囊性病变,伴有轻度脑干受压,符合囊性听神经瘤诊断。患者取仰卧位,头转向右侧。完成 乳突切除和迷路切除 后,对内听道进行270度减压的骨骼化处理,并打开后颅窝及内听道硬脑膜。 囊液引流被刻意延迟 ,直至肿瘤结构、分离平面及邻近的神经血管结构被清晰界定。使用显微剪刀和吸引器,对肿瘤包膜上极与三叉神经之间(尤其是在塌陷的囊壁附近)的致密粘连进行锐性分离。通过 超声吸引器 对肿瘤实性部分进行瘤内减容,重建安全通道。
在缺乏清晰平面的区域,策略性地调整分离角度以降低损伤神经束的风险,优先采用锐性分离。在神经上保留一薄层囊壁,并使用精细的钩子和软棉片进行对抗牵引,从神经上剥离肿瘤边缘。最终实现了肿瘤的全切,未侵犯脑干或发生出血。术后以0.02 mA的电流对面神经进行强刺激,确认了神经功能完好。为防止术后脑脊液漏,进行了 多层闭合 。术后患者面神经功能为House-Brackmann I级。
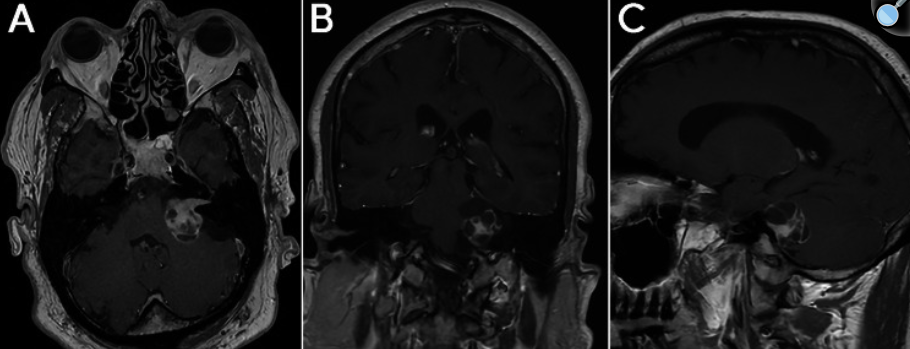
图1.术前轴位、冠状位及矢状位MRI,显示一大小约3厘米、部分囊性、呈对比强化的病变,扩大内听道并充满桥小脑角,符合Koos 4级 听神经瘤。
手术适应症与时机
手术切除适用于症状进行性加重、肿瘤生长或伴有脑干受压的患者。手术入路规划的关键决定因素是肿瘤形态、囊的位置以及听力状况。对于实用听力丧失由于经迷路入路能很好地在解剖结构变形之后早期、可靠地辨认脑干段及内听道段的面神经,因此对患者而言,经迷路入路是首选。位于前部或多房性囊肿更易扭曲脑干及神经结构,故此类病变宜尽早处理以避免不可逆的功能损害。近期出血或不稳定性与瘤周粘连程度加重、手术难度增大直接相关。对于因囊性占位导致脑脊液通路梗阻并有明显症状的患者,为缓解颅内压、防止神经功能恶化,减压手术确实十分紧迫。
囊性听神经瘤手术难点有哪些?
由于薄壁囊性听神经瘤可能发生塌陷、破裂,故常造成触觉反馈消失、结构扭曲、重要解剖标志模糊,因而更易对邻近神经产生牵拉、拉伸或热损伤。前部或内侧的囊肿常推移面神经,因此其脆弱性增大,识别起来更加困难。更重要的是,多房性囊性前庭神经鞘瘤与周围神经血管结构的界面关系极难预测,面神经走行常被囊肿本身模糊或遮蔽,尤其当囊膜破裂、塌陷而失去分离平面时。与面神经或脑干的致密粘连也直接限制了其可切除性。
首选方法是用显微剪刀做锐性分离,但此种方法有造成神经损伤的风险,因此当没有明确的分离平面、解剖结构严重变形,或肿瘤包膜与面神经、脑干难以分离时,主动修改分离轨迹或残留薄层肿瘤往往有利于保留功能、避免医源性损伤。故而原则十分清楚:在最大安全切除的基础上优先考虑功能。
即使最大安全切除也会有肿瘤再生长的风险,故原则上必然要长期随访。而既往手术或放疗所致的瘢痕组织常会使分离平面模糊,难以可靠分离,故追求全切除极易造成不可接受的神经功能缺损。极少数情况下会发生这样的——肿瘤直接侵犯神经,很难在不牺牲功能的前提下做到完全解剖学分离。
如何避免并发症?
由于预防并发症要依靠预见性、警惕性及应变能力,因此外科医生应当主动根据术中监测结果及解剖变化及时调整治疗方案,力求做到最大安全切除。囊性听神经瘤的解剖平面消失使得钝性分离具有危险性,尤其是在肿瘤包膜致密粘连时。 锐性、有控制性的分离技术 常常是首选,尤其是在囊壁破裂后,因为内部阻力丧失会使周围组织更容易位移和损伤。
经迷路入路可早期可视化并恒定地到达面神经的脑池段和内听道段,这是乙状窦后入路可能无法做到的,尤其对于位于前方的囊肿或与脑干广泛粘连的病例。尽管早期囊肿减压可改善暴露,但肿瘤塌陷和变形的可能性更大。由于减压后关键解剖标志会发生移位,分离应暂停,直至重新建立方向感。严重的粘连可能需要在术中改变分离轨迹,以避免危及功能。从肿瘤的不同象限接近可显著降低风险。在粘连无法分离的病例中,追求全切可能带来不可接受的神经功能风险,此时选择最大安全切除并辅以密切的术后影像学随访,是优先考虑安全和功能的优选方案。资深作者常通过稳定神经的同时,从内向外沿神经平面剥离肿瘤,从神经上提起肿瘤包膜。
由于内听道口粘连十分紧密,故对这类肿瘤宜从内听道内开始沿由外向内的方向作分离操作,由此最大限度地清除肿瘤而尽可能保护功能。肌电图反馈及术中神经监测可直接、可靠地提供分离时的神经活动数据,因此有利于早期识别面神经,尤其是囊肿塌陷之后。更重要的是,囊肿减压后空间关系改变,此时用更高电压刺激更有利于识别移位的面神经。影像学特征绝非绝对可靠。术中所见的粘连程度及解剖平面缺失均需及时调整。
囊性听神经瘤与较高的术后出血率相关,这可能是由于其脆弱的肿瘤血管和容易再积聚血液或液体的倾向。术后监测脑脊液通路梗阻和脑积水,并在止血和早期影像检查中格外警惕,有助于在临床恶化前发现并发症。
患者须知
在 实性听神经瘤 中,达到House-Brackmann I-II级面神经功能的比率为80-90%,而在 囊性听神经瘤 中,该比率约为60-70%,特别是在需要进行最大安全切除或涉及较大、粘连性囊肿的病例中。即使有专业的监测和精细的技术,仍可能出现暂时性或永久性的面部肌力减弱。由于本病需要个体化的手术策略,而术中为保护功能有时要偏离原定计划,因此从安全角度出发,术中宜优先选择最大安全切除而非大体全切。最大安全切除之后定期行MRI监测小范围残留肿瘤,其复发风险极低。又因为囊性肿瘤壁薄质脆,且常邻近脑脊液通路,故其术后并发症风险较实性肿瘤更高。因此患者应充分了解头痛、恶心、意识模糊诸种警告征象。

