刷新纪录!礼来70亿美元天价收购in vivo CAR-T公司Kelonia


撰文丨王聪
编辑丨王多鱼
排版丨水成文
2026 年 4 月 20 日,国际制药巨头礼来公司(Eli Lilly)与 in vivo CAR-T 细胞疗法开发公司 Kelonia Therapeutics 宣布达成最终协议,礼来公司将收购 Kelonia。


Kelonia 公司开发了一种专有的体内基因定位系统(in vivo gene placement system,iGPS®),该系统使用经过包膜修饰的慢病毒载体,以提高体内基因递送效率,并使用趋向分子来促进组织特异性递送,从而高效且有选择性地进入体内 T 细胞,使患者自身能够生成 CAR-T 细胞疗法,从而治疗潜在疾病。Kelonia 的主推项目 KLN-1010 是一种研究性的一次性静脉基因疗法,可生成 BCMA 靶向的 CAR-T 细胞,靶向多发性骨髓瘤细胞表面表达的 BCMA 蛋白。在 2025 年美国血液学会年会的全体会议上,公布了令人鼓舞的早期临床结果,提供了初步的临床验证,并显示出良好的耐受性。
首批接受治疗的四名多发性骨髓瘤患者的结果显示:
四名患者均达到 100%的微小残留病(MRD)阴性反应率;随访时间最长的两名患者在三个月内均保持了 MRD 阴性反应。
无需进行淋巴细胞清除化疗,而体内产生的 CAR-T 细胞的扩增情况与体外 CAR-T 细胞疗法相似,达到循环 T 细胞的 85%。
所有四名患者在三个月的随访期内均观察到持续的 CAR-T 记忆细胞。
毒性特征良好,未出现 3 级及以上的细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)或迟发性神经毒性,且细胞减少症明显少于体外 CAR-T 细胞疗法。
四名患者中有三名接受了 2×107 国际单位/千克体重的治疗剂量。深度反应和良好的安全性促使进一步探索治疗窗口以降低生产成本。第四名患者接受了较低剂量的 6×106 国际单位/千克体重的治疗剂量,并在一个月时达到了 MRD 阴性反应。
根据国际骨髓瘤工作组(IMWG)的标准,所有四名患者均保持缓解状态,最长随访时间为五个月;完全缓解(CR)是最佳总体反应。
这些记过表明,KLN-1010 有望成为多发性骨髓瘤治疗的变革性进展,因为它避免了复杂、耗时且昂贵的体外 CAR-T 细胞的生产制造流程,且无需对患者进行预给药化疗。
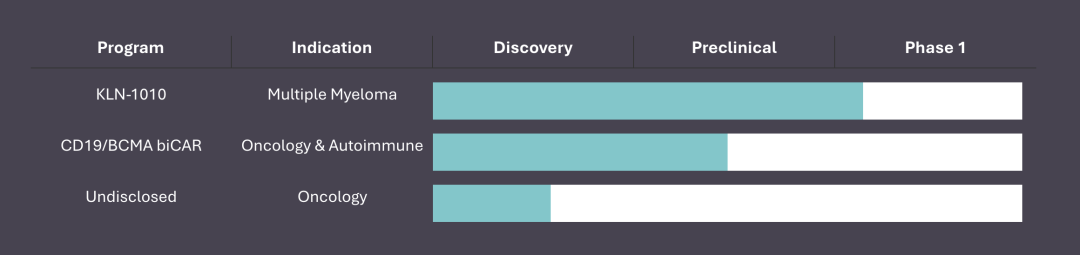
Kelonia公司的研发管线
礼来公司执行副总裁 Jacob Van Naarden 表示,自体 CAR-T 疗法已显著改善了多种癌症患者的治疗效果,但其生产、安全性和可及性方面存在的重大障碍意味着,实际上只有少数符合条件的患者能够接受这种疗法。而 Kelonia 的体内平台有可能改变这一现状,以一种更简单、即用即取的形式实现快速且持久的疗效。KLN-1010 的早期临床数据非常令人鼓舞,这既为多发性骨髓瘤患者带来了潜在的治疗进展,也证明了其体内平台的概念。我们期待与 Kelonia 团队合作,迅速推进 KLN-1010 的研发,以满足患者需求,并在其他可能受益的疾病领域充分发掘其平台的潜力。
Kelonia 公司 CEO Kevin Friedman 博士表示,Kelonia 在推进体内细胞疗法的巨大潜力方面处于领先地位,其影响力和覆盖范围已超越了个性化医疗的传统界限。我们已证明,与体外 CAR-T 细胞疗法相比,我们的体内 iGPS 平台能够以显著降低的复杂性和成本实现多发性骨髓瘤的深度缓解。结合礼来公司的优势,我们的体内 iGPS 平台有望将细胞疗法的应用范围从当前的血液恶性肿瘤领域拓展开来,并在更广泛的癌症及其他严重疾病治疗领域带来变革。
根据协议条款,礼来公司(Eli Lilly)将收购 Kelonia Therapeutics,Kelonia 的股东们将获得总计高达 70 亿美元的现金,其中包括 32.5 亿美元的预付款,以及在达成某些临床、监管和商业里程碑时的后续付款。该交易须满足惯常的交割条件,包括惯常的监管审批,预计将于 2026 年下半年完成。
参考资料:
https://keloniatx.com/lilly-to-acquire-kelonia-therapeutics-to-advance-in-vivo-car-t-cell-therapies/




点在看,传递你的品味




