4例患者,70亿美金!礼来这把赌大了


近日,礼来再次震惊了医药界。在距上一次出手仅两个月后,这家凭减重药替尔泊肽赚得盆满钵满的制药巨头,将以32.5亿美元首付款、最高70亿美元的“天价”,将体内CAR-T公司Kelonia Therapeutics收入囊中,同时刷新该领域的最高收购记录。加上今年2月以最高24亿美元收购的Orna Therapeutics,礼来仅在体内CAR-T这一条赛道上就已砸下近百亿美元。



70亿买的是什么?

过去几年,礼来一直在“买买买”,收购标的覆盖肿瘤、眼科、减重、免疫及神经等领域,收购规模合计超过300亿美元。而这次,礼来为什么愿意为一个尚未有产品上市、核心管线仅处于I期临床阶段的公司掏出70亿美元?

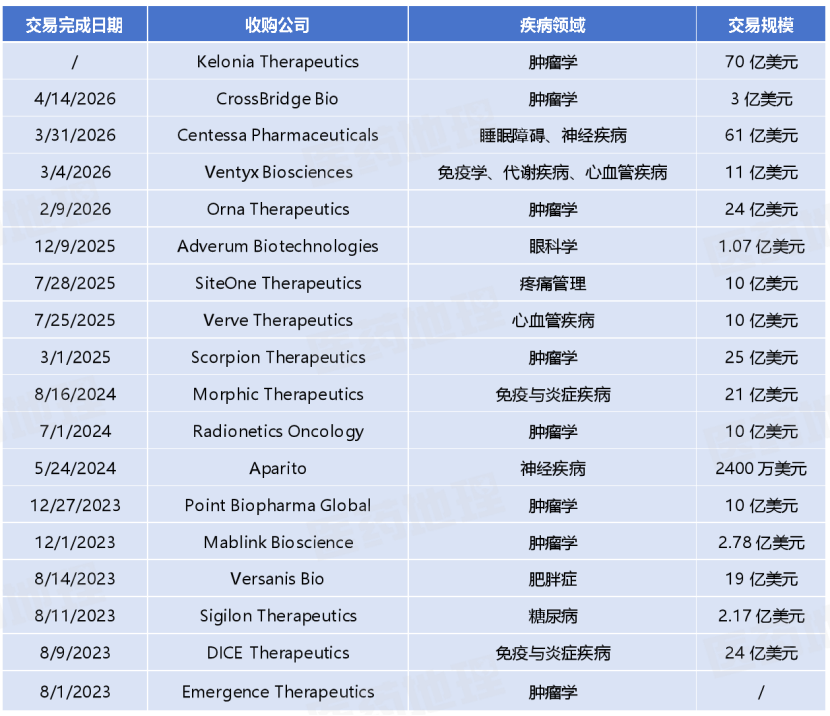
近年礼来收购事件
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
Kelonia开发了一套专有的体内基因定位系统(iGPS),利用经特殊改造的慢病毒颗粒,在体内高效、精准地进入T细胞,使患者自身能够在体内生成CAR-T,从而治疗潜在疾病。其核心管线KLN-1010是一款在研的一次性静脉输注基因疗法,能够在体内生成靶向多发性骨髓瘤细胞表面BCMA蛋白的抗BCMA CAR-T细胞。
2025年ASH年会上,Kelonia展示了KLN-1010的首批人体数据:四例复发/难治性多发性骨髓瘤患者,在接受单次KLN-1010输注后,全部实现了微小残留病(MRD)阴性缓解,最长随访已达五个月。早期数据验证了疗法的临床可行性,并显示出良好的耐受性前景。
KLN-1010不仅省去了体外制备患者特异性细胞疗法的繁琐流程,也免去了给药前的清淋化疗,有望成为多发性骨髓瘤治疗领域的变革性突破。去年7月,Kelonia在澳大利亚启动了KLN-1010复发/难治性多发性骨髓瘤的I期临床试验。今年1月,FDA批准了KLN-1010的IND申请。

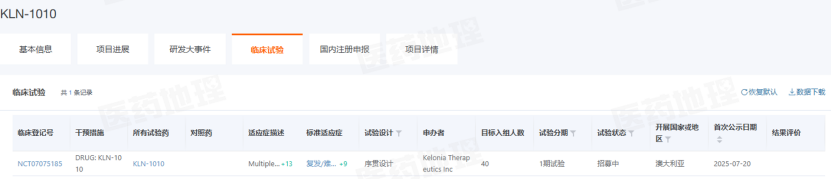
KLN-1010临床试验进展
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
在自体CAR-T疗法领域中,强生与传奇合作的Carvykti在多发性骨髓瘤中表现惊艳,吉利德旗下Yescarta在淋巴瘤领域也已站稳脚跟。然而,真正能用上这些疗法的患者,只是冰山一角。
问题出在哪?自体CAR-T需要先采集患者T细胞,运往中央化工厂进行基因改造和体外扩增,再回输体内。整个过程动辄数周,期间患者还需接受清淋化疗。单次治疗成本数十万美元,只有少数顶尖医疗中心能够承接。礼来肿瘤事业部总裁Jacob Van Naarden提到:“生产、安全性和可及性方面的重重壁垒,使得符合条件的患者中仅有一小部分真正用上了这类疗法。”
然而体内CAR-T的颠覆性在于,它不再把T细胞取出来“实验室改造”,而是将携带CAR基因的载体直接注入患者体内,让T细胞“原地转化”。省去了采集、培养、运输、回输的全链条——从“个体化定制”变为“现货型给药”。理论上成本更低、等待更短、可及性更高。
体内CAR-T赛道“群雄逐鹿”
当然,礼来并不是唯一一个看到体内CAR-T潜力的玩家。
过去一年间,这条赛道上的交易密度令人咋舌。阿斯利康以10亿美元收购EsoBiotec,其ESO-T01同样以BCMA为靶点,在I期临床中五分之四的患者实现客观缓解,其中三例达到严格意义上的完全缓解。不过,ESO-T01的数据中也出现了致死性不良事件——一名患者因脊髓压迫于治疗后19天死亡,这也为体内CAR-T的安全性敲响了警钟。
吉利德旗下Kite以3.5亿美元买下Interius BioTherapeutics,并与Pregene签署了价值高达16亿美元的合作协议。艾伯维21亿美元收购了专注自身免疫疾病的Capstan Therapeutics。BMS 15亿美元收入Orbital Therapeutics。强生则选择了另一条路径——去年11月与Kelonia达成合作,而非直接收购。
全球范围内,已有超过40项体内CAR-T进入临床阶段,适应症从血液肿瘤扩展到实体瘤和自身免疫病。各家采用的技术路径也各有千秋——慢病毒载体、LNP脂质纳米颗粒、外泌体载体等。不同平台之间的差异化竞争才刚刚开始。
为什么几乎所有MNC都在跑步进场?对于自体CAR-T而言,细胞的采集、运输、改造、扩增、质控、回输,每一步都需要复杂的中央化工厂和精密供应链。疗效虽好,但商业模式天然受制于产能上限。而体内CAR-T则是一个经过严格设计的基因载体,可以像化学药那样大规模生产、标准化质控、直接给药。边际成本更低,规模效应更显著,市场渗透潜力更大。
从产业逻辑看,体内CAR-T将CAR-T从一个“服务”(细胞定制加工)变成了一个“产品”。对于大型药企而言,“产品”比“服务”更好管理、更容易规模化、更符合既有的商业体系。大佬们纷纷入场,不是因为突然对细胞治疗产生兴趣,而是看到了细胞治疗“产品化”的可能性。
体内CAR-T用慢病毒载体在体内直接“升级”T细胞,省去体外制造的繁琐链条,在科学逻辑上是完全走得通的;早期临床数据也确实亮眼,KLN-1010四例患者全部MRD阴性且安全性可控,给了行业极大的想象空间。但四例样本、数月随访,远不足以宣告胜利;长期插入突变风险、免疫原性对重复给药的限制、以及实体瘤领域的空白,仍是悬在头顶的三把剑。所以它既不是空中楼阁,也绝非板上钉钉,而是正处于“概念验证初步成立、亟待大样本长周期数据检验”的关键爬坡期,离真正“靠谱”还差一场硬仗。
对于手握替尔泊肽庞大现金流的礼来而言,如果赌赢了,得到的不仅是一款药,更是一个能批量生产CAR-T的“操作系统”。



