外周T细胞淋巴瘤治疗格局重塑:维布妥昔单抗引领一线新标准,靶向药物开辟复发难治新路径
发布时间:2026-04-21来源:药事纵横
外周T细胞淋巴瘤(PTCL)是一组起源于成熟T细胞和自然杀伤细胞的非霍奇金淋巴瘤。作为一种具有高度异质性的血液系统恶性肿瘤,该疾病在临床特征、病理亚型及分子生物学行为上表现出极大的复杂性。流行病学数据表明,PTCL的发病率存在显著的地域差异。在亚洲国家尤其是中国,该疾病占非霍奇金淋巴瘤的比例高达25%-30%,远高于西方国家的10%-15%。这种高发病率与复杂的亚型分类使得该疾病的治疗成为临床实践中的一大挑战。传统化疗方案在过去几十年中一直是PTCL的基础治疗手段,但其总体疗效存在明显的局限性。不同病理亚型之间的生存获益差异巨大,除间变性淋巴瘤激酶阳性间变性大细胞淋巴瘤外,绝大多数亚型患者的长期生存率低于50%。近年来,随着分子病理学、肿瘤微环境学以及免疫学的飞速发展,靶向治疗、免疫治疗及新型联合治疗策略不断涌现,彻底改变了这一难治性疾病的临床格局。本文基于近期PTCL治疗领域的核心研究数据,系统梳理从一线治疗到复发难治性治疗的全链条进展,以期为临床实践提供科学客观的参考。一、一线治疗的传统局限与标准方案优化
PTCL的一线治疗长期依赖以蒽环类药物为基础的传统化疗方案。临床最常用的方案包括环磷酰胺联合多柔比星、长春新碱和泼尼松的CHOP方案,在此基础上加用依托泊苷的CHOEP方案,以及剂量调整的EPOCH方案和高剂量Hyper-CVAD方案。这些方案在不同亚型中的表现差异显著。以CHOP方案为例,其在间变性淋巴瘤激酶阳性间变性大细胞淋巴瘤患者中的五年总生存率可达70%-88%,但在除外该亚型的其他PTCL中,五年总生存率普遍不足50%。Hyper-CVAD方案同样呈现出类似趋势,虽然能使间变性淋巴瘤激酶阳性患者获得极高的三年生存率,但排除该亚组后生存率大幅下降。由于传统化疗难以满足绝大多数患者的长期生存需求,临床研究开始将重心转向靶向药物与传统化疗的联合。二、CD30抗体偶联药物联合化疗的确立与扩展
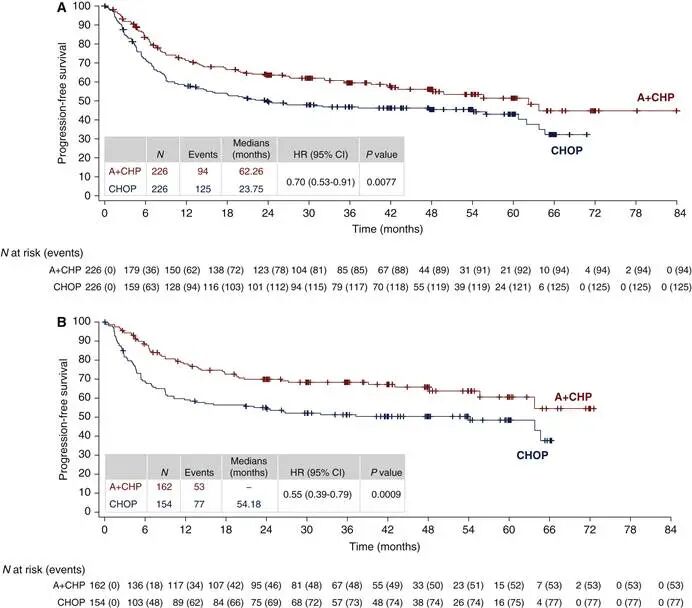
CD30在间变性大细胞淋巴瘤中呈现特异性高表达,同时在PTCL非特指型、血管免疫母细胞性T细胞淋巴瘤等亚型中也有不同程度表达。维布妥昔单抗作为一种靶向CD30的抗体药物偶联物,能够通过阻滞细胞周期并诱导肿瘤细胞凋亡发挥强效抗肿瘤作用。具有里程碑意义的ECHELON-2 III期随机对照试验比较了维布妥昔单抗联合环磷酰胺、多柔比星和泼尼松的BV-CHP方案与传统CHOP方案在CD30阳性PTCL一线治疗中的疗效。该研究入组患者中间变性大细胞淋巴瘤占70%。结果显示,BV-CHP方案在不增加总体毒性的前提下显著改善了患者生存。BV-CHP组的五年无进展生存率达到51.4%,五年总生存率达到70.1%,完全缓解率达到68%,各项指标均显著优于CHOP组。值得注意的是,BV-CHP组外周神经病变的发生率反而低于CHOP组,且因不良事件导致的停药率更低。基于这一坚实证据,BV-CHP已被确立为间变性大细胞淋巴瘤及其他CD30表达阳性T细胞淋巴瘤的标准一线治疗方案。图1. ECHELON-2临床研究无进展生存期结果在此基础上,临床学者进一步探索了维布妥昔单抗与其他化疗方案的强化联合。一项II期临床研究评估了CHOEP联合维布妥昔单抗序贯维布妥昔单抗巩固治疗在非间变性大细胞淋巴瘤患者中的疗效,结果显示客观缓解率高达91%,完全缓解率达到79%,且未发生治疗相关死亡。中国开展的真实世界研究将维布妥昔单抗联合环磷酰胺、依托泊苷和泼尼松的BV-CEP方案应用于初治患者,涵盖间变性大细胞淋巴瘤、滤泡辅助T细胞淋巴瘤及血管免疫母细胞性T细胞淋巴瘤。结果表明总体客观缓解率为89.5%,完全缓解率为52.7%,其中间变性大细胞淋巴瘤和血管免疫母细胞性T细胞淋巴瘤亚组的完全缓解率分别达到100%和75%。与历史对照的CHOEP方案相比,BV-CEP方案显著延长了无进展生存期,且安全性良好,无患者因不良事件中断治疗或死亡。三、CHOP联合新型药物的多元化探索
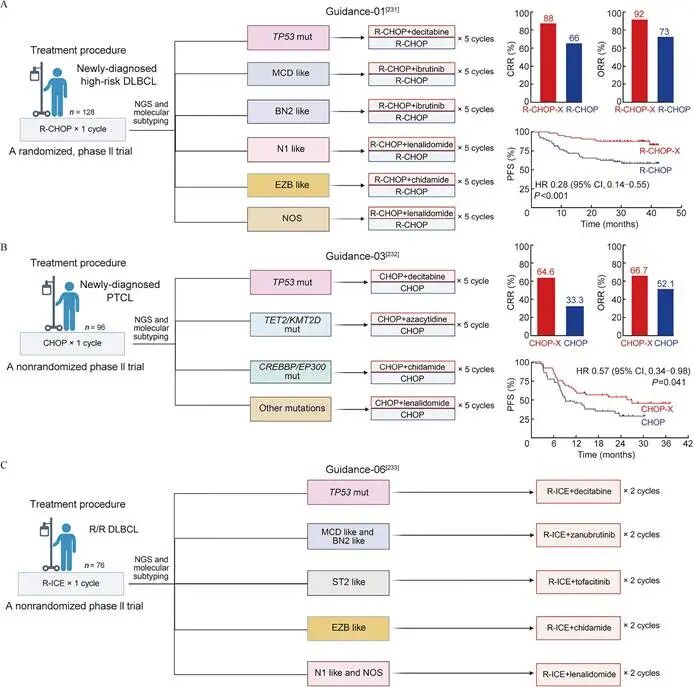
在维布妥昔单抗获批之前,CHOEP是唯一被广泛认可的CHOP联合其他药物的方案。研究表明,对于年龄小于60岁且乳酸脱氢酶正常的患者,CHOEP可改善无事件生存期,但增加的化疗毒性使老年患者难以耐受。为寻找更高效低毒的联合策略,CHOP联合X方案的研究全面铺开。表观遗传药物是CHOP-X探索中的重要分支。组蛋白去乙酰化酶抑制剂如罗米地辛、贝利司他和西达本胺以及DNA甲基转移酶抑制剂如阿扎胞苷被陆续引入一线治疗。一项评估罗米地辛联合CHOP的III期研究未能改善总体人群的生存结局且增加了毒性,但事后分析发现在滤泡辅助T细胞淋巴瘤亚组中,中位无进展生存期显著延长。我国原研的西达本胺联合CHOP方案在最新SWIFT II期研究中针对初治滤泡辅助T细胞淋巴瘤患者展现出极高活性,客观缓解率达到85.7%,完全缓解率达到71.4%,且不良反应多为可逆可控。在DNA甲基转移酶抑制剂方面,阿扎胞苷联合CHOP的小型II期研究在滤泡辅助T细胞淋巴瘤亚组中取得了88.2%的完全缓解率,两年无进展生存率达到69.2%,显示出表观遗传调控在该亚型中的特殊价值。基于分子标志物的精准化疗代表了未来的发展方向。中国的GUIDANCE-03 II期研究根据不同基因突变匹配不同靶向药物联合CHOP。携带TET2或KMT2D突变的患者联合阿扎胞苷,TP53突变患者联合地西他滨,CREBBP或EP300突变患者联合西达本胺,无特定突变患者联合来那度胺。这种分子标志物驱动的个体化治疗方案使得实验组的完全缓解率提升至64.6%,中位无进展生存期延长至25.5个月,远超传统CHOP组的九个月。该研究不仅证实了CHOP-X的临床优势,更验证了精准医学在PTCL一线治疗中的可行性。其他联合方案也在不断尝试。免疫调节剂来那度胺联合CHOP在老年初治血管免疫母细胞性T细胞淋巴瘤患者中的完全代谢缓解率仅为41%,未能达到预期标准,且血液学毒性导致部分患者中断治疗。人源化CCR4单克隆抗体莫格利珠单抗联合CHOP在日本老年侵袭性成人T细胞白血病患者中取得了64.6%的完全缓解率,为不适合移植的CCR4阳性患者提供了新选择。此外,PI3Kδ抑制剂林普利塞联合CHOP的LINCH研究初步数据显示客观缓解率达80%,完全缓解率达46.7%,展现出一联合方案的早期潜力。四、间变性淋巴瘤激酶抑制剂与去化疗方案的尝试
针对间变性淋巴瘤激酶阳性的特殊亚型,小分子酪氨酸激酶抑制剂克唑替尼被尝试与儿科标准方案联合用于儿童患者一线治疗。然而随访数据显示其两年无事件生存率为76.8%,且血栓栓塞事件发生率较高引起临床担忧。相比之下,维布妥昔单抗联合化疗方案在儿童患者中表现出更优的两年无事件生存率和总生存率,且未增加毒性,提示在儿童间变性淋巴瘤激酶阳性间变性大细胞淋巴瘤中,抗体偶联药物联合化疗可能比激酶抑制剂联合化疗更具优势。连续监测特定融合基因转录水平和抗ALK抗体滴度被证实对该亚型的治疗指导及预后评估具有重要价值。对于不适合接受高强度化疗的老年或体能状态较差的患者,去化疗方案成为重要探索方向。一项多中心II期研究采用罗米地辛联合来那度胺治疗不适合化疗的初治PTCL患者。结果显示客观缓解率为65.2%,完全缓解率为26.1%。达到完全缓解的患者中位缓解持续时间长达27.1个月,两年无进展生存率和总生存率分别为31.5%和49.5%。该方案的安全性特征与既往单药报道一致,为脆弱人群提供了一种有效的初始治疗替代选择。五、巩固治疗与缓解后维持治疗的新策略
由于单纯化疗效果欠佳,造血干细胞移植在提高PTCL生存率和降低复发率方面扮演着关键角色。自体造血干细胞移植在一线治疗中的价值虽存在争议,但多项大规模回顾性分析支持其特定获益。多中心研究显示,对于化疗后达到首次完全缓解的患者,接受自体造血干细胞移植可显著改善五年无进展生存率和总生存率,III-IV期患者获益尤为明显。国际前瞻性T细胞淋巴瘤项目的长期随访证实,接受自体造血干细胞移植患者的十年总生存率得到显著提升。欧洲血液与骨髓移植学会的回顾性分析指出,自体造血干细胞移植在首次或第二次完全缓解阶段进行预后更优,且一线移植的生存获益优于二线及三线。异基因造血干细胞移植的预后则主要取决于移植前的疾病状态,而与既往治疗线数或具体亚型无关。在完成一线诱导治疗达到完全缓解或部分缓解后,维持治疗的核心目标是延长缓解期并降低复发风险。近年来新型靶向药物在维持治疗领域的表现令人瞩目。高选择性JAK1抑制剂戈利昔替尼在JACKPOT26 II期研究中展现了卓越的维持治疗效果。入组的四十八例患者在接受戈利昔替尼维持治疗后,达到完全缓解的患者十二个月和二十四个月无病生存率分别高达82.1%和73.7%。更值得关注的是,38.9%的部分缓解患者在维持治疗后转化为完全缓解,中位无进展生存期达到17.4个月。该药物的不良事件以血液学毒性为主,且多数可逆可控,有望成为标准维持方案。图2.临床试验中基因亚型指导的联合治疗结果组蛋白去乙酰化酶抑制剂西达本胺在真实世界研究中同样表现出良好的维持活性。在维布妥昔单抗联合化疗诱导治疗后序贯西达本胺维持治疗的队列中,患者持续缓解,客观缓解率和完全缓解率分别维持在87.9%和75.8%。回顾性数据进一步表明,一线缓解后即使用西达本胺维持的患者,其中位无进展生存期和总生存期均显著优于在复发挽救治疗后才使用该药的患者。免疫调节剂来那度胺在缓解状态但不适合移植的患者中进行维持治疗,一年无进展生存率为49%,中位总生存期约34个月,为不适合移植的群体提供了延缓疾病进展的可能。六、复发难治性PTCL的靶向与免疫突破
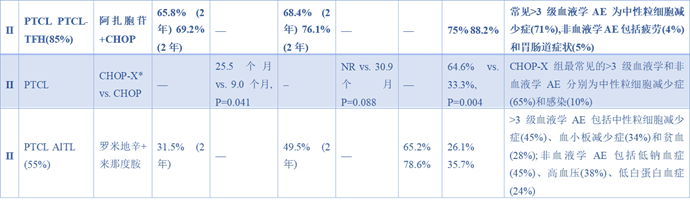
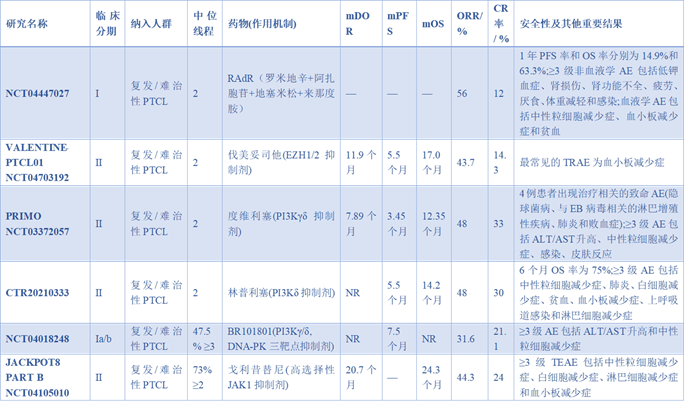
复发难治性PTCL的预后极差,异基因造血干细胞移植是目前唯一有望治愈的手段,且移植前达到完全缓解的患者预后最佳。对于计划进行自体造血干细胞移植的患者,二线治疗以快速获得完全缓解为目标。随着新药研发的加速,多种新型药物改变了挽救治疗的格局。表观遗传调控药物在复发难治性治疗中持续发力。一项I期临床研究采用罗米地辛联合阿扎胞苷、地塞米松和来那度胺的RAdR方案治疗复发难治性患者,客观缓解率达到56%,一年总生存率为61.3%,安全性可控,可作为桥接移植的优选方案。贝利司他在真实世界研究中的客观缓解率达到45%,证实了其作为挽救治疗选择的可行性。以伐美妥司他为代表的EZH1和EZH2抑制剂在VALENTINE-PTCL 01二期研究中展现出跨亚型的抗肿瘤活性,客观缓解率达43.7%,中位缓解持续时间达11.9个月,为患者提供了深度且持久的应答。PI3K信号通路在T细胞淋巴瘤中常发生异常激活,相关抑制剂成为研究热点。度维利塞在PRIMO二期研究中针对复发难治性PTCL表现出显著疗效,总体客观缓解率为48%,完全缓解率为33%,其中血管免疫母细胞性T细胞淋巴瘤亚型获益最为显著。基于此结果,评估度维利塞单药与标准化疗差异的三期TERZO研究正在推进。我国自主研发的PI3Kδ抑制剂林普利塞在国内外的二期临床研究中均显示出高度一致的抗肿瘤活性,总体客观缓解率约为48%,完全缓解率达30%-33%,且所有亚型均观察到缓解,患者耐受性良好。新型三靶点抑制剂BR101801通过同时抑制PI3Kγ、δ和DNA-PK,在一期临床试验中获得了31.6%的客观缓解率和21.1%的完全缓解率,中位无进展生存期达7.5个月。表2.复发/难治性PTCL新型靶向药物关键临床研究JAK/STAT通路的异常与PTCL的发生发展密切相关。戈利昔替尼在JACKPOT8全球多中心研究中作为单药用于复发难治性治疗,客观缓解率达44.3%,完全缓解率为24%,中位缓解持续时间长达20.7个月,中位总生存期达到24.3个月。所有纳入亚型均观察到超过40%的客观缓解率。该药物凭借深度缓解、全亚型获益和长期生存优势,确立了其在复发难治性治疗中的重要地位。在间变性淋巴瘤激酶阳性复发难治性间变性大细胞淋巴瘤中,克唑替尼的真实世界数据显示其完全缓解率高达92%。第二代ALK/ROS1抑制剂劳拉替尼在克服克唑替尼耐药突变方面表现出显著疗效,长期随访数据显示其在中枢神经系统受累的患者中同样安全有效,五年的随访数据证实了其长期疗效的稳定性。七、免疫治疗与细胞治疗的创新与前景
免疫调节剂与单克隆抗体在复发难治性治疗中持续进行单药及联合探索。维布妥昔单抗联合减低剂量的来那度胺在复发难治性PTCL中取得了50%的客观缓解率,且联合毒性未显著增加。莫格利珠单抗的日本真实世界监测数据显示其在复发难治性亚组中的客观缓解率为47.6%。针对KIR3DL2靶点开发的拉可妥单抗正在一期临床试验中进行评估,该靶点在约一半的PTCL患者中表达,有望成为新的治疗突破口。双特异性和三特异性衔接器代表了抗体工程的最新进展。AFM13是一种新型的CD30和CD16A双特异性天然细胞衔接器,能够同时结合肿瘤细胞表面的CD30和自然杀伤细胞表面的CD16A,从而特异性招募自然杀伤细胞杀伤淋巴瘤细胞。其在二期研究中获得了32.4%的客观缓解率,部分完全缓解患者获得了长期生存。目前联合脐血来源自然杀伤细胞的LuminICE研究正在推进中。三特异性衔接器SAR442257可同时靶向肿瘤细胞上的CD38及T细胞上的CD3和CD28,临床前研究证实了其靶向杀伤与免疫激活的双重作用。免疫检查点抑制剂在PTCL中的表现存在显著的亚型差异。帕博利珠单抗单药治疗的临床获益有限,仅在EB病毒阳性患者中显示出一定潜力。联合策略正在成为突破方向,帕博利珠单抗联合组蛋白去乙酰化酶抑制剂以及纳武利尤单抗联合维布妥昔单抗的方案均在临床探索中。CheckMate 436研究数据显示,纳武利尤单抗联合维布妥昔单抗在复发难治性患者中的客观缓解率为45.5%,完全缓解率为33.3%,为免疫联合靶向策略提供了循证依据。嵌合抗原受体T细胞疗法在T细胞淋巴瘤中面临难以区分恶性与正常T细胞的特殊难题。AUTO4作为首个靶向T细胞受体β链恒定域1的CAR-T疗法,通过选择性清除TRBC1阳性肿瘤细胞同时保留TRBC2阳性正常T细胞实现了精准治疗。其一期和二期临床研究显示出良好的安全性且无剂量限制性毒性,高剂量组的客观缓解率达到66.7%。此外,靶向CD7和CD70的CAR-T疗法也在一期研究中展现出初步疗效,极大丰富了细胞治疗的武器库。在传统药物方面,新型蒽环类药物脂质体制剂盐酸米托蒽醌脂质体已在国内获批用于复发难治性PTCL,其关键二期研究数据显示单药客观缓解率为46.3%,中位总生存期达到23.3个月,为临床提供了可靠的传统药物升级选择八、结语
总的来说,PTCL的治疗领域正处于一场深刻的变革之中。从传统化疗的单一模式,发展到如今涵盖小分子靶向药物、抗体偶联药物、表观遗传调控药物、免疫检查点抑制剂以及基因工程细胞疗法的多元化格局,临床医生拥有了前所未有的治疗手段。一线治疗中维布妥昔单抗联合化疗标准的建立以及基于分子标志物的CHOP-X精准策略,显著提高了初治患者的缓解深度。维持治疗中JAK抑制剂和表观遗传药物的应用,有效填补了诱导治疗与复发之间的空白,延长了患者的高质量生存期。在复发难治性领域,PI3K抑制剂、JAK抑制剂及新型CAR-T疗法的涌现,为过去缺乏有效挽救方案的患者带来了重获新生的希望。尽管取得了显著突破,PTCL的长期生存率仍有待进一步提升。肿瘤异质性导致的耐药性、创新疗法带来的新型毒性以及高昂治疗成本带来的可及性问题,是当前面临的核心挑战。未来的研究将更加依赖于多组学技术对疾病生物学本质的深度解析,通过发现更多预测性生物标志物来实现真正的个体化精准用药。同时,新型药物之间的合理排兵布阵及联合方案的优化,以及多学科协作诊疗模式的常态化,将是提升整体治愈率的关键推力。随着基础医学研究与临床转化的持续共振,PTCL的治疗必将迈向更深层次的精准化与规范化,广大患者将迎来更具希望的生存获益与更优的生活质量。1. Horwitz S, O'Connor OA, Pro B, et al. The ECHELON-2 Trial: 5-year results of a randomized, phase III study of brentuximab vedotin with chemotherapy for CD30-positive peripheral T-cell lymphoma. Ann Oncol. 2022 Mar;33(3):288-298. doi: 10.1016/j.annonc.2021.12.002.2. Ogura M, Kim WS, Uchida T, et al. Phase I studies of darinaparsin in patients with relapsed or refractory peripheral T-cell lymphoma: a pooled analysis of two phase I studies conducted in Japan and Korea. Jpn J Clin Oncol. 2021 Feb 8;51(2):218-227. doi: 10.1093/jjco/hyaa177.3. Wang S, Qiu Y, Zhao W. Targeting signaling pathways in lymphoma: From molecular mechanisms to clinical breakthroughs. Chin Med J (Engl). 2026 Apr 5;139(7):949-972. doi: 10.1097/CM9.0000000000004017.作者:栗雅,主要从事药物质量控制与分析检测等方面工作。
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。