全球第二款BTK PROTAC启动III期临床
4月7日,美国临床试验收录网站显示,
Nurix Therapeutics启动了
Bexobrutideg
(
NX-5948)的首个III期临床试验。

该研究是一项随机、多中心、开放标签III期临床试验(n=620),旨在评估
Bexobrutideg(口服,每日1次)
对比
Pirtobrutinib
(口服,每日1次)
治疗既往接受过共价BTK抑制剂治疗的复发或难治性慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)患者的有效性和安全性。研究的主要终点是无进展生存期(PFS)。
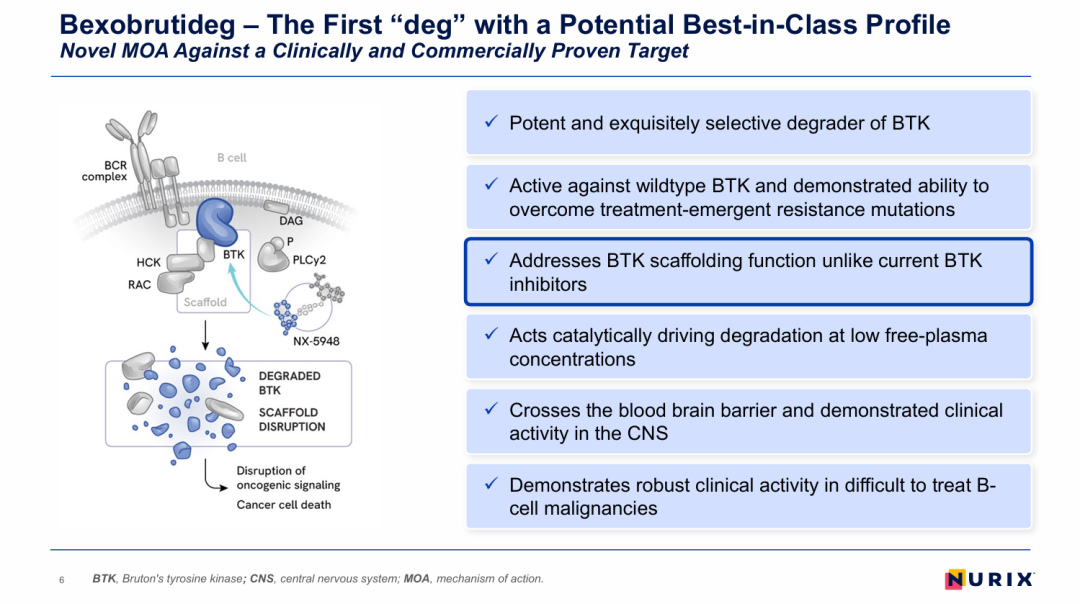
Bexobrutideg是Nurix Therapeutics自主研发的一款可口服且可透脑的高选择性BTK降解剂。该药物是继
Catadegbrutinib
后第二款进入III期阶段的
BTK PROTAC
药物。
Pirtobrutinib(匹妥布替尼)是礼来开发的一款非共价BTK C481S抑制剂,于2023年1月首次获批上市。截至目前,Pirtobrutinib已获批两项适应症,包括:1)既往接受过至少两线系统治疗(包括BTK抑制剂)的复发或难治性套细胞淋巴瘤(
MCL
)成人患者;2)既往接受过共价BTK抑制剂治疗的复发或难治性CLL/SLL成人患者。
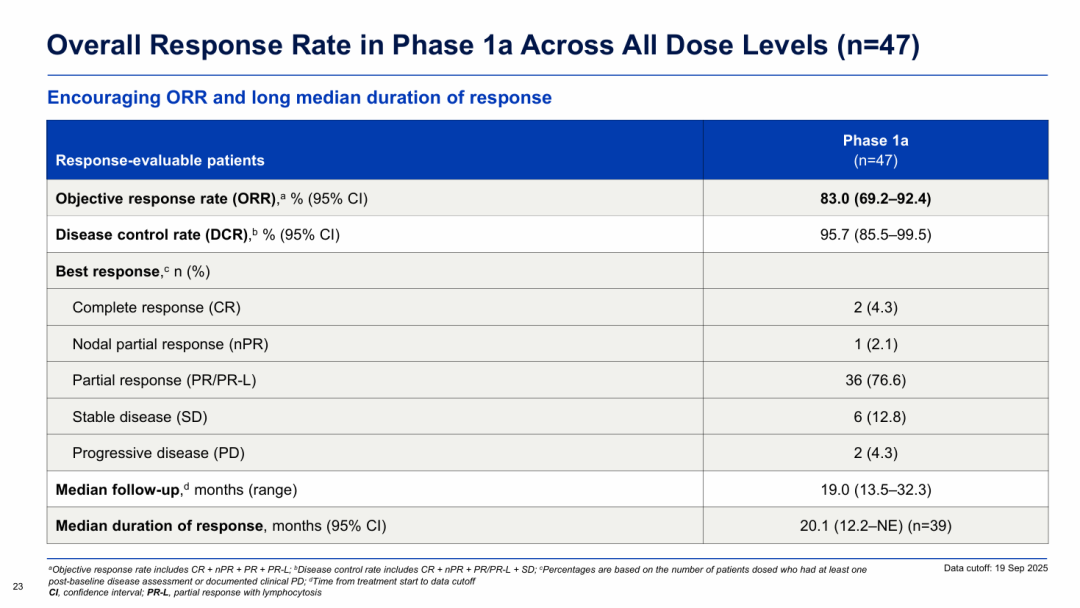
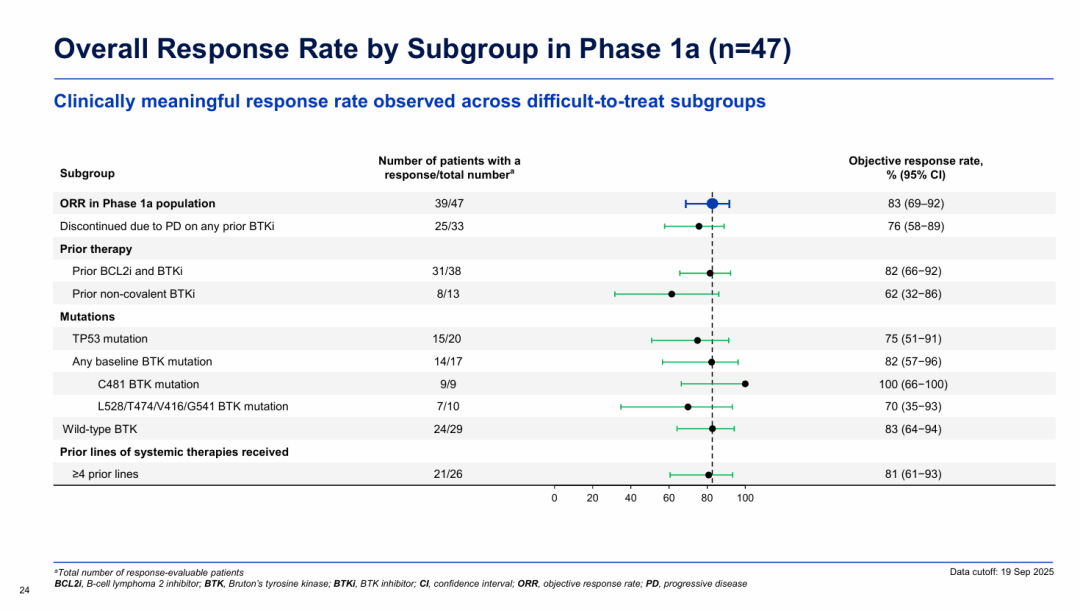
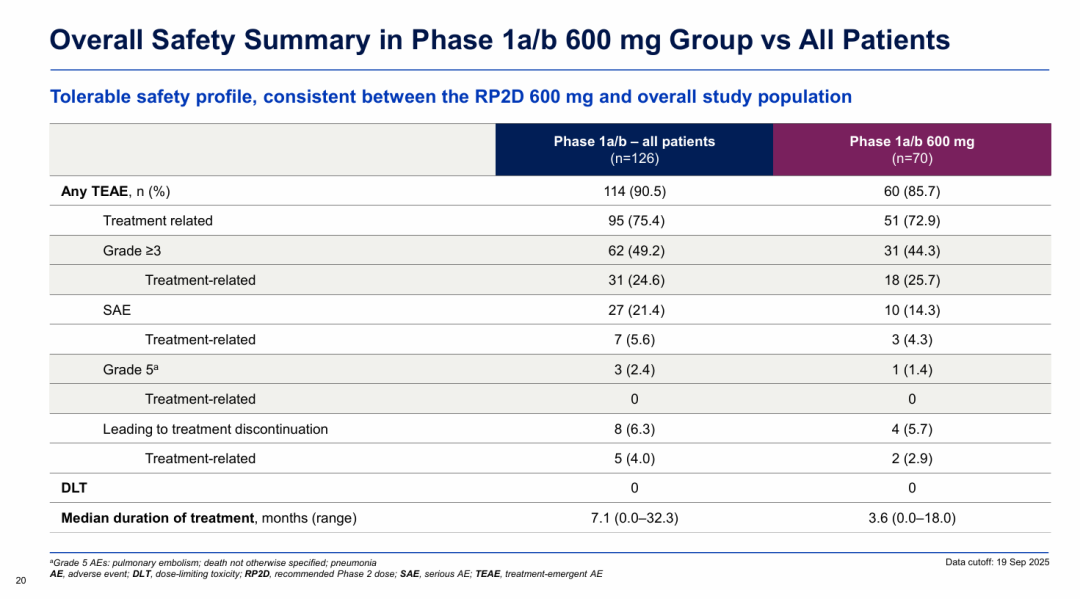
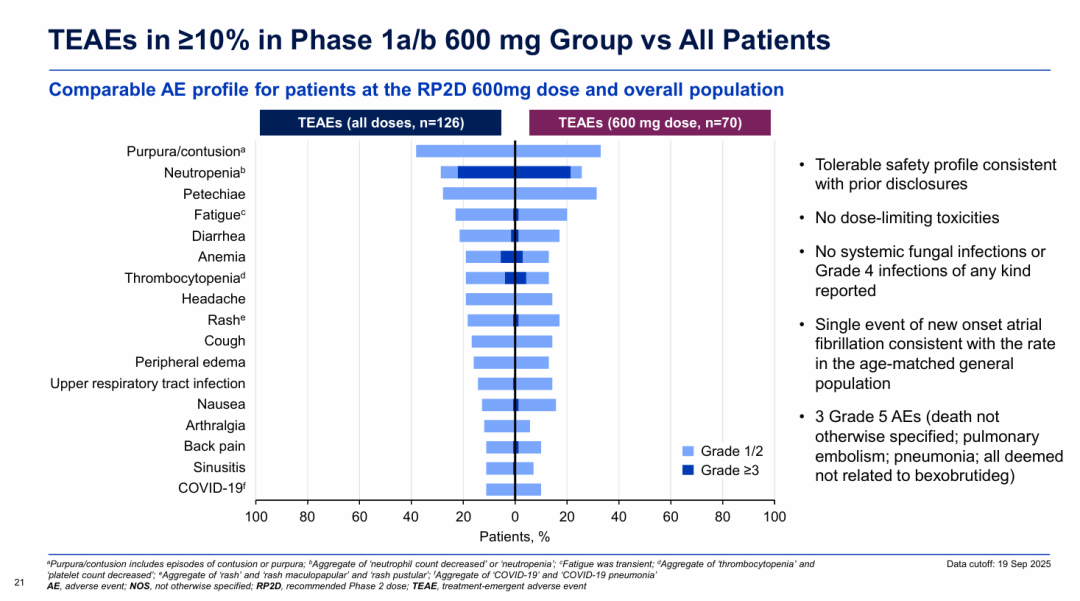
Ia期NX-5948-301研究结果显示,重度经治CLL/SLL患者接受Bexobrutideg(50-600mg)治疗后,客观缓解率(ORR)达到83%(39/47),其中2例患者实现完全缓解(CR),疾病控制率(DCR)为95.7%(45/47);中位PFS达到22.1个月,中位缓解持续时间(DOR)达到20.1个月。
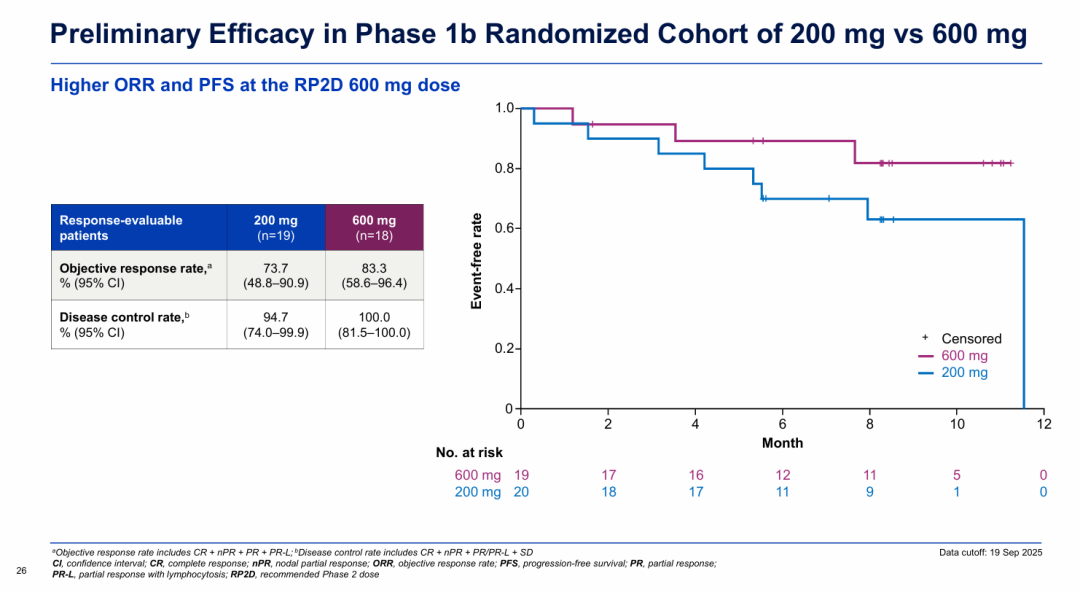
Ib期NX-5948-301研究结果显示,200mg剂量组和
600mg剂量组
重度经治CLL/SLL患者的ORR分别为73.7%和83.3%。
据医药魔方Nextpharma数据库统计,全球临床在研BTK PROTAC药物仅10款,包括
Catadegbrutinib
(百济神州)、Zelebrudomide(Nurix Therapeutics)、HSK29116(海思科)、APG-3288(亚盛医药)、ABBV-101(艾伯维)、Bexobrutideg(Nurix Therapeutics)、HZ-Q1070(和正医药)、UBX-303(Ubix Therapeutics)、TQB3019(正大天晴)和AC0676(Accutar Biotechnology)。
