Science:线粒体功能对树突状细胞的抗肿瘤能力至关重要
在所有免疫细胞中,
树突状细胞
独特的外形最容易给人留下深刻的印象。
作为人体免疫系统的重要组成部分,树突状细胞主要是通过呈递抗原,启动并激活人体免疫反应。不难看出,它是决定癌症免疫治疗成败的关键细胞类型。
在营养物质匮乏的肿瘤微环境中,树突状细胞也面临严峻的代谢压力,这会导致它的功能下降。不过,瘤内树突状细胞的代谢变化如何影响它的抗肿瘤作用,科学家还知之甚少。
今天,由
美国圣裘德儿童研究医院迟洪波
领衔的研究团队,在
Science
杂志上发表了一篇重要研究论文[1],它在一定程度上甚至
改写了我们对瘤内树突状细胞代谢的认知。
他们发现,
肿瘤里面的常规1型树突状细胞(cDC1)存在不同的线粒体状态,只有拥有高线粒体膜电位的cDC1亚型具有较强的抗原提呈能力,能有效激活CD8阳性T细胞。要知道,过往的体外研究表明,线粒体氧化磷酸化对于树突状细胞的成熟并非必需。
他们还发现,
线粒体融合蛋白OPA1通过维持线粒体氧化磷酸化,防止cDC1因能量不足而降解关键的抗原呈递MHC-I蛋白
。遗憾的是,随着肿瘤生长,cDC1的线粒体健康状况会逐渐恶化,导致抗肿瘤功能受损。不过,
通过代谢重编程或注射具有健康线粒体的cDC1,就可以显著提升免疫检查点抑制剂的疗效。

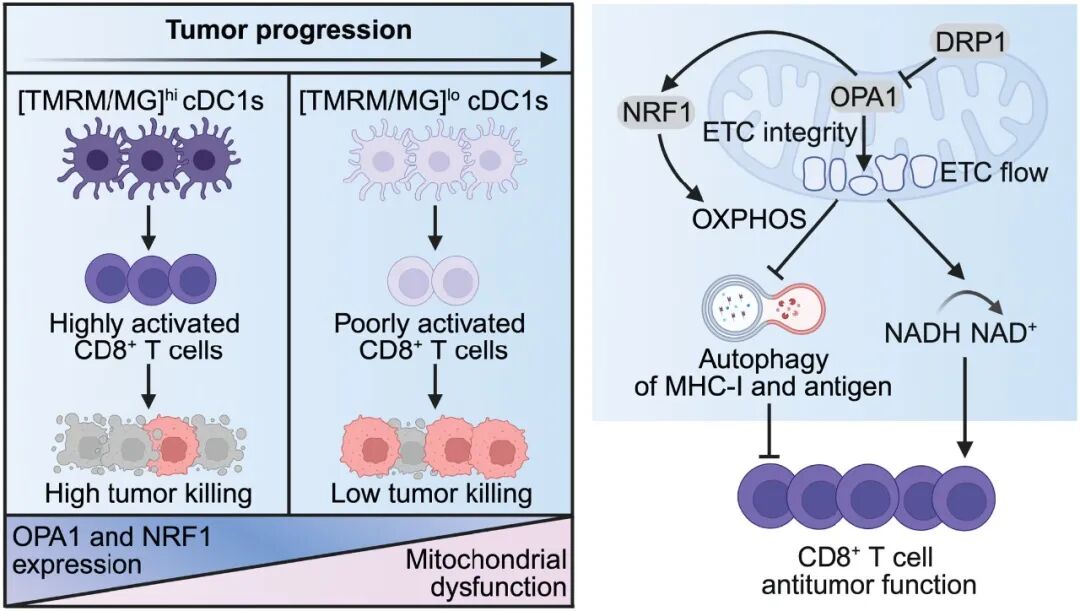
借助于荧光标记技术,迟洪波团队在小鼠和人的肿瘤中,发现cDC1存在两种截然不同的线粒体状态:
一类是极化线粒体(单位质量的线粒体具有更高的膜电位),另一类则是
去极化线粒体
。
他们还注意到,
含有极化线粒体的cDC1,表现出更强的氧化磷酸化活性、更高的ATP产量,以及更完整的线粒体嵴结构;在功能上,它还比去极化线粒体cDC1亚群能更好地激活CD8阳性T细胞
。
接下来,迟洪波团队开始探索cDC1线粒体发生上述变化的原因。他们的研究结果显示,
线粒体内膜融合
蛋白OPA1在瘤内cDC1中显著上调。如果在树突状细胞中特异性敲除OPA1的编码基因,则会导致线粒体碎片化、嵴结构紊乱,以及极化线粒体cDC1亚群的丧失。
从抗肿瘤效果来看,
OPA1缺失会显著削弱cDC1介导的抗肿瘤T细胞反应,导致多种肿瘤模型(如黑色素瘤、结肠癌、肝癌)生长加速
。后续的实验还发现,OPA1对于T细胞在肿瘤微环境中的二次激活至关重要,但对树突状细胞的迁移或在淋巴结中的首次激活影响较小。
至于背后的分子机制,研究人员也做了一些探索。对于含有极化线粒体的cDC1而言,
OPA1通过促进线粒体内膜融合和嵴结构的完整性,促进转录因子NRF1的表达和转录活性;这会维持线粒体高水平的氧化磷酸化活性,确保了充足的ATP供应,从而抑制
AMPK信号
的激活和病理性自噬的发生,防止了MHC-I和肿瘤抗原在溶酶体中被降解,从而确保cDC1能够有效地将信号传递给CD8阳性T细胞
。
不过,研究人员也注意到,
随着肿瘤从早期进展到晚期,瘤内cDC1的线粒体膜电位和体积呈现进行性下降
。这种退化与OPA1和NRF1表达水平的下调密切相关,导致cDC1在肿瘤晚期逐渐失去激活T细胞的能力,从而产生免疫逃逸。
至于解决办法,迟洪波团队发现,
将含有极化线粒体的cDC1过继回输到荷瘤小鼠体内,就可以提升小鼠的抗肿瘤免疫
。更重要的是,这种细胞疗法还能与PD-L1、CTLA-4或
PD-1抑制剂
产生强大的协同抗肿瘤作用,并建立长效抗肿瘤免疫记忆,防止肿瘤复发。
总的来说,迟洪波团队这项研究成果证实了线粒体功能对cDC1抗肿瘤功能的重要性,并初步揭示了背后的分子机制,为靶向cDC1的免疫疗法提供了新思路。
至于cDC1的线粒体功能为啥会随着肿瘤的进展而下降,研究人员认为肿瘤微环境中的缺氧、营养竞争、慢性炎症或代谢副产物等,可能是导致这种退化的潜在驱动信号。不过,过往还有研究显示,
癌细胞可以从树突状细胞等免疫细胞中“抢夺”线粒体
。这也可能是潜在原因之一。
