透明质酸酶作用概念重构:从“溶解”到“修饰”
透明质酸酶(Hyaluronidase)是医美领域应用最广泛的药剂之一。它在血管栓塞的处理中不可或缺,同时也越来越多地被用于改善过度填充、轮廓异常以及填充剂扩散(移位)等问题。最新指南细化了择期与急救场景下的给药策略。
虽然透明质酸酶具有如此重要的作用,但目前主流使用的“溶解填充剂”(Dissolving Filler)这一表述,在科学层面并不精准,在临床层面也有误导性。该表述默认透明质酸填充剂可被完全、均匀且可预测地清除,但这一假设并未得到填充剂流变学、透明质酸生物学特性、超声或磁共振成像结果的支持。临床中普遍观察到,透明质酸酶治疗带来的美学改善,无法仅由影像学检查结果完全解释;即便经过多次透明质酸酶治疗,仍有透明质酸残留。这一矛盾现象提示,透明质酸酶的作用靶点是填充剂-组织复合体,而非孤立、分散的凝胶沉积物。
本文作为一篇叙述性社论,综合了生物学原理、影像学观察结果与临床经验,而非一项基于假设的实验性研究或对照临床研究。本文主张摒弃“溶解”这一过时的表述,转而采用符合生物学事实、具备临床严谨性的概念:填充剂修饰(Filler Modification)。临床中,透明质酸酶治疗后产生的有临床意义的美学改善,往往与超声或MRI检查中可见的透明质酸残留同时存在。在分子层面,透明质酸酶可将透明质酸聚合物裂解为短片段,降低其黏度、内聚性与亲水性。交联减缓但无法阻止酶促降解过程。流变学研究显示,酶治疗后凝胶逐渐软化、凝胶完整性逐步丧失,而非被完全清除。针对市售透明质酸填充剂开展的体外对比研究表明,受生产工艺与凝胶结构影响,不同填充剂对透明质酸酶的敏感性存在显著差异。这些发现对可预测或完全溶解的假设提出了挑战。
内源性透明质酸的生物学特性,进一步反驳了常见的“溶后自发复原”(Dissolve and replace)的说法。原生真皮透明质酸的半衰期约为24小时,通过多种酶促途径(包括HYAL1、HYAL2、TMEM2、CEMIP)以及氧化降解等非酶促机制持续进行代谢周转。重要的是,这种基础代谢周转不会因透明质酸酶作用导致的原生透明质酸急性流失而上调,也无法将组织结构或组织容量恢复至治疗前状态。因此,“溶后自发复原”的理念在生理学层面并不准确。
在慢性过度填充的病例中,会观察到一种复合基质,其组成包括部分降解的填充剂、符合纤维化与间隔增厚特征的组织改变、长期亲水性引发的慢性水肿,以及发生机械性重分布的凝胶。透明质酸酶通过减轻肿胀、松解凝胶结构、提升组织柔韧性、释放下方原生解剖结构,与该复合体发生相互作用并对其进行修饰。因此,临床改善反映的是对填充剂-组织复合体的修饰,而非彻底清除每一个透明质酸分子。
反复注射或陈旧性填充剂,并不以离散、局限的沉积物形式存在。相反,填充剂融入一个动态的组织环境中,而该环境受水合作用、纤维组织增生、面部运动与挤压等机械力,以及沿解剖平面的间室内弥散或移位的影响。
这一模型解释了为何部分区域的透明质酸对透明质酸酶反应良好,而另一部分区域则耐抗;为何往往需要多次治疗;为何虽然临床已出现改善,影像学检查却常显示填充剂残留。因此,承诺“完全溶解”在科学上是站不住脚的,尤其是针对慢性、已与组织整合的填充剂-组织系统(图1、图2)。
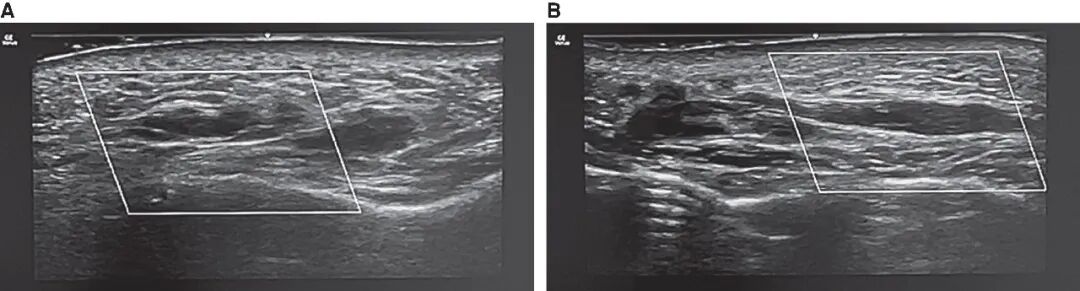
图1. 超声图像示透明质酸填充剂沿SMAS筋膜平面,从鼻唇沟区(A)向眶下区(B)走行,直观呈现了填充剂沿最小阻力路径、经解剖平面发生的移位。
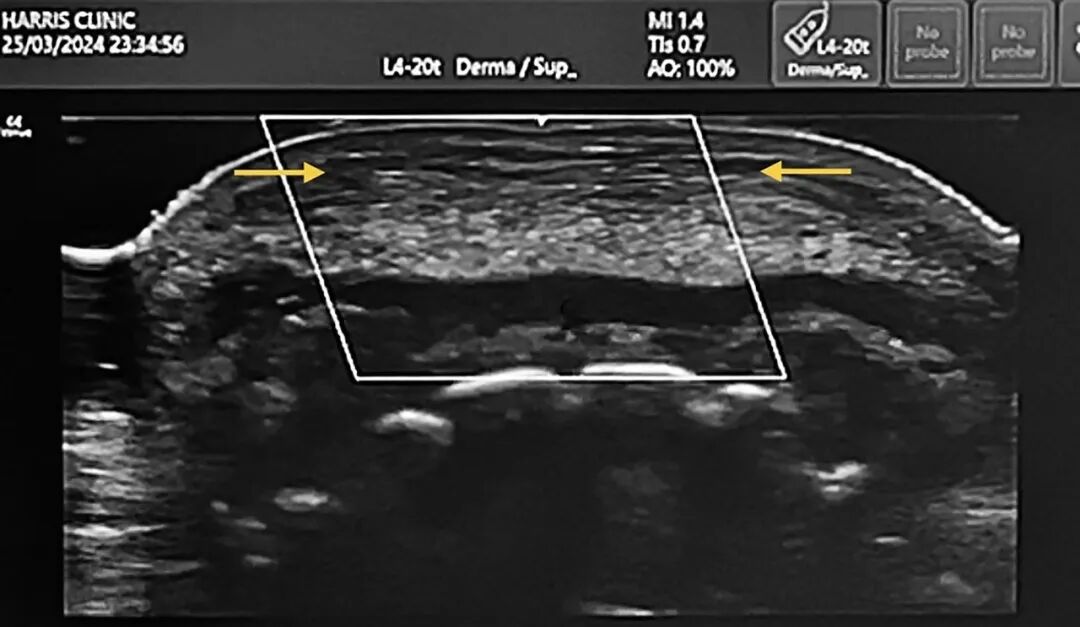
图2. 下唇部位的高频超声图像,示非计划性注入口轮匝肌缘部的透明质酸填充剂(箭头之间),符合陈旧性过度填充的影像学表现。
超声可为上述复杂机制提供重要影像学参考,高频超声成像可清晰显示:填充剂分布呈不均质性,即便非刻意注射,也常出现肌内置入现象;填充剂可沿筋膜或肌肉平面发生间室内弥散;且经透明质酸酶干预后,超声回声信号物质仅部分消减,而非完全消失。上述结果提示,酶解效果存在多样性差异,并非呈现「完全溶解 / 未溶解」的二元对立结局。
然而,超声发现仅为描述性而非确定性的,且回声模式不具备特异性——低回声区域可能代表残留透明质酸、水肿或积液,而纤维化通常呈高回声,可能部分遮挡下方的填充剂。陈旧性填充剂往往会产生混合回声,需要结合临床背景进行解读,且图像的采集与解读高度依赖操作者。设备质量也存在很大差异:与低分辨率的手持超声设备相比,高频医用超声系统(15–22MHz)可提供更优异的轴向分辨率与侧向分辨率;手持设备可能难以区分填充剂与水肿、深部脂肪或肌肉等邻近低回声结构,也可能无法清晰显示细微的纤维化改变。目前,业内尚无针对“完全清除”的统一超声诊断标准,因为即便临床外观已得到改善,残留凝胶、水肿与纤维组织增生仍可能同时存在(图3,视频1、视频2)。
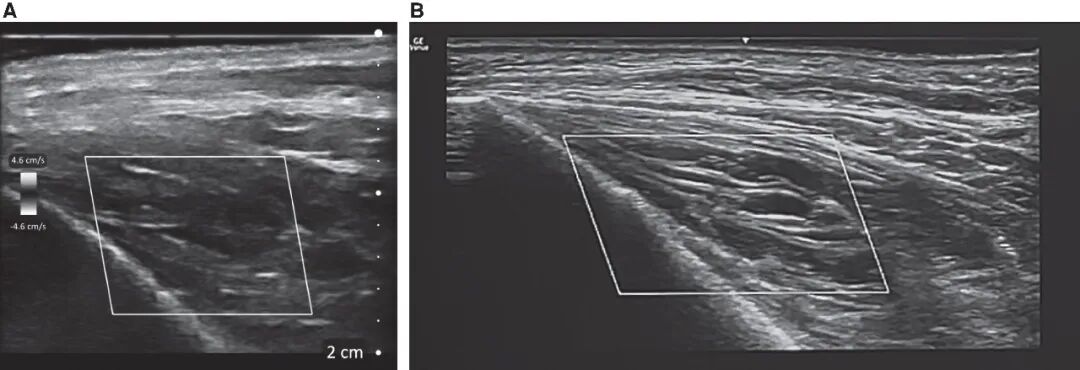
图3. 两种超声设备的成像效果对比。(A)手持式超声设备 Clarius L20;(B)高分辨率医用超声系统 GE Venue Go,搭配 L420 探头;图像清晰展示了二者在轴向分辨率与侧向分辨率上的差异。
MRI研究证实,填充剂在注射多年后仍可能在影像学检查中显影。然而,MRI存在重要的局限。目前尚无标准化的透明质酸特异性成像方案,且T2高信号与水肿、炎症、积液的信号存在重叠。因此,影像学解读结果差异极大,且MRI无法对残留填充剂的含量进行定量分析。因此,影像学检查只能明确:填充剂的留存情况远比此前设想的复杂,且影像学检查结果不应被解读为临床治疗成功的定量或确定性标志(图4)。
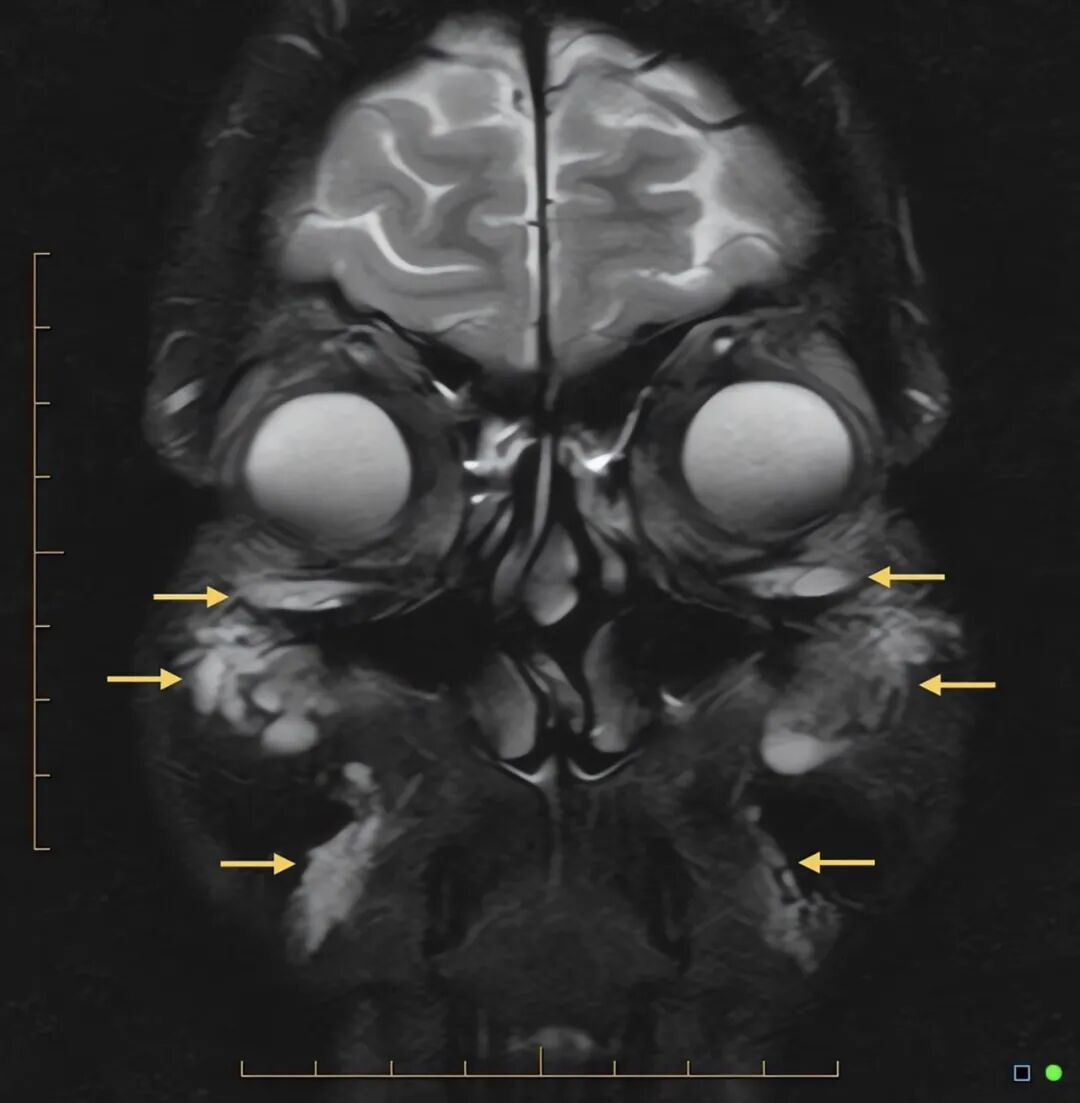
图4. 冠状位 T2 加权磁共振成像(MRI),示眶下区、颧前区、面颊深部及木偶纹区可见多发 T2 高信号灶(箭头所示);上述信号符合残留透明质酸填充剂的影像学特征,但可与水肿或其他软组织积液的信号相重叠。
“溶解”这一表述,错误诠释了酶的作用机制,易使患者产生不切实际的预期,且当后续影像学检查显示填充剂残留时可能增加医疗法律风险。透明质酸酶仅能裂解透明质酸,无法破坏胶原蛋白、脂肪、筋膜、韧带或其他结构性组织。长期沉积的填充剂与发生病理改变的软组织深度交织,绝非简单的 “溶解与否” 模型所能概括(图5)。
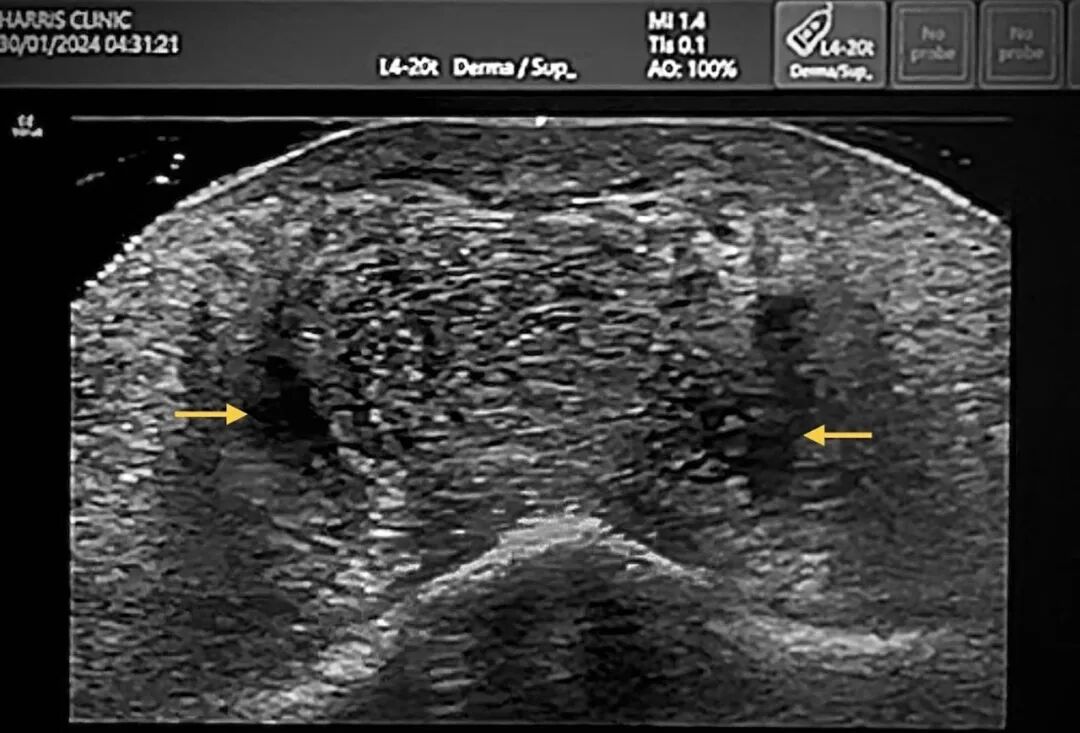
图5. 颏部超声图像,示陈旧性填充剂相关继发改变,包括持续存在的透明质酸填充剂(箭头所示)、间质水肿,以及高回声纤维性间隔。
心理因素进一步增加了结果解读的复杂性。大多数患者对透明质酸酶持正面看法,但少数群体(通常在在线论坛上很活跃)将正常的解剖差异、年龄相关改变,或陈旧性填充剂的继发效应(如组织扩张或牵拉)错误归因于“透明质酸酶损伤”。关于感知漂移的定性研究表明,经过多年的填充剂注射,患者可能会对失真的面部比例产生适应,以至于原生解剖结构的恢复被患者感知为组织缺损。上述结论均基于临床观察分析得出,虽有待前瞻性研究进一步验证,但也提示我们:在为患者进行咨询沟通时,务必使用精准、符合生物学原理的严谨表述。
大剂量透明质酸酶治疗,无疑是救治血管栓塞的金标准。但择期性透明质酸酶治疗,其临床应用场景与救治性治疗存在本质区别。陈旧性填充剂的理化特性与近期注射的填充剂截然不同,治疗效果取决于周围组织微环境,且美学修复往往需要分期干预。将此类择期干预重新定义为“填充剂修饰”(Filler Modification)而非填充剂溶解(Filler Dissolution),更贴合临床现实,同时也会直接影响诊疗沟通、知情同意、给药剂量策略、治疗时机选择及疗效评估等全流程管理。
目前,尚无经过验证的美学量表、容积测量或标准化的患者报告结局指标,可对透明质酸酶治疗后出现的上述结构改变进行定量分析。同样,本文提出的将透明酸酶的作用表述从“溶解”转为“修饰”,也尚未经过实证检验。该理念是一个基于生物学作用机制、影像学结果差异性与临床经验建立的概念框架,而非基于数据的结局对比。全球范围内,临床实践模式、监管环境与影像学专业水平均存在差异,本文提出的概念应结合当地临床背景进行解读。
透明质酸酶并非如现有术语所简单表述的那样,直接 “溶解” 透明质酸填充剂。它实则通过改变凝胶结构、水合状态、力学特性及解剖显见性,对复杂的填充剂‑组织系统起到修饰作用。采用 “修饰” 这一表述,可让临床实践与生物学客观事实相契合,提升患者认知、降低医疗法律风险,同时有助提升医美服务的透明度与规范性。
Steven Harris, Steven Weiner, Reframing Hyaluronidase in Aesthetic Medicine: From “Dissolving Filler” to “Modifying Filler”, Aesthetic Surgery Journal, 2026;, sjag022,
↑ 原文 → 点击本文底部“阅读原文”
