死细胞去除磁珠如何提升稀有细胞分析的准确性?
一、为什么死细胞会干扰下游分析结果?
在单细胞测序、流式细胞术及循环肿瘤细胞检测等前沿技术中,样本中死细胞的存在始终是影响数据质量的关键因素之一。死细胞在凋亡或坏死过程中会释放DNA酶、蛋白酶及自身抗原,这些物质不仅会降解活细胞内的目标核酸分子,还可能诱发非特异性抗体结合,导致背景信号显著升高。此外,死细胞的膜通透性增加,使得荧光染料或核酸标记物易于被动扩散进入胞内,从而产生高比例的假阳性信号。尤其在稀有细胞(如循环肿瘤细胞或干细胞)分析中,死细胞所占比例虽可能不高,但其释放的游离核酸与碎片却足以掩盖真实信号,导致目标细胞被误判或遗漏。因此,在样本前处理阶段高效去除死细胞,已成为保障稀有细胞分析准确性的必要步骤。
二、磁珠去除死细胞的原理是怎样的?
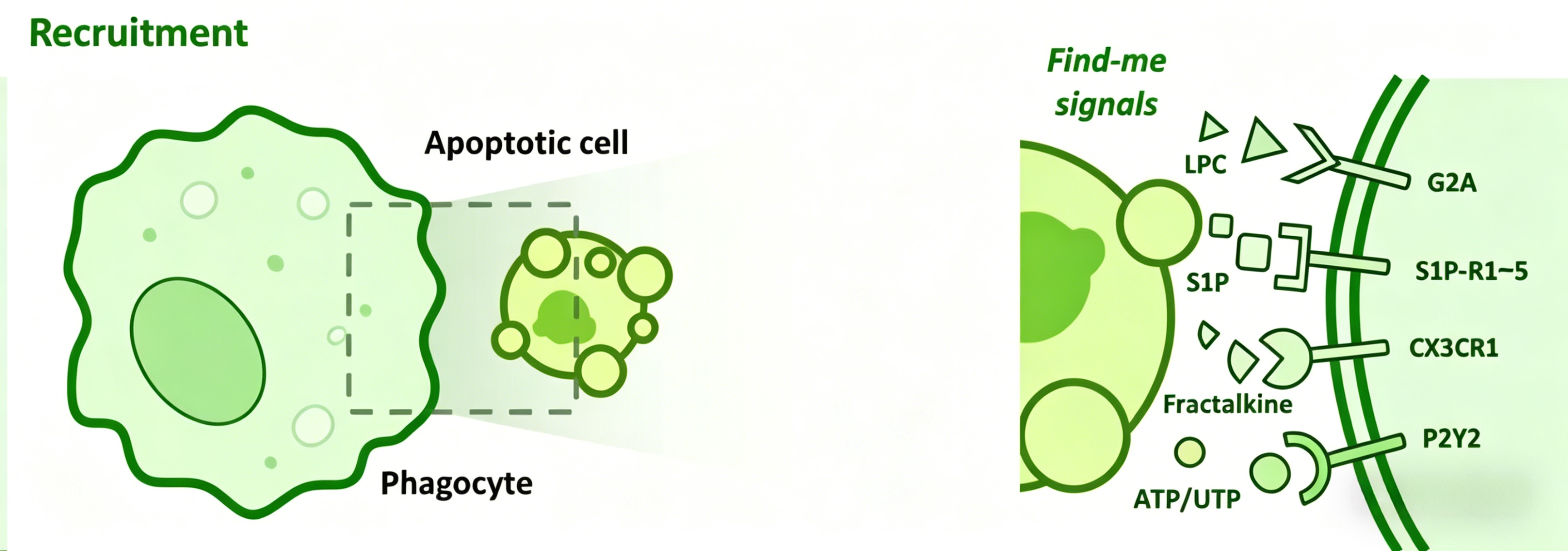
死细胞去除磁珠主要基于表面化学修饰与磁分离技术的协同作用。具体而言,磁珠表面共价偶联了对死细胞具有特异性识别能力的亲和配体,例如靶向死细胞暴露的磷脂酰丝氨酸的膜联蛋白V,或识别细胞内受损DNA的阳离子染料衍生物。当将磁珠与待处理细胞悬液混合孵育时,磁珠能够选择性地结合在死细胞膜表面或进入其胞内。随后,将混合体系置于外加磁场中,结合了磁珠的死细胞被磁场捕获并富集于管壁或分离柱上,而活细胞则因未结合磁珠而保留在上清液中。通过一次或多次磁吸分离操作,即可高效移除样本中的死细胞,获得高活性的活细胞悬液。该过程无需离心,操作温和,对活细胞的物理损伤极小,尤其适用于脆弱或数量稀少的细胞类型。
三、实验参数如何影响去除效率?
为获得理想的死细胞去除效果,若干关键实验参数需予以优化。第一,磁珠与细胞的比例是决定结合充分性的核心变量。比例过低会导致死细胞残留,比例过高则可能因非特异性吸附而误伤活细胞。第二,孵育温度与时间也显著影响结合特异性。通常,在4℃条件下孵育15至30分钟可有效降低非特异性背景,同时保持配体与死细胞标志物的亲和力。第三,磁场强度与分离时长需根据磁珠型号及细胞密度进行调整。强磁场虽可加速分离,但可能造成活细胞的机械应力损伤;弱磁场则可能无法完全捕获结合磁珠的死细胞。建议研究者通过预实验建立标准曲线,并借助流式细胞术或细胞活性染色对去除前后样本进行对比验证,以确定针对特定细胞类型的最优参数组合。
四、该技术在稀有细胞分析中具体有哪些应用?
死细胞去除磁珠已在多个前沿研究领域展现出不可替代的作用。在循环肿瘤细胞检测中,血液样本经过冷冻运输或低氧环境处理后,大量白细胞可能发生凋亡,若不加以去除,这些凋亡白细胞的碎片会干扰肿瘤特异性标志物的检测。通过磁珠去除死细胞后,循环肿瘤细胞的检出率可提升约两至三倍。在神经干细胞培养中,死细胞释放的活性氧物质会抑制邻近干细胞的增殖与分化,利用磁珠及时清除死细胞,可显著提高克隆形成率与细胞活力。此外,在单细胞RNA测序流程中,死细胞占比若超过百分之十,将导致测序数据中出现大量线粒体基因高表达的劣质细胞,严重影响降维聚类与差异基因分析。应用死细胞去除磁珠预处理样本后,合格单细胞的比例与测序文库的复杂度均得到实质性改善。
五、未来技术发展方向有哪些潜在可能?
尽管当前死细胞去除磁珠已相对成熟,但仍存在若干可优化方向。其一,开发基于多种死细胞标志物联合识别的新型磁珠,以覆盖不同死亡通路下的细胞亚型,避免因单一标志物下调而造成的漏除。其二,将死细胞去除模块与活细胞分选或单细胞捕获平台集成于同一微流控芯片中,实现"样本进、活细胞出"的全封闭自动化流程。其三,探索可生物降解或可逆释放型磁珠,在完成死细胞捕获后,通过酶切或pH变化使磁珠从死细胞上解离,从而避免磁珠对后续检测(如质谱或电镜)的干扰。这些进展将进一步提升稀有细胞分析的通量与精度。
