核苷治疗的患者,合并MASLD的疾病进展与远期风险显著更高
编者按
近年来,随着全球肥胖和代谢综合征的流行,代谢相关脂肪性肝病(MASLD)的患病率急剧上升,与慢乙肝构成了日益普遍的“共病”状态。这种“病毒-代谢”双重打击对肝脏长期预后的影响,目前仍存在一定争议。部分观点认为,肝脏脂肪变性可能通过某些机制抑制HBV复制,似乎具有潜在的“保护作用”,也有观点认为,MASLD可能通过代谢性炎症环境,加剧肝细胞损伤及纤维化,从而加速肝病进展。
近期,台北市立万芳医院吴明顺教授团队发表一项大样本回顾性研究成果,结果显示,在接受长期核苷(酸)类似物(NAs)治疗获得病毒学抑制的慢乙肝患者中,合并MASLD会显著增加肝硬化及肝癌的发生风险,并大幅降低10年总生存率。
 研究方法
研究方法
本研究采用了创新的双队列设计,旨在从群体规律和个体机制两个层面全面评估MASLD的影响。
真实世界分析部分:利用美国TriNetX协作网络数据库,筛选了接受长期NAs治疗且血清HBV DNA检测不到的慢乙肝患者,并将其划分为合并MASLD组与无MASLD组。为控制偏倚,研究采用1:1倾向性评分匹配(PSM),严格平衡了年龄、性别、种族、ALBI/FIB-4指数及多种合并症,最终两组各纳入4761例患者进行对比分析。该部分的主要临床终点为10年内肝癌及肝硬化的累积发病率,次要终点为总生存率(OS)。
临床队列部分:研究回顾性纳入了201例受试者,其中包含64例接受长期NAs治疗且血清HBV DNA检测不到的慢乙肝患者(其中50例为慢乙肝合并MASLD,14例为单纯慢乙肝),以及137例单纯MASLD对照患者。根据受控衰减参数(CAP),患有MASLD的患者被分为轻度(S1,215-252 dB/m)、中度(S2,252-296 dB/m)及重度(S3,>296 dB/m)脂肪变性亚组。通过瞬时弹性成像技术评估肝脏硬度(LSM),并系统检测了受试者的代谢参数及TNF-α、IFN-γ等核心细胞因子水平,以深度探究MASLD影响肝脏的病理生理机制。
研究结果
1.合并MASLD的慢乙肝患者代谢紊乱特征更显著
PSM后的TriNetX基线数据显示,尽管两组在肝脏生化指标及基础背景上基本均衡,但相比于无MASLD的慢乙肝患者,合并MASLD组的BMI、甘油三酯、总胆固醇以及糖化血红蛋白(HbA1c)水平显著更高。
表1 PSM后的TriNetX患者基线特征
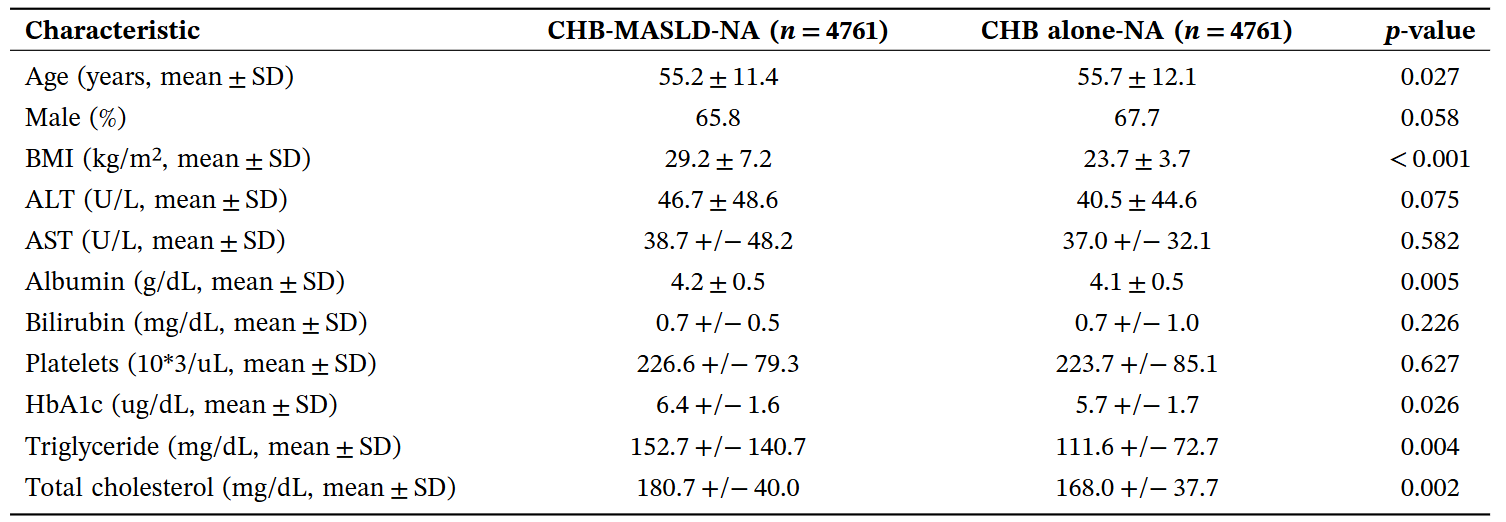
2.MASLD显著降低患者10年总体生存率,并显著增加肝癌与肝硬化风险
Kaplan-Meier分析显示,合并MASLD组的10年总生存率仅为61.45%,显著低于无MASLD组的79.30%(p<0.001)。进一步的多因素Cox比例风险回归模型确认,合并MASLD使全因死亡风险增加了1.75倍(HR=1.75),此外,MASLD也是慢乙肝进展为肝癌或肝硬化的独立危险因素,风险增加1.55倍(HR=1.55)。而值得注意的是,在该模型中,HBV DNA病毒载量并不是一个有预测意义的指标,提示对于共病患者,代谢因素已取代病毒复制,成为决定预后的主导力量。
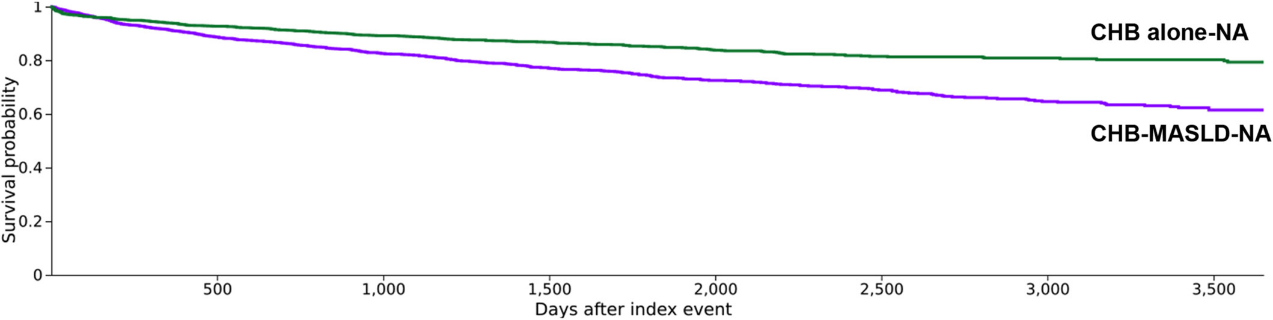
图1 K-M分析的10年生存率
表2 Cox比例风险模型评估进展为肝癌或肝硬化的风险因素
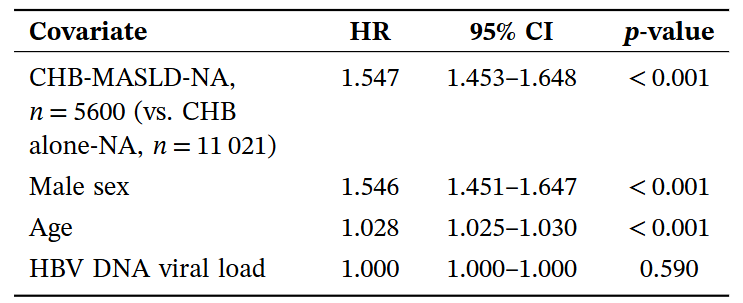
3.临床队列证实:慢乙肝合并MASLD显著增加晚期肝纤维化负担
临床队列的数据进一步印证了以上结果。随着肝脏脂肪变性严重程度的增加,慢乙肝合并MASLD组患者的肝脏硬度值呈现出显著升高的趋势,在中度脂肪变性(S2亚组)时达到峰值9.853 kPa,而处于同等脂肪变性程度的单纯MASLD患者,其肝脏硬度仅为4.952 kPa。以上结果提示,HBV感染与代谢紊乱在诱导肝脏纤维化方面可能存在协同叠加效应。
表3 按CAP分层的临床队列特征
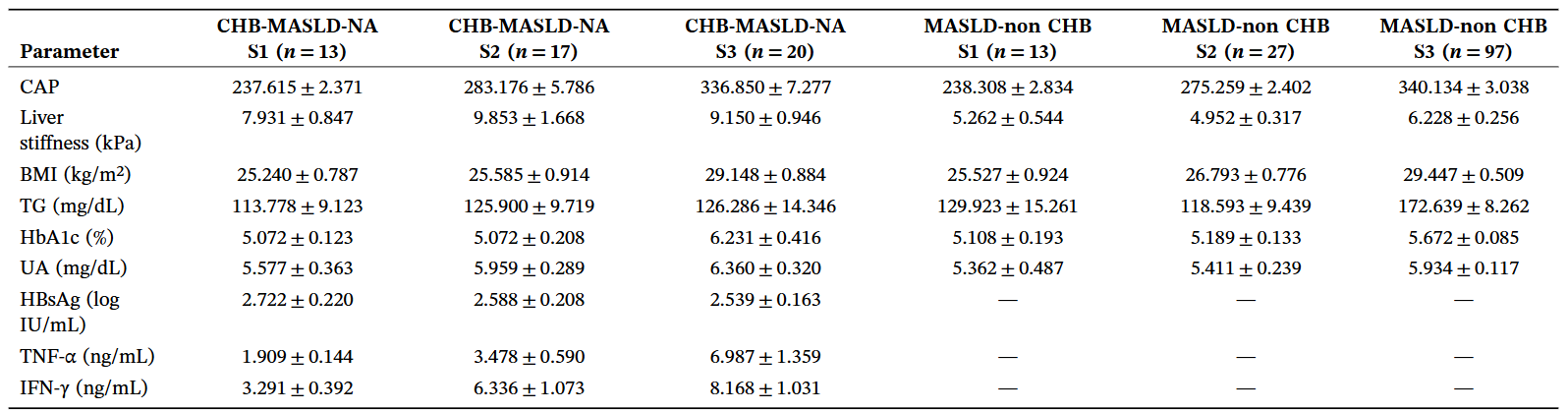
在纤维化分期分布上,慢乙肝合并MASLD组中患有晚期肝纤维化(F4期)的患者比例高达28.0%,显著高于单纯慢乙肝患者(14.3%)及单纯MASLD患者(4.38%),进一步提示了HBV与MASLD在促进肝纤维化上的协同效应,即使病毒已被抑制,这种由代谢异常驱动的纤维化进程仍在加速。
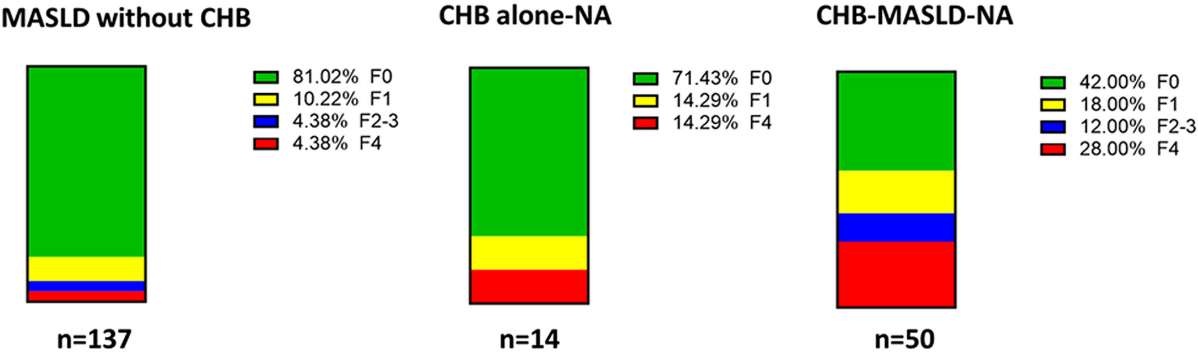
图2 临床队列中单纯MASLD、单纯慢乙肝及慢乙肝合并MASLD患者的肝纤维化分期分布
4.肝脏脂肪变性诱导促炎性免疫微环境
研究进一步通过细胞因子分析揭示了潜在的免疫机制。随着脂肪变性严重程度(从S1到S3)增加,患者体内的HBsAg水平呈现出下降趋势(2.722下降至2.539 log IU/mL),表明肝脏脂肪变性似乎有助于病毒清除。然而,随着脂肪变性的加剧,患者体内的抗病毒因子IFN-γ和促炎因子TNF-α水平会出现失衡——在S3组,TNF-α的水平相较S1组增加约3.73倍,而IFN-γ仅增加约2.13倍。这种“促炎/抗病毒”比值失衡,不仅无法带来真正的免疫获益,反而让肝脏处于由过度代谢炎症主导的持续性损伤之中,最终导致了肝硬化和肝癌的发生。
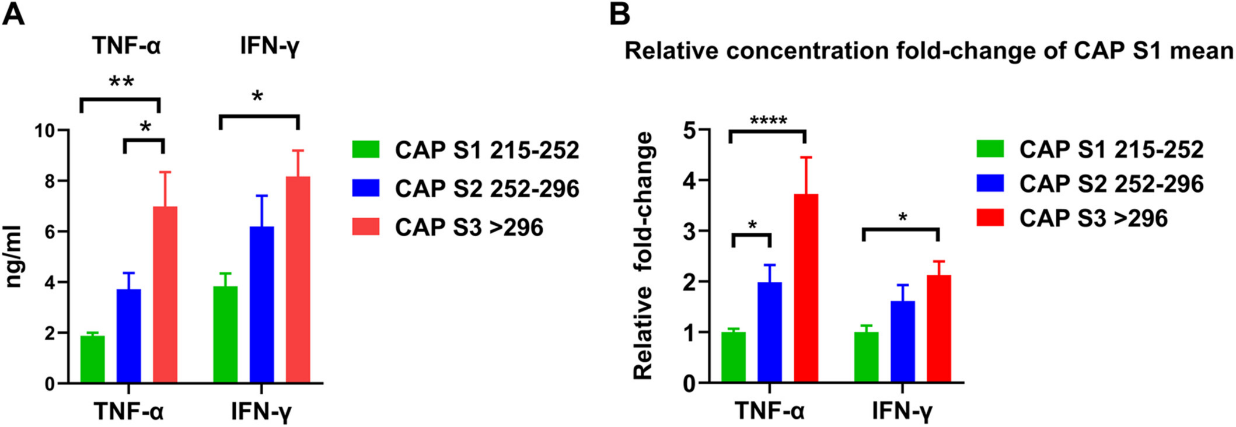
图3 不同程度肝脏脂肪变性亚组中TNF-α和IFN-γ的水平
A:TNF-α和IFN-γ的水平;B:IFN-γ和TNF-α水平的相对倍数变化(以S1组为参考)
* p < 0.05,** p < 0.01,**** p < 0.0001
肝霖君有话说
本研究表明,当慢乙肝患者合并MASLD时,即便患者表现出较低的病毒水平甚至更高的HBsAg清除倾向,其罹患肝硬化、肝癌与全因死亡的风险不仅没有降低,反而显著升高。以上结果提示,对于长期接受NAs治疗的慢乙肝患者,即使实现了理想的病毒学抑制,可能也不足以阻断由代谢因素驱动的纤维化进展。因此,对于共病患者,应实现“抗病毒+代谢干预”的整合,将改善代谢指标(如减重、控制血糖血脂)提升到与抗病毒同等重要的战略高度。此外,在常规的病毒学监测之外,可将基于瞬时弹性成像等无创工具的定期肝纤维化与脂肪变性筛查纳入诊疗流程,以便早期发现肝纤维化进展,为共病患者赢得更长的生存期和更好的生活质量。
参考文献
Shiue S J, Ho T H, Lin H Y, et al. Impact of Metabolic Associated Steatotic Liver Disease on Antiviral Therapy Outcomes on Chronic Hepatitis B Patients Receiving Antiviral Therapy[J]. Journal of Medical Virology, 2026, 98(3): e70864.
