TR-FRET技术的PCSK9抑制剂在缺血性卒中防治策略
一、PCSK9的分子机制与脂质代谢调控
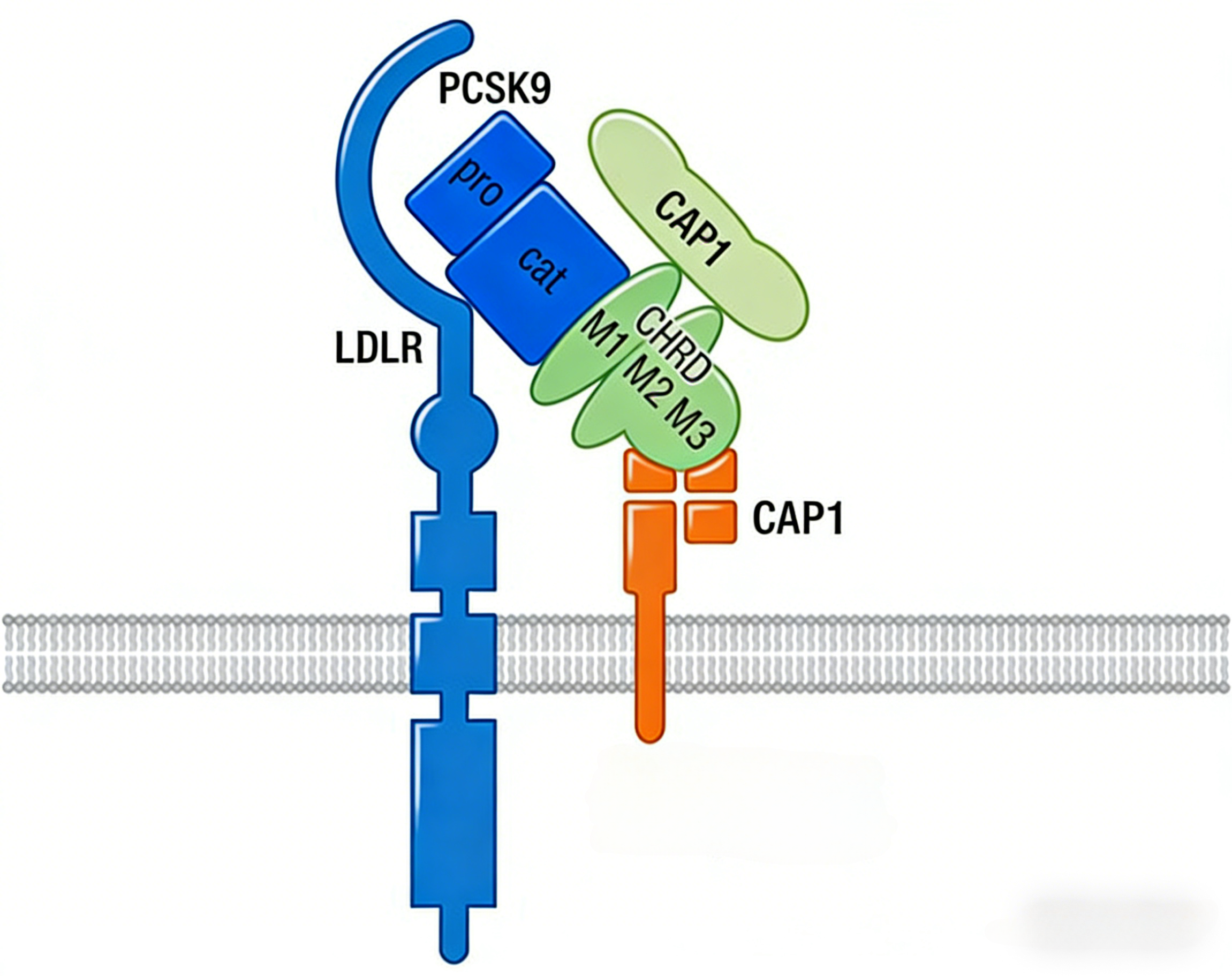
PCSK9是主要由肝脏合成的分泌型丝氨酸蛋白酶,在维持胆固醇稳态上发挥重要作用。PCSK9通过抑制循环LDLR而升高LDL-C水平,竞争性结合肝细胞表面LDLR,形成PCSK9/LDLR复合物,经囊泡转运进入胞内被溶酶体降解,导致血浆LDL-C水平升高。此外,PCSK9还能促进LRP-1、VLDLR、ApoER2的降解,并通过载脂蛋白E和LDLR相关通路促进肝脏脂质和脂蛋白生成。TR-FRET PCSK9-LDLR检测试剂盒可用于定量检测PCSK9与LDLR的结合活性,为研究该蛋白的生物学功能提供技术工具。
二、PCSK9在动脉粥样硬化与血栓形成中的作用
PCSK9经JNK/p38 MAPK通路诱导内皮细胞凋亡,促进ox-LDL所致动脉粥样硬化,并降低动脉粥样硬化斑块稳定性。在动脉粥样硬化斑块进展中,巨噬细胞和平滑肌细胞生成的载脂蛋白E可与ApoER2结合而降低胞内脂蛋白积聚、抑制泡沫细胞形成,PCSK9通过降低ApoER2表达而削弱载脂蛋白E的血管保护作用。在血小板活化与血栓形成方面,PCSK9是血小板过度活化与加速血栓形成的独立危险因素。一方面,血浆PCSK9水平升高通过降低脂蛋白消耗而间接激活血小板;另一方面,PCSK9可独立于LDLR通路与CD36受体结合,直接促进血小板活化与血栓形成。TR-FRET技术可应用于筛选能够阻断PCSK9与LDLR结合的抑制剂,评估其阻断效率。
三、PCSK9抑制剂的临床研究证据
FOURIER研究在27564例ASCVD患者中评估了PCSK9抑制剂的疗效,结果显示治疗48周可显著降低MACE事件风险达15%,并降低缺血性卒中风险达20%。ODYSSEY OUTCOMES研究在18924例ACS患者中评估了PCSK9抑制剂的疗效,亚组分析表明对于既往缺血性卒中患者,治疗78周可显著降低缺血性卒中风险,且不会增加出血性卒中风险。GLAGOV研究表明,他汀联合PCSK9抑制剂治疗76周后,64%的患者实现了动脉粥样硬化斑块逆转。此外,PCSK9抑制剂还能增加早期纤维帽厚度,逆转富含脂质斑块,改善斑块形态。
四、PCSK9抑制剂的安全性特征
临床研究数据显示,PCSK9抑制剂总体耐受性良好。常见不良反应包括注射部位反应,如轻度红斑、疼痛或肿胀,通常为一过性。与安慰剂组相比,PCSK9抑制剂组新发糖尿病和神经认知事件发生率无显著差异。出血性卒中风险也未增加,这一安全性特征对缺血性卒中患者的长期管理尤为重要。在肾功能不全患者中,PCSK9抑制剂的药代动力学和药效学特征与肾功能正常患者相似,无需剂量调整。TR-FRET PCSK9-LDLR检测试剂盒可用于评估不同PCSK9抑制剂对靶点的结合亲和力,为安全性评价提供分子水平依据。
五、新型PCSK9抑制剂的研发进展
小干扰RNA药物通过诱导PCSK9 mRNA降解,阻止其翻译成蛋白质。临床研究显示该类药物可显著降低PCSK9和LDL-C水平,作用可持续达6个月,不良事件均为轻度或中度。研究发现,PCSK9与LDLR结合时依赖于CAP1,提示CAP1亦可能是潜在的降脂靶点。此外,PCSK9抑制剂可通过抑制血小板活化和血栓形成而预防或降低缺血性卒中风险。天然化合物如小檗碱、姜黄素和虎杖苷在体外研究中显示出抑制PCSK9表达的潜力,为开发新型PCSK9抑制剂提供了思路。TR-FRET技术可应用于高通量筛选新型PCSK9抑制剂,评估其与LDLR的结合活性。
六、未来研究方向与展望
随着对PCSK9新型降脂靶点的研究日益深入,PCSK9在升高血脂、加速动脉粥样硬化进展、促进血栓形成中的作用机制正被层层揭示。当前已有多项PCSK9抑制剂临床研究正在进行之中,一些研究旨在考察PCSK9抑制剂对急性卒中的疗效,另一些研究则评估其对颅内动脉粥样硬化斑块的改善作用。PCSK9抑制血小板活化的背后机制当前仍未完全阐明,有待后续研究进一步探索,以建立更具靶向性的缺血性卒中治疗方案。TR-FRET PCSK9-LDLR检测试剂盒为研究PCSK9与LDLR相互作用和抑制剂筛选提供了灵敏、高效的检测工具,可应用于药物发现、活性评价和质量控制等多个环节。
七、总结
PCSK9抑制剂通过阻断PCSK9与LDLR结合,降低LDL-C水平,同时通过抑制动脉粥样硬化斑块形成和血栓形成,为缺血性卒中患者带来临床获益。临床研究证实PCSK9抑制剂可显著降低缺血性卒中风险,并逆转动脉粥样硬化斑块。TR-FRET PCSK9-LDLR检测试剂盒在该类药物研发和质量控制中具有重要应用价值。
