发酵或半合成抗生素杂质:FDA要求做毒理,中欧设具体限度

*仅作示意用。
4月17日,FDA发布题为《建立抗生素的杂质质量标准》(Establishing Impurity Specifications for Antibiotics)的指南草案。
FDA指出,完全通过化学合成生产的抗生素应遵循ICH Q3A、Q3B及M7指南中关于杂质和降解产物的控制原则(识林会员可登录ICH索引页面查阅本文提及的ICH指南)。本指南旨在填补发酵法和半合成法生产抗生素(包括部分特定抗生素品种)杂质和降解产物控制的监管空白,明确其识别、界定(qualification)与控制策略。
针对同类主题,我国最新指南是CDE于2025年7月定稿的《发酵或半合成化学仿制药抗生素有关物质限度制定指导原则》,EMA早在2012年7月定稿了《关于抗生素中相关杂质的质量标准设定的指导原则》。相比之下,我国与欧盟指南更为接近,均明确杂质限度,FDA新指南则要求做毒理研究。识林读者可仔细阅读甄别。
篇幅所限,本文仅作摘要,供参考。
FDA提出总体原则,虽不追溯但预期指南定稿后贯彻实施
指南不涵盖以下类型杂质:不应存在的外源性污染物;微生物控制项目(如内毒素限度、微生物限度);发酵来源的细胞底物衍生杂质(如残留宿主细胞蛋白、残留宿主细胞DNA);残留溶剂和元素杂质;以及容器密封系统或生产设备产生的浸出物。
FDA给出杂质与降解产物可接受标准的建立原则,应基于以下数据支持:临床试验数据;非临床研究数据(如计算机模拟、体外及动物研究);在适用情形下,药品与其对应参比制剂(RLD)中降解产物的对比分析、使用场景(context of use)、先验知识、公开信息,以及分析方法的精密度。
一个原则是,对于发酵法和半合成法生产的抗生素,也应适用ICH Q3及ICH M7的原则。凡在美国药典(USP)中各论收载的抗生素药品,必须符合相应各论对原料药(API)和制剂的规定。
一个关键信息是,FDA明确不追溯该指南定稿前已提交申请或补充申请的抗生素药品,亦不适用于此前已上市的抗生素药品,以避免因生产中止或中断导致供应链风险。但是,FDA预期已上市抗生素申请人在进行重大变更(如更换API来源)时,应考虑依据本指南更新杂质标准,并确保药品生产符合CGMP要求。
FDA分别针对新药、仿制药和OTC提出要求,超限需做毒理研究
对于新药申请和505(b)(2)及相关API,FDA要求:
API中特定杂质或制剂中特定降解产物的可接受标准不超过ICH Q3规定的界定限度(qualification threshold)时,无需额外论证。
若高于界定限度,申请人应提交该杂质或降解产物在拟订限度下安全性的论证资料,如采用适宜给药途径和剂量、周期为14至90天的重复剂量全身毒性研究,具体取决于适应症的用药周期。
对于505(b)(2)“改良型新药”中无毒理学担忧的杂质,申请人可参考相关USP各论或采用相关替代药典各论中的限度。申请人也可开展与RLD的并列对比分析(side-by-side comparative analysis)来制定可接受标准。对比分析应采用经过验证、适用于预期用途的同一分析方法,并采用申报药品和RLD的多个批次样品。
API中总杂质或制剂中总降解产物的可接受标准不应超过各特定杂质(已鉴定和未鉴定)和非特定杂质可接受标准之和。
对于仿制药申请及相关API,FDA建议申请人可采用以下三种方法之一。方法一:若存在相关USP各论且无毒理学担忧,则参考USP各论或相关替代药典各论。方法二:采用申报药品与RLD的并列对比分析,使用经过验证、适用于预期用途的同一分析方法在多个批次上进行对比,据此制定可接受标准。方法三:若不超过ICH Q3规定的界定限度,且无毒理学担忧,则无需额外论证。申请人可采用基于风险的方法提出更高的可接受标准,FDA将基于总体证据进行评估。但若杂质限度超出ICH Q3界定限度,或杂质水平高于RLD,申请人应提交安全性的论证资料(如14至90天重复剂量全身毒性研究)。此外,总杂方面的要求与新药一致。
对于新药和仿制药,FDA均建议申请人通过会议或受控通信提前与之沟通。
对于非处方药(OTC)各论药品,FDA更强调对于USP各论和通则的依从。当存在毒理学担忧或有致突变可能性,则也需安全性的论证(如14至90天重复剂量全身毒性研究)或按ICH M7的要求开展风险评估。
EMA和NMPA设具体限度
相比FDA,EMA指南通过分类预先划定限度,我国指南也沿用(如下图)。
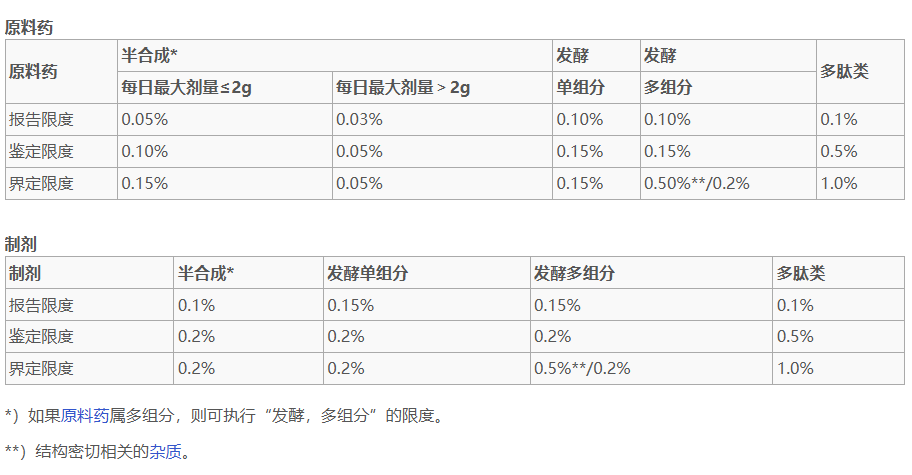
*截取自CDE指南(识林页面)
如果杂质高于上述限度,EMA进一步提供多种界定选项,包括与已上市产品进行比较。但EMA指出,部分已上市产品含有高于鉴定限度的未知杂质,此时新申请人应当至少鉴定其结构,还可能因此修订欧洲药典各论。对于替考拉宁(teicoplanin)和庆大霉素(gentamicin)等特别存在问题的现有活性物质,EMA已认识到在达到报告限度和鉴定限度方面存在困难,可参考EMA指南的范围和分析方法章节进行处理。CDE指南要求“如发现存在安全性隐患,应适当收紧限度;如需设定更宽的限度,应进行充分论证”。
EMA和NMPA对分析方法的要求更为具体
对于分析方法,FDA指南未具体提出额外要求,仅特别强调,方法学专属性应采用强制降解试验(stress testing)样品证明方法的稳定性指示(stability-indicating)特性。
EMA指南在分析方法部分表述更为详细。EMA指出,分析方法应尽可能采用外标法并以重量/重量(w/w)计算,以评估并排除任何可能的质量不平衡。若采用面积归一化法,相关组分及有关杂质应在检测器中具有相似响应,否则应使用校正因子。对于由一系列化合物组成的某些活性物质,面积归一化法可接受。采用面积归一化法时,应证明在拟定范围内的线性,并明确定义忽略限(disregard criterion)。
进行杂质谱与已批准产品的界定时,分析方法的专属性应足够。对于复杂混合物,分离技术(如高效液相色谱法)应与质谱法或其他技术联用,但日常检验可合理采用简化方法。分析方法的定量限不应超过报告限度。对于具有弱发色团的物质,应采用紫外吸收以外的检测方法。
CDE指南对分析方法的要求是,“有关物质分析方法应对潜在杂质具有良好的分离和检出能力,推荐采用富含杂质的样品(如,杂质加标样品、原料药粗品或分离纯化前样品等)确证方法的专属性。杂质定量方法通常建议采用外标法或加校正因子的主成分自身对照法。对属于弱发色团的抗生素,应筛选适宜的检测方法,确保方法定量限不高于报告限度。对于杂质谱复杂的药物,推荐将分离技术(如,HPLC 法等)与质谱分析等技术联合应用,经充分的合理性论证后,常规检测时可采用较简单的方法。”
|责任编辑:识林-木姜子
|编辑:识林-雪见
识林®版权所有,未经许可不得转载

【关于识林-常见问题与解答】

