铁死亡(Ferroptosis)是一种由脂质过氧化过度积累所引发的细胞死亡形式。质膜(PM)是含多不饱和脂肪酸(PUFA)的磷脂过氧化的主要发生部位,会导致膜破裂并引发铁死亡。除了质膜,多个亚细胞器膜也参与铁死亡过程。线粒体膜上脂质过氧化的积累或膜通透性的增加已被证明可调控铁死亡敏感性。最近,内质网(ER)膜被确定为脂质过氧化发生于质膜之前的初始部位。有趣的是,高尔基体这一负责蛋白质和脂质加工及分选的膜结合细胞器,参与氧化应激的调控,并表现出膜脂质过氧化。然而,高尔基体如何响应铁死亡诱导以及定位于高尔基体的蛋白是否能调控铁死亡的执行,目前仍不清楚。
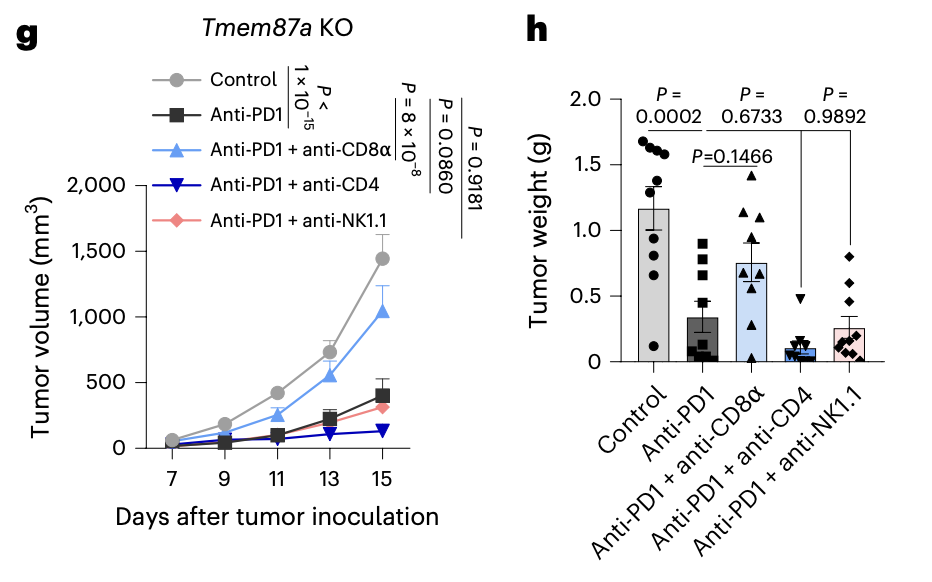
2026 年 4 月 21 日,华中科技大学王维民教授团队在 Nature 子刊 Nature Cancer 上发表了题为:TMEM87A suppresses ferroptosis and increases cancer immunotherapy resistance by maintaining the Golgi apparatus pH homeostasis 的研究论文。该研究表明,TMEM87A 通过维持高尔基体的 pH 值稳态来抑制铁死亡并增强癌症免疫治疗耐药性,而靶向抑制 TMEM87A 可作为增强癌症免疫治疗一种有效策略。大多数膜结合细胞器都与铁死亡的启动和执行有关。然而,高尔基体及其定位于高尔基体的蛋白在铁死亡中的作用,目前仍不清楚。在这项最新研究中,研究团队发现,铁死亡诱导剂在铁死亡早期阶段会触发高尔基体膜的脂质快速氧化,导致高尔基体的 pH 值失衡。研究团队还发现,定位于高尔基体的跨膜蛋白 TMEM87A 通过缓冲高尔基体 pH 值介导铁死亡抵抗。敲除 TMEM87A 会导致高尔基体的过度酸化,从而损害铁死亡抑制蛋白 FSP1 介导的辅酶 Q 还原过程。体内实验表明,TMEM87A 的缺失能抑制包括黑色素瘤、结直肠癌和肝癌在内的多种小鼠肿瘤的进展。此外,TMEM87A 缺失还能增强抗肿瘤 T 细胞反应,并增强 PD-1 阻断疗法的治疗效果。TMEM87A 缺失使肿瘤对免疫疗法更敏感
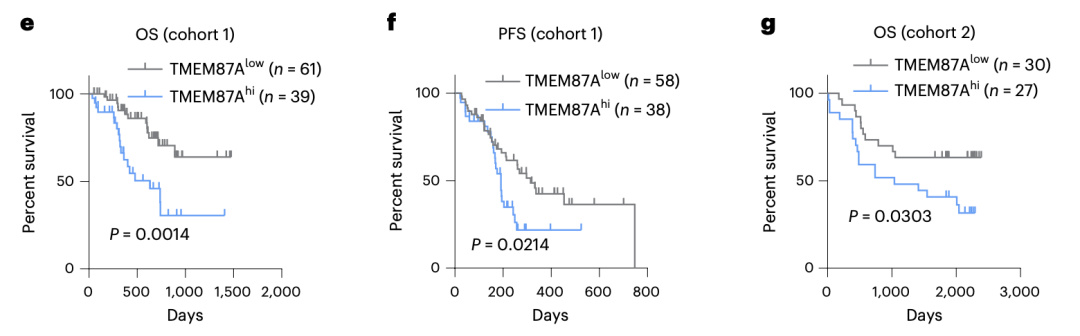
临床分析进一步验证了上述发现——肿瘤组织中 TMEM87A 的表达水平与免疫治疗响应及临床疗效呈负相关。TMEM87A 表达水平高与免疫治疗耐药相关
总的来说,这项研究揭示了 TMEM87A 通过维持高尔基体 pH 稳态以抑制肿瘤铁死亡的作用机制,并表明了靶向抑制 TMEM87A 可能作为增强癌症免疫治疗一种有效策略。![]()
https://www.nature.com/articles/s43018-026-01156-9
为促进前沿研究的传播和交流,我们组建了多个专业交流群,长按下方二维码,即可添加小编微信进群,由于申请人数较多,添加微信时请备注:学校/专业/姓名,如果是PI/教授,还请注明。