千亿美金出口额背后的喜与忧,中国创新药如何从“卖项目”走向“全球化运营”?
发布时间:2026-04-22来源:药事纵横
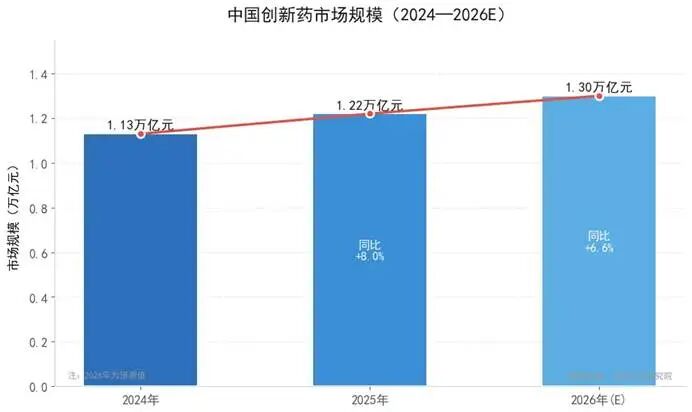
近年来,中国创新药产业在政策导向与研发能力双重驱动下,实现了规模与质量的快速提升。从市场规模看,2024年中国创新药市场规模达1.13万亿元,2025年增长至约1.22万亿元,预计2026年将超过1.3万亿元。从审评审批看,2025年国家药监局共批准上市创新药76个,较2024年大幅增长58.3%,其中国产化学药品和生物制品占比均超过80%。在此背景下,创新药出海已成为衡量产业核心竞争力的重要指标。2025年中国创新药对外授权交易总金额达1356.55亿美元,占全球总额的49%,2026年第一季度对外授权交易总额更是超过600亿美元。然而,在宏观数据持续走高的同时,产业内部正经历着深刻的结构性调整。深入剖析我国创新药出口的现状、面临的困境及应对策略,对产业从规模扩张向高质量国际化发展具有重要现实意义。图1. 中国创新药市场规模一、我国创新药出口的现状
1.1我国创新药类型
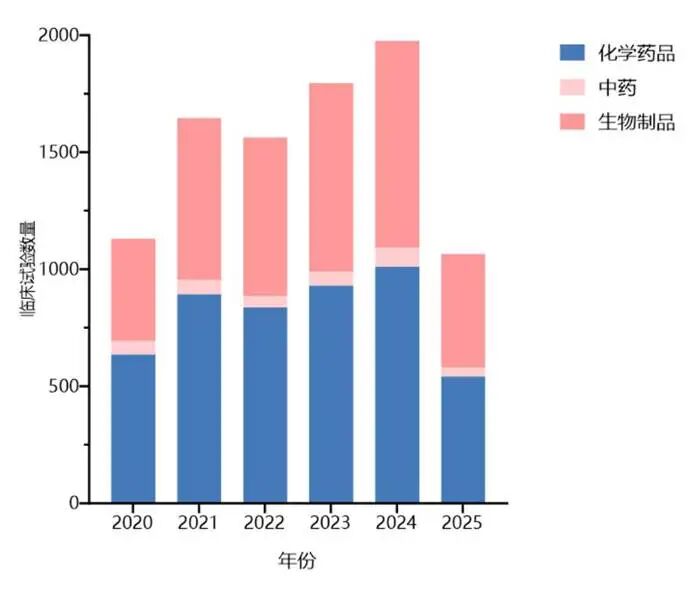
按药品类型划分,化学药品临床试验数量始终位居首位,从2020年的635项增长至2024年的1011项,2025年上半年为542项,保持着50.0%左右的占比。生物制品临床试验数量从2020年的437项持续上升至2024年的886项,涨幅与化学药品持平。相比之下,中药临床试验数量规模相对较小,在2020年至2024年间于48项至80项之间波动。图2. 2020年至2025上半年中国创新药临床试验药品类型分布1.2我国创新药出口现状
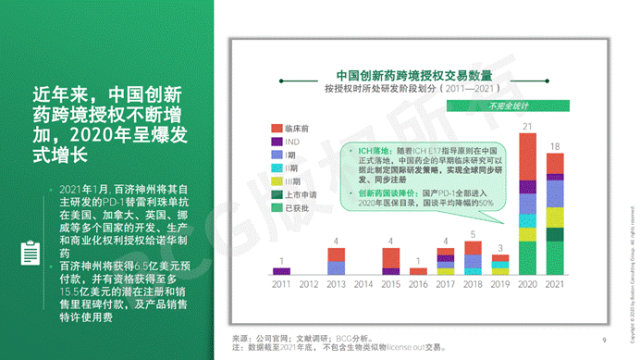
对外授权交易规模呈现跨越式增长。中国创新药对外授权已成为全球医药市场的重要交易来源。2025年,中国创新药交易额占全球总额的49%,对外许可总金额达到美国同期对外许可金额的3.2倍。进入2026年,这一增长势头进一步延续,第一季度交易总额接近2025年全年的一半。从交易结构看,首付款规模显著提升,2026年第一季度首付款总额达33亿美元,同比增长267%,单笔首付款平均额达到0.67亿美元,较2022年提升180%。部分头部企业的单笔交易首付款甚至达到12亿美元量级,反映出海外跨国药企对中国早期创新分子支付意愿的实质性增强。出口产品类型从生物类似药向创新药过渡。我国医药产品出口早期以原料药和仿制药为主,近年来逐步向生物类似药和创新药攀升。以复宏汉霖为例,其自2020年首款生物类似药曲妥珠单抗出海欧盟以来,经过五年拓展,该产品已在全球50多个国家和地区获批。2025年,复宏汉霖全球化增长动能持续释放,全球产品收入达到57.746亿元,同比增长17.0%。值得注意的是,2025年海外产品收入超过2亿元,同比增长翻倍;海外产品利润达0.939亿元。与此同时,创新药出海开始起步,如PD-1单抗斯鲁利单抗已在超过40个国家和地区获批,并通过选择广泛期小细胞肺癌等差异化适应症切入欧盟市场,2025年海外销售额同比增长1327%。截至目前,公司共有10款产品在全球60个国家和地区获批上市,其中7款已在中国获批,4款获得美国FDA批准、4款获得欧盟EC批准,惠及全球超100万患者。图3. 曲妥珠单抗上市情况图4. 复宏汉霖产品全球营收情况前沿技术赛道成为出口主力。在对外授权的靶点和机制方面,抗体药物偶联物、双特异性抗体、细胞与基因治疗等前沿领域构成了当前出海的核心管线。券商机构统计显示,具备全球竞争力的出海型创新药企多集中于ADC、双抗、放射性核素偶联药物等赛道。此外,小核酸药物凭借独特的机制和自主递送平台,也逐渐成为海外授权的新兴热点。这些技术赛道的产品在海外临床研究中展现出替代现有疗法的潜力,是吸引海外大额授权交易的基础。图5. 中国创新要跨境交易数量出海模式呈现多元化演进。当前中国创新药出海已逐步告别单一的权益转让模式,进入以价值共创为核心的新阶段。企业不再单纯将海外授权作为维持现金流的融资替代手段,而是转向深度的战略合作。例如,部分企业在出海过程中调整合作策略,将部分区域的权益从当地药企转移至具备更强商业化能力的跨国药企,同时保留部分核心市场的自主拓展权益,形成了自主商业化与对外授权并行的格局。不乏高交易金额产品。2021年中国创新药跨境授权交易中存在多个高交易金额项目,例如维迪西妥单抗RC48、替雷利珠单抗、代谢偶创疗法等,交易金额从5亿到26亿美元不等。其中维迪西妥单抗RC48交易总额达26亿美元,为最高值。这些交易涉及荣昌生物、百济神州、诺诚健华等中国药企,以及Seagen、Novartis、Bogen等国际药企。值得注意的是,具有战略意义的高竞争力产品、临床进度接近后期且拥有强大海外背景团队的项目更易获得高额交易。同时,首付款及里程碑授权费有助于药企扩大现金流,增加研发投入,从而形成正向循环。图6. 中国创新药代表性高交易金额项目二、我国创新药出口面临的困境
2.1商业化变现与前期投入存在错配
尽管对外授权总金额庞大,但实际落袋资金比例较低。创新药海外BD的里程碑付款兑现率随研发阶段递减,临床前阶段约为55%,至临床III期仅剩12%,商业化阶段不足5%。综合来看,中国创新药海外BD的退货率曾高达40%,主要原因在于后续临床数据未达预期或合作方战略调整。即使是已经实现海外销售的成熟产品,其商业化进程也较为缓慢。复宏汉霖的曲妥珠单抗在欧洲上市五年后,2025年海外产品总收入刚突破2亿元,但与其在全球50多个国家的广泛布局形成反差。美国市场数据显示,FDA批准的生物类似药与品牌药物相比,市场份额不足20%,表明突破原研药壁垒的难度依然较大。2.2研发管线同质化导致国际市场竞争力受限
国内创新药研发存在明显的靶点聚集现象,大量资源集中于PD-1/PD-L1、HER2等已充分验证的成熟靶点。全球四款头部PD-(L)1单抗占据了500亿美元的销售收入,而大量中国企业开发的同类产品不仅出海困难,即便在海外获批,也只能局限于鼻咽癌等小众适应症,难以进入主流肿瘤治疗市场。在ADC、细胞治疗等热门新药研发领域,部分国内企业同样面临创新深度不足的问题,缺乏具备全球首创新药潜质的管线,导致在海外授权谈判中难以获得优势地位。2.3国际合规与临床运营能力存在短板
创新药出海需要严格遵守美国FDA、欧洲EMA等监管体系的准入规则,这对企业的临床试验设计和国际多中心研究能力提出了极高要求。目前,除少数头部企业外,大多数创新药企在应对海外复杂监管要求时经验不足。此外,海外市场的医保准入体系与国内存在显著差异,美国等发达国家以商业保险为主,定价机制复杂,企业需要具备专业的海外市场准入和卫生经济学评价能力,而这正是当前国内企业的普遍弱项。2.4复合型人才供给不足
创新药出海是一项高度专业化的系统工程,需要兼具医药专业背景、研发经验、国际监管知识、跨文化谈判能力的BD人才。目前,此类高层次复合型人才多集中于跨国药企或少数头部生物科技公司,流动性极低,相关人才缺口高达80%。人才短缺直接制约了企业项目出海的运营能力,导致部分企业在条款谈判、合作伙伴筛选以及后续项目追踪管理中处于被动地位。2.5地缘政治与供应链安全风险加剧
在国际贸易环境日趋复杂的背景下,创新药出海面临非经济因素的干扰。在关键技术领域,部分国家已对高参数流式细胞仪、特定质谱设备及生物药数据库等实施出口管制。同时,国内在高端生物药反应器、基因编辑工具等核心设备与耗材方面仍存在依赖进口的情况,面临供应链卡脖子的隐患。这些地缘政治风险增加了创新药海外拓展的不确定性。2.6一级市场融资遇冷削弱出海支撑能力
自2021年触顶后,国内创新药一级市场融资持续下行。2025年上半年,国内创新药一级市场融资事件188起,同比下降7.4%;总融资额约15.8亿美元,同比下降约24.5%。部分初创企业融资周期长达20个月以上。国内融资环境的阶段性收紧,迫使部分企业为了短期生存而低价出售有潜力的海外管线,削弱了企业长期参与国际竞争的能力。2.7出海热情高涨有产品未被FDA通过
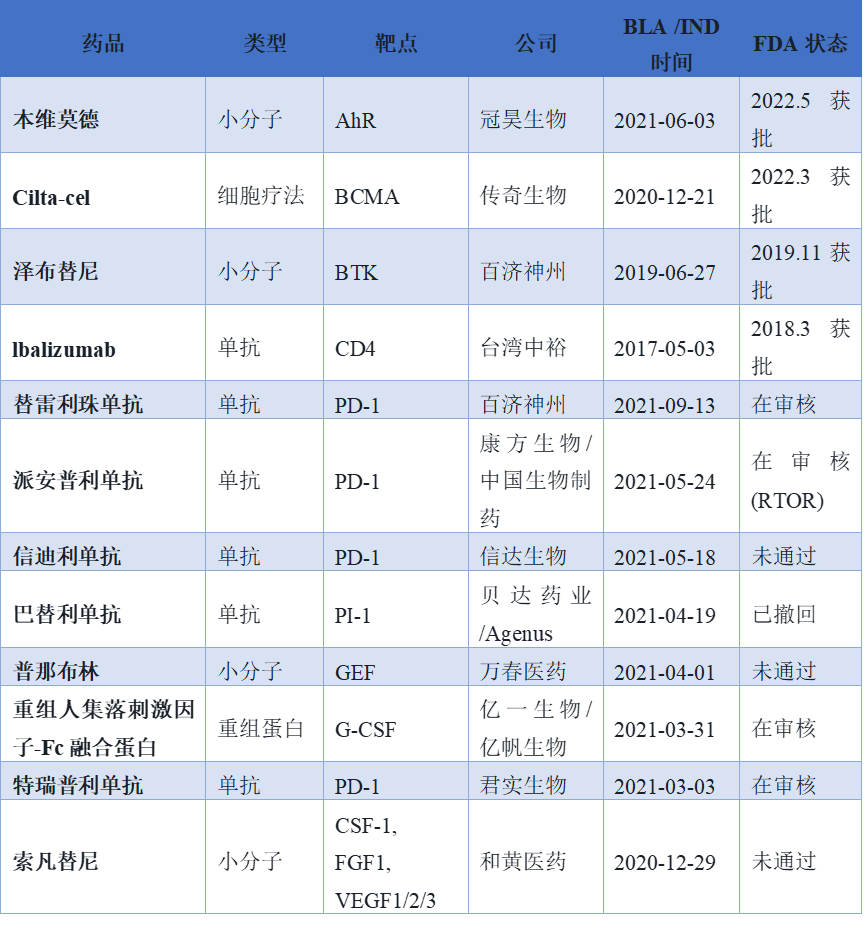
中国出口创新药涵盖小分子、单抗、细胞疗法、重组蛋白等多种类型,靶点分布广泛,包括PD-1、BTK、BCMA等热门靶点。从FDA状态看,本维莫德、Cilta-cel、泽布替尼、Ibalizumab已获批上市,其余8个品种处于在审核或未通过状态。其中,信迪利单抗、普那布林、索凡替尼未通过FDA审批,巴替利单抗已撤回申报。值得注意的是,派安普利单抗以及重组人集落刺激因子-Fc融合蛋白处于在审核状态。三、推动我国创新药出口高质量发展的对策
3.1强化基础研究,提升源头创新能力
改变靶点跟随的研发惯性,聚焦肿瘤、神经退行性疾病、罕见病等重大疾病领域,加大对新靶点、新机制、新结构药物的探索力度。支持创新药研发企业与高校院所、临床机构组建创新联合体,开展扎实的转化医学研究。推动人工智能技术在靶点发现、药物设计、临床试验预测等环节的深度应用,差异化构建具备全球专利布局潜力的研发管线,从源头减少同质化竞争。3.2构建多层次出海路径,提升商业化兑现率
针对不同发展阶段的创新药企,构建差异化的出海路径体系。对于初创期企业,可通过早期研发授权获取资金回流;对于成长期企业,可采用New-Co(新建海外公司)模式,引入海外资本与专业团队共同开发国际市场;对于成熟期企业,应逐步建立自主海外商业化能力。在对外授权协议中,需科学设置里程碑条款,直接挂钩产品临床进展,并嵌入充分的信息披露权,确保交割后能够有效监督项目进展,降低退货风险。3.3完善临床试验与注册合规体系
全面对标国际主流监管机构的审评标准,在药物研发早期即引入国际多中心临床研究(MRCT)设计。充分利用国家药监局突破性治疗药物、附条件批准、优先审评审批等通道,加快临床急需药品上市,为后续出海奠定临床数据基础。同时,企业内部需建立专业的海外注册部门,深入研究FDA、EMA等机构的法规动态,如密切关注FDA在生物类似药临床疗效对比研究方面的政策调整,利用政策红利降低研发成本与注册周期。3.4加快高层次国际化人才培育与引进
将新药研发、国际BD等核心岗位纳入国家级或省级紧缺人才需求目录,加大海外高层次人才团队引进力度。鼓励高校与科研院所开设医药法规、药品国际注册、医药商务拓展等交叉学科,扩大人才基数。支持企业选派具备潜力的研发和商务人员赴欧美知名药企或监管机构开展实训,通过实战积累经验,培育一批具备全球胜任力的专业人才队伍。3.5建立健全出海综合服务平台与联盟机制
依托医药产业集聚区,由政府牵头联合行业协会、投资机构,构建一站式出海服务平台,提供海外法规咨询、知识产权布局、本地化注册代理等服务。支持组建区域性或全国性的生物医药出海联盟,整合上下游资源,实现信息共享与风险共担。定期举办高规格国际医药创新峰会,畅通本土药企与跨国药企的常态化对接渠道,降低交易信息壁垒。3.6积极应对地缘政治风险,保障供应链安全
针对高端生物反应器、核心耗材及底层技术面临的卡脖子风险,引导产业链上下游开展协同攻关,提升关键设备的国产化率。建立医药领域关键技术与设备的战略储备机制。在出海目标市场的选择上,采取多元化策略,在巩固欧美成熟市场的同时,积极拓展东南亚、中东、拉美等新兴市场,分散地缘政治带来的单一市场风险。3.7优化国内支付环境,形成内外市场良性互动
国内市场是创新药出海的坚实后方。应进一步落实健全药品价格形成机制的若干意见,完善以临床价值为核心的分层首发定价机制,使高水平创新药在上市初期获得与高投入相匹配的价格回报。加快构建基本医保保基本、商业健康险保创新的多层次支付体系,扩大商保对创新药的覆盖规模。通过国内市场利润反哺研发,使企业具备更充裕的资金和时间窗口去筛选优质的海外合作伙伴,避免因短期现金流压力贱卖核心资产。四、结语
总的来说,中国创新药出口正处于从规模扩张向质量提升转型的关键期。对外授权交易额的屡创新高,证实了国内研发体系在全球医药产业链中地位的跃升;而高退货率、商业化变现缓慢以及同质化竞争等现实困境,则揭示了产业在核心创新力与国际运营能力上的不足。未来,中国创新药的全球化进程无法仅依靠授权交易数字的堆砌,而是需要回归创新本质,在底层机制探索、临床试验质量、跨国合规运营以及供应链安全等维度构建系统性壁垒。随着国内政策支持链条的进一步完善和企业国际化运营能力的持续锤炼,中国创新药有望在全球化市场竞争中实现从产品输出到技术引领的实质性跨越。[2] 黄佳欣,姚泽坤,李惟妙,等.2020-2025上半年中国创新药临床试验发展趋势回顾性分析[J/OL].医药导报,1-10[2026-04-20].https://link.cnki.net/urlid/42.1293.R.20251225.0910.002.
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。