停摆管线,默沙东如何救回?


4月21日,FDA批准默沙东(Merck & Co.)每日一次口服双药疗法Idvynso(doravirine/islatravir)上市,适用于已实现病毒学抑制、抗逆转录病毒治疗方案稳定且无耐药史的HIV-1成人感染者。该疗法不仅是全球首个非整合酶抑制剂、不含替诺福韦的每日一次单片双药方案,更是一场迟来的“复出”。就在三年前,这款药的核心成分Islatravir,曾因安全性问题被“宣告出局”,如今又何拿下FDA批文?

剂量“做减法”赢回FDA
倘若单看Idvynso疗法获批的临床数据,似乎是一场顺理成章的胜利,但是值得深挖的是该药身后的“惊险一跃”,只因Islatravir的研发历程堪称一部小分子药物的逆袭剧本。
时间回到2021年12月,默沙东因在临床试验中发现Islatravir(每日0.75 mg)导致CD4+T细胞和总淋巴细胞(HIV患者免疫力的重要参考指标)下降,不得不暂停多项试验。默沙东甚至搁置了与吉利德合作的每周一次口服联合方案,这在当时,几乎称得上是对默沙东HIV管线的毁灭性打击。然而,默沙东并没有放弃Islatravir,经过数据复盘和建模分析,公司的科学家们确定,该药物在淋巴细胞中积累,高浓度会导致细胞凋亡,或细胞死亡,淋巴细胞减少呈现剂量依赖性。
默沙东随即展开了“剂量优化”攻坚战,将Islatravir每日剂量从0.75 mg大幅下调至0.25 mg,并启动新的III期临床试验。在一项剂量范围的研究中,0.25 mg每日一次的给药方案对总淋巴细胞和CD4+T细胞计数的影响与标准抗逆转录病毒疗法相当。两项III期试验在第48周的结果给出了强有力的答案:在MK-8591A-052试验中,Idvynso组仅1%病毒载量反弹至≥50拷贝/mL,与Biktarvy组完全持平。截至去年年底,0.25 mg剂量已在多项研究中被确认为最低有效剂量且不影响淋巴细胞水平。这一“减量不减效”的剂量优化策略,使Islatravir从“濒死分子”重新被推上审批跑道。

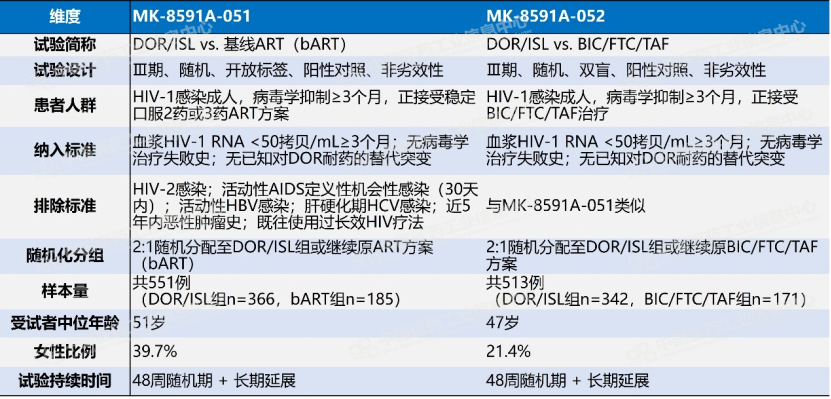
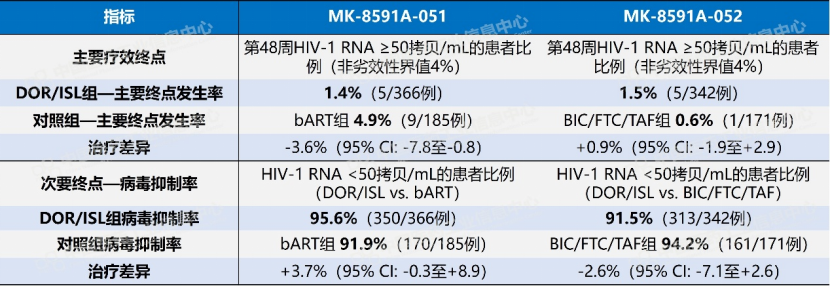
数据来源:Pharma ONE药物研发大数据平台-全球临床试验板块,中国医药工业信息中心
点击“阅读原文”获取更多数据
绕开“整合酶帝国”:Idvynso在切谁的蛋糕?
当前HIV治疗市场,整合酶抑制剂已筑起了一座难以撼动的帝国。吉利德的三药方案必妥维(比克替拉韦+恩曲他滨+丙酚替诺福韦)以143.34亿美元的销售额稳居全球处方量最大的抗艾药物,GSK旗下ViiV的双药方案多伟托(多替拉韦+拉米夫定)以35.08亿美元紧随其后,两者瓜分了全球双药疗法的半壁江山。
国内市场,根据PDB数据库显示,2025年吉利德国内全渠道销售额占42%,ViiV约占21%,整合酶抑制剂赛道几乎被外资垄断,国产创新药仅有江苏艾迪的艾诺米替片和河南真实生物的阿兹夫定片等零星突围。Idvynso的获批,开辟了一条截然不同的赛道。

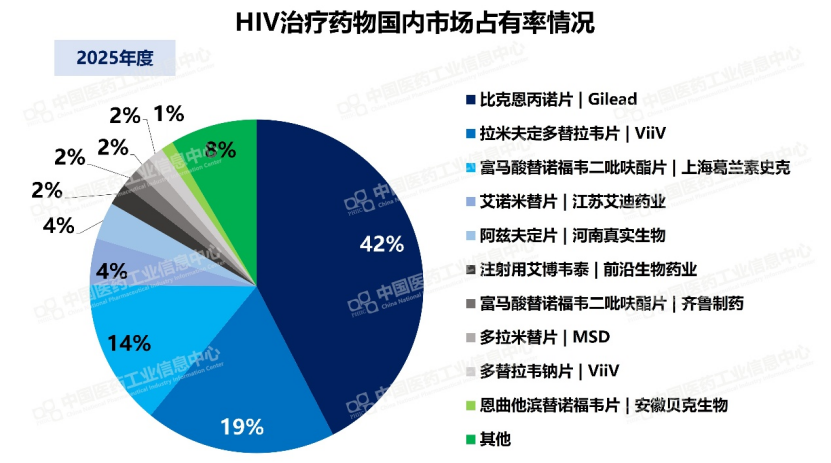
数据来源:PDB药物综合数据库-国内全渠道放大板块,中国医药工业信息中心
从临床定位来看,Idvynso的差异化竞争力体现在两个维度。第一是机制替代性。随着整合酶抑制剂类药物的广泛使用,耐药性正在缓慢积累,部分患者还面临体重增加、肾功能影响等代谢负担。Idvynso作为非核苷类逆转录酶抑制剂/核苷类似物的双药组合,恰好针对这一临床痛点。相关行业分析师指出,该产品到2033年有望在七大主要市场实现约18亿美元的峰值销售额。与此同时,吉利德的Bictegravir/Lenacapavir(BIC/LEN)双药方案已进入III期临床,ViiV的广谱中和抗体Lotivibart(N6LS)联合卡博特韦也在推进每4个月注射一次的长效方案,双药赛道竞争将持续升温。
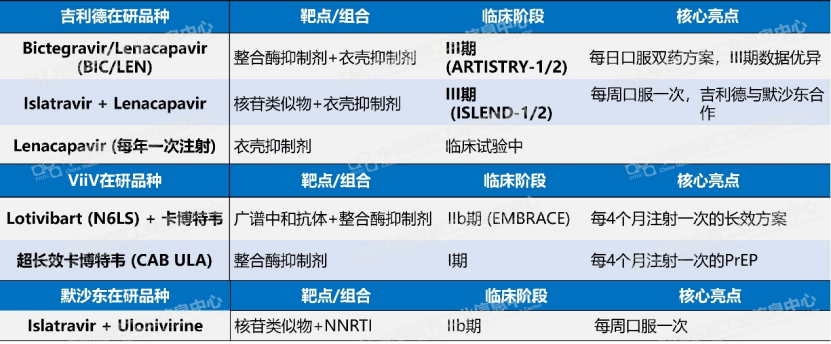
数据来源:Pharma ONE药物研发大数据平台-全球药物研发板块,中国医药工业信息中心
点击“阅读原文”获取更多数据
第二是老龄化适配。随着HIV感染者带病生存时间延长,合并症管理需求日益突出。不含替诺福韦的双药方案在长期用药安全性上具备天然优势。在国内,艾迪药业的ACC017作为首个进入III期临床的国产整合酶抑制剂创新药,同样瞄准了这一未被满足的临床需求,国产替代窗口正在打开。
不过,这并不意味着Idvynso能轻易撼动现有格局,因为必妥维的医生处方惯性极强。当然,默沙东自身也在推进Islatravir联合Ulonivirine的每周口服方案,长效化趋势下的竞争维度正在重构。Idvynso当下的战场,是在整合酶抑制剂治疗失败的“替代市场”和追求简化治疗方案的“转换市场”中精准卡位。同时,它也为国内正在追赶的国产创新药们提供了可参照的差异化路径。
从每日一片到每周一片的阶梯式布局
Idvynso的获批并不是默沙东在HIV领域的终点。细看其管线布局,就会发现从每日口服、每周口服、每月口服到长效注射的“阶梯式给药矩阵”正在成型,而Islatravir是该矩阵的基石。
在与吉利德的合作中,双方正在推进一项每周一次口服的Islatravir联合Lenacapavir(ISL/LEN)方案,目前已进入III期临床开发。两项III期试验的完整数据预计将于2026年上半年公布,若顺利,该产品有望在2027年上市,届时HIV治疗将从“每日服药”迈向“每周服药”,极大降低患者的服药负担和用药依从性压力。默沙东还在推进“每月口服”的HIV暴露前预防候选药物MK-8527的III期临床试验。这款尚未获批的长效PrEP口服药已引发全球177家组织的联合公开信,要求默沙东承诺将其纳入针对中低收入国家的可及性计划,由此可见MK-8527的潜在市场影响力。
从Idvynso的每日一次,到ISL/LEN的每周一次,再到MK-8527的每月一次,默沙东正沿着“给药频率递减”的阶梯稳步推进,每一步用的是同一核心分子在不同适应症、不同用药场景下的多维度延展。
Idvynso的获批只是一个开始。当默沙东的阶梯式产品矩阵全面铺开后,HIV治疗领域的竞争格局是否会迎来一场新的洗牌?



