2026年Q1:14款创新药,12款中国造!


2026年一季度,国家药品监督管理局(NMPA)批准1类新药14个(按通用名计),其中国产新药12个,进口新药2个。从药物类型来看,涉及7款化学药品和7款生物制品。
Pharma ONE药物研发大数据平台显示,2018–2025年间,NMPA批准的1类创新药总体呈波动上升态势,2018-2021年小幅增长,2022年略有回落,2023-2025年再度攀升并刷新峰值,今年一季度获批14个,单季数量已接近2024年全年的三分之一,但仍略少于2025全年的四分之一,有望延续强劲的增长势头,进一步彰显我国创新药研发与审批的蓬勃活力。
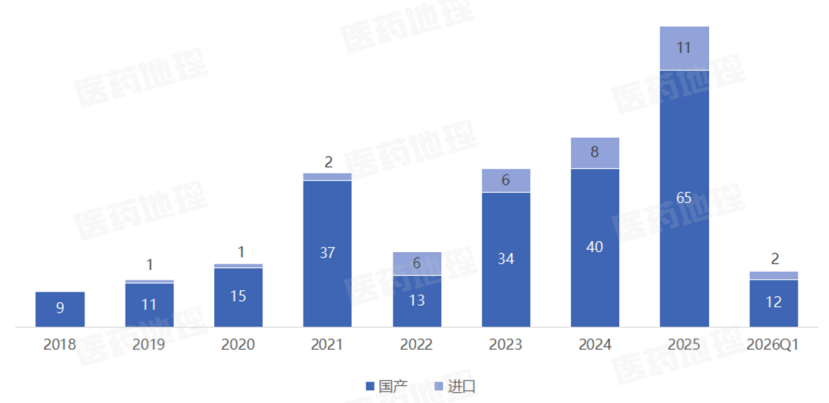
2018-2026Q1国内获批的1类创新药数量
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
从治疗领域看,2026一季度年NMPA批准的1类创新药仍以抗肿瘤药为主,共3款,占比高达22%,内分泌及代谢调节用药及抗感染药紧随其后,各有2款,占比均为15%。其余治疗大类(包括血液和造血系统系统、呼吸系统、心血管系统等)各占1款,呈现出多元化的布局趋势。值得注意的是,在神经等机制更复杂、转化路径不确定性更高的领域,一季度暂未有新药获批。随着脑科学、基因治疗等前沿技术的持续推进,这些领域有望在未来迎来更多创新突破。
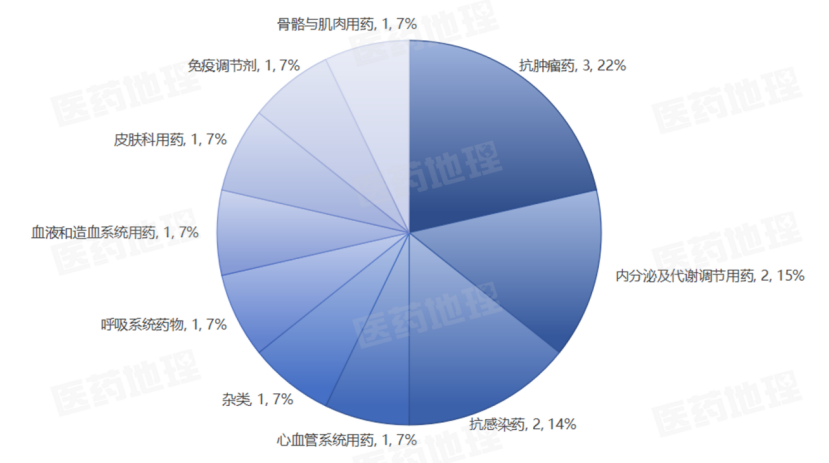
2026Q1国内获批的1类创新药治疗大类分布
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心
点击“阅读原文”获取更多数据
从审评角度看,通过优先审评、突破性疗法、以及特殊审评的新药共有6款,占比43%,涉及4款化学药品及2款生物制品。其中,浙江杭煜制药有限公司的硫酸索西美雷塞片、正大天晴药业集团股份有限公司的罗伐昔替尼片及华辉安健(北京)生物科技有限公司的立贝韦塔单抗注射液获得了CDE授予的突破性疗法。这体现了监管层面对于真正具有临床价值品种的精准扶持,不仅显著缩短了创新药的上市周期,也激励更多差异化创新成果加速落地。
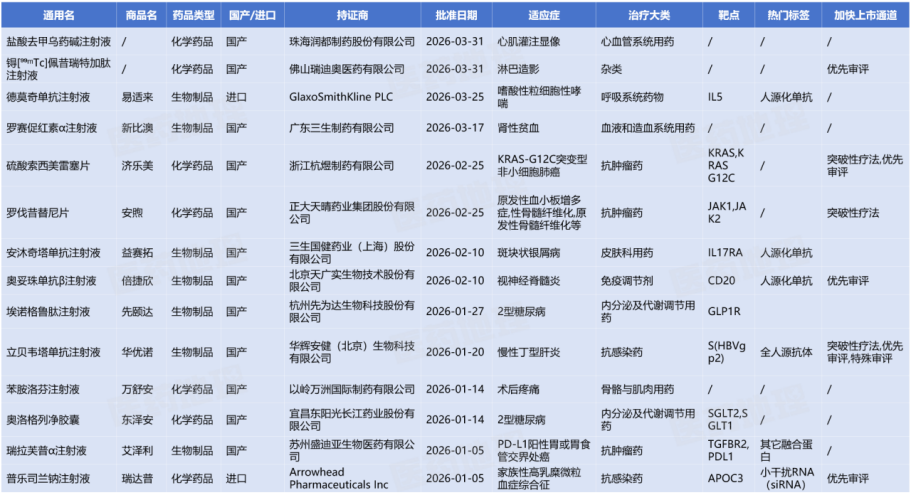
2026Q1国内获批的1类创新药一览
来源:Pharma ONE药物研发大数据平台,中国医药工业信息中心

埃诺格鲁肽注射液是由先为达生物自主研发的全球首个获批的cAMP偏向型GLP-1受体激动剂,与非偏向型的GLP-1受体激动剂不同,埃诺格鲁肽偏向性激活cAMP信号通路,同时最小化β-arrestin的募集,这种信号偏向限制了受体的脱敏和下调,使受体更多的留存在细胞表面,并维持治疗性信号传导,偏向型的独特机制是其提升临床疗效与改善代谢获益的关键因素之一。临床研究证明埃诺格鲁肽注射液在降糖、降低体重和改善代谢指标等方面具有全面综合获益,52周持续有效,整体安全性和耐受性良好。
立贝韦塔单抗是华辉安健公司自主开发的全球首个乙肝/丁肝病毒PreS1单抗药物同时也是中国首个丁肝治疗药物。其主要作用机制为,通过特异性结合乙肝/丁肝病毒表面的PreS1区域,阻断乙肝/丁肝病毒和其受体NTCP的结合从而阻止病毒感染或再感染肝细胞。临床研究结果显示,立贝韦塔单抗在病毒学和生化的复合终点应答率、病毒学抑制、丙氨酸氨基转移酶(ALT)复常及肝脏硬度改善等核心指标上,均显著优于对照组,并且具备良好的耐受性和优异的安全性。治疗48周时,其复合终点应答率达44.1%,HDV病毒学抑制应答率达60%,ALT复常比例达70%,可显著且持续改善肝脏硬度。

普乐司兰钠注射液是全球首个靶向APOC3 mRNA的小干扰RNA(siRNA)药物,用于降低家族性乳糜微粒血症综合征(FCS)成人患者的甘油三酯水平,可较基线降低80%的空腹甘油三酯,并将急性胰腺炎发生风险降低80%。其给药频率仅为一年四次,显著改善了患者依从性,打破了FCS领域“无药可控”的困局。此外,该药已于2025年12月获得美国FDA针对严重高甘油三酯血症(sHTG)的突破性疗法认定,未来有望惠及更广泛的患者群体。
德莫奇单抗注射液是中国首款且目前唯一一款用于治疗嗜酸性表型重度哮喘的超长效生物制剂,已获批用于成人和12岁及以上青少年的维持治疗。该药每年仅需给药两次,可持续控制2型炎症,显著降低哮喘急性发作风险。基于SWIFT-1和SWIFT-2两项III期临床试验,德莫奇单抗治疗52周可使年哮喘急性发作率分别降低58%和48%;在中国患者亚组中,降幅更达85%。此外,该药还获批用于慢性鼻窦炎伴鼻息肉的成人患者,为2型炎症相关疾病提供了创新的超长效治疗选择。



