Science:颜宁/黄隽豪/闫创业等揭示共价修饰、水分子与阳离子配位介导糖质高级组装的新模式


编辑丨王多鱼
排版丨水成文
糖质(glycan)是生命四大基本生物大分子(核酸、蛋白质、糖质、脂质)之一,在细胞识别、信号转导、免疫调控和结构支持等多种生理过程中发挥关键作用。历史上,糖质曾常被统称为“碳水化合物”(carbohydrates),这一名称源于其经典化学表达形式Cx(H2O)n;尽管糖质研究可追溯至 19 世纪,但与蛋白质和核酸相比,糖质科学的发展长期相对滞后。其根本原因在于:糖质太过复杂,一直缺乏有效的研究手段。糖质的生物合成并不像 DNA、RNA、蛋白质一样依赖模板,因此缺乏从基因组到糖质序列的对应关系;而高度多样的单糖组成、复杂的糖苷键连接方式和显著的空间构象异质性,限制了对于复杂糖质复合物的高分辨率三维结构解析。这种结构信息的长期缺失,也在很大程度上阻碍了人类对糖质在多种生理和病理过程中作用机制的深入理解。
2026 年 4 月 23 日,颜宁、黄隽豪、闫创业等在国际顶尖学术期刊 Science 上发表了题为:Structural N- and O-glycans revealed by high-resolution cryo-EM analysis of tubular mastigonemes 的研究论文。
研究团队以金藻(Ochromonas danica)的管状纤绒毛(T-mastigoneme)糖质-蛋白质复合物为研究对象,建立了整合高分辨率冷冻电镜、糖蛋白质组学与人工智能建模的综合研究策略,获得了整体糖质分辨率约 2 Å(即 0.2 纳米),核心局部最高达 1.8 Å 的超高分辨率三维电镜密度图,进一步将天然糖质复合物的研究推进至近原子分辨率层面。
这一分辨率水平使对天然糖质的直接可视化成为可能,不仅支持多种单糖类型的精确识别,也为乙酰化、甲基化和硫酸化等多种共价修饰的判定提供了明确的结构依据。在此基础上,研究者还通过整合结构生物学研究与靶向质谱技术,发现了一类基于“AND” 基序的新型非经典 N-糖基化类型,并借助结构聚类搜索揭示了该基序在多种高致病性物种中的进化保守性。与此同时,由颜宁实验室开发的 AI 自动建模工具 EModelG 显著提升了糖质结构自动建模的效率,推动糖质结构解析从依赖间接片段信息推断向高精度直接建模转变,也为复杂天然糖质的大规模结构研究提供了方法学支撑。

进一步结构分析表明,不同类型的 N-糖质在该体系中承担着彼此明确区分、各不相同的结构功能。研究系统提出了三种糖质介导大分子组装的功能模式:
其一,“糖质缝合”(glycostitch)通过非经典 AND(Aln-Asa-Asp)基序糖链形成规则螺旋样构象,稳定重复单元内部的亚基界面;
其二,“糖质桥”(glycobridge)主要由高甘露糖型结构介导,跨越重复单元形成长程相互作用,并表现出一定的跨物种保守性;
其三,“糖质岛”(glyco-islet)以簇状方式分布于复合物表面,通过增加表面积和亲水性提升整体稳定性与可溶性。这些发现突破了将糖质仅视为蛋白质附属修饰的传统认识,表明糖质本身可以直接作为驱动生物大分子折叠与高级组装的关键结构单元。
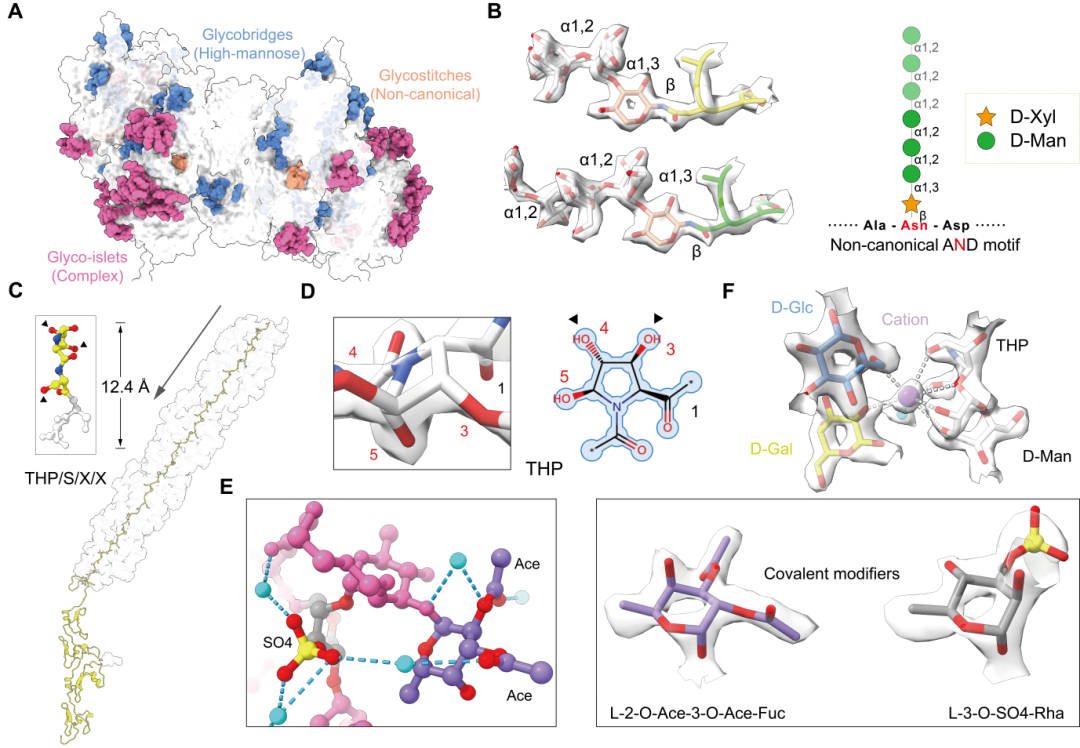
图1. 高分辨率冷冻电镜解析揭示管状纤绒毛中结构 N-和 O-糖质
在 O-糖质结构方面,研究团队进一步解析了基于 PSXX 四肽重复形成的高级糖质纤维。结构显示,3,4,5-三羟基脯氨酸(THP)和丝氨酸位点被致密糖基化,形成规则排列的表面“糖刺”样突起,并共同构建出稳定的糖质纤维骨架。研究首次在该体系中鉴定出罕见的 THP 修饰,并精确揭示了由八种单糖及多种共价修饰共同构成的复杂 O-糖质折叠形式。更为重要的是,高分辨率密度图还揭示出广泛存在的有序水分子网络和多价阳离子配位中心。这些此前难以被直接观测的结构因素,通过氢键网络和配位作用显著增强了糖质之间的相互作用。其中,金属阳离子可介导跨越重复单元的八配位网络,增强糖质螺旋核心的机械刚性,并伴随特征性的甘露糖“扭船式”构象翻转,以实现局部能量补偿,为理解复杂糖质装配体稳定性的物理化学基础提供了直接实验依据。
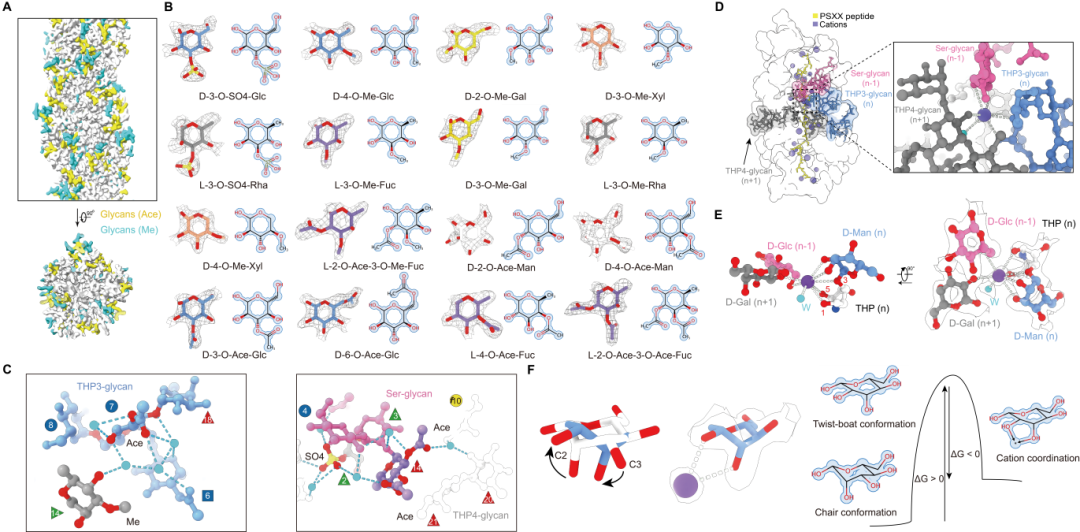
图2. 共价修饰、水分子以及金属离子在糖质螺旋组装中的结构作用
综上,该研究实现了对天然糖质从化学组成到空间构象的直接解析,提出了一系列新型糖质组装元件,例如“糖质缝合”(glycostitch)、“糖质桥”(glycobridge)和“糖质岛”(glyco-islet),系统揭示了糖质在生物大分子高级组装中的结构性作用,为复杂糖质高级结构的发现、鉴定与工程化利用提供了新的方法学框架,标志着糖质结构生物学正进入原子分辨率解析的新阶段。
深圳医学科学院创始院长、深圳湾实验室主任颜宁,清华大学生命学院黄隽豪博士、闫创业副教授为论文共同通讯作者。黄隽豪、水木学者陶慧、陈晟为论文共同第一作者。科研助理崔亚华、博士生徐艺然为研究工作做出了重要贡献。深圳医学科学院生物结构解析平台、高性能计算平台提供了电镜数据采集和计算支撑。实验的质谱鉴定工作得到了清华大学蛋白质化学与组学平台、深圳医学科学院人类免疫学研究所盛心磊研究员的支持。该研究得到了国家自然科学基金“破译生命的糖质密码”重大研究计划,国家自然科学基金青年学生基础研究项目,北京生物结构前沿研究中心与清华-北大生命科学联合中心的经费支持。同时,特别感谢鹏瑞基金会捐赠的“迈瑞教授”经费对颜宁研究工作给予的支持。
该研究最初于 2026 年 1 月 28 日发布在浪淘沙预印本平台(Langtaosha.org.cn)【1】,第一时间通过预印本平台向全球公开,供大家研读、讨论与交流,也为后续研究提供了重要参考。目前,发布在浪淘沙预印本平台上的文章已逐步被 Google Scholar、ResearchGate 等主流学术平台收录,学术影响力持续扩大。该平台始终致力于打造开放、高效、规范的学术交流环境,为全球研究者提供成果快速发布、广泛传播与长期存证的服务。
该研究中所报道解析的糖纤维结构及其对应的冷冻电镜密度图目前已上传至 CryoSeek数据库(Cryoseek.org.cn;结构和电镜密度图详见【2、3】)。CryoSeek 数据库是由颜宁团队依托深圳医学科学院建立,系统收录了以糖质为代表的“生命暗物质”的结构与鉴定成果,并提供在线服务,从而更好地支持糖质等相关结构数据的管理与共享,服务于科研界。CryoSeek 数据库以及高通量 CryoSeek 结构测定技术体系的相关研究成果已发布于浪淘沙预印本平台【4】。
论文链接:
https://www.science.org/doi/10.1126/science.aef4958
参考文献:
1.
2. https://www.cryoseek.org.cn/home/maps/20260421173015A321/
3. https://www.cryoseek.org.cn/home/maps/20260421172519A305/
4. https://langtaosha.org.cn/lts/en/preprint/view/20




点在看,传递你的品味




