拜耳两款“1类”新药,在国内迎来“双突破”!

4月24日,国家药品监督管理局药品审评中心(CDE)官网公示,拜耳的在研抗凝新药BAY 2433334片上市申请拟纳入优先审评,拟用于降低缺血性卒中或短暂性脑缺血发作(TIA)成人患者的卒中(复发)风险,不包含心源性栓塞型卒中患者。
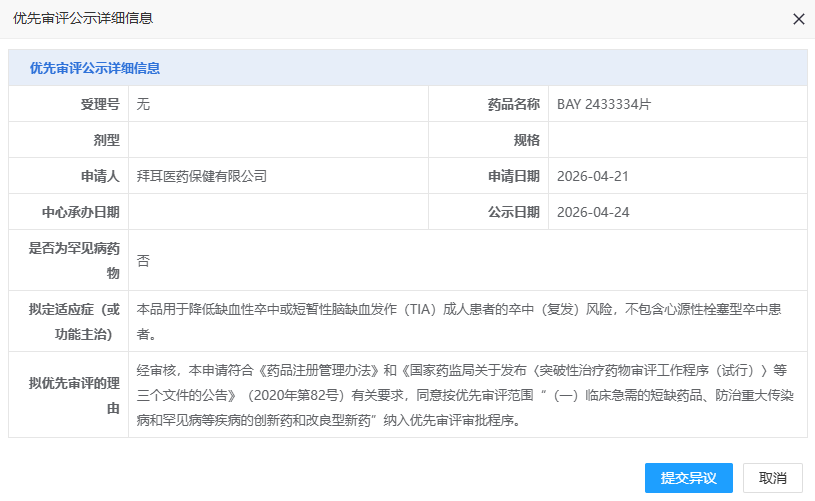
截图来源:CDE官网
此前不久(4月21日),拜耳另一款1类新药塞伐艾替尼片已正式获得NMPA批准,用于治疗存在HER2(ERBB2)激活突变且既往接受过至少一种系统治疗的不可切除的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者。一月之内,拜耳在心血管和肿瘤两大核心治疗领域的创新管线在国内接连取得关键进展。
01
重磅抗凝1类新药,拜耳加速在国内上市
此次拟纳入优先审评的BAY 2433334,是拜耳公司开发的一款在研的每日一次口服FXIa因子抑制剂。FXIa是内源性凝血途径中的关键蛋白酶,被认为在病理性血栓形成中扮演重要角色,但对生理性止血影响较小。因此,选择性抑制FXIa有望在有效预防血栓的同时,显著降低传统抗凝药带来的大出血风险,是新一代抗凝药物研发的前沿靶点。
摩熵医药数据显示,该药于2019年11月首次提交临床试验申请,次年即2020年成功获批开展临床试验。同年9月,该药物推进至Ⅱ期临床试验阶段,针对缺血性卒中展开研究。至2023年,其在卒中及血栓栓塞相关适应症方面进入Ⅲ期临床试验。
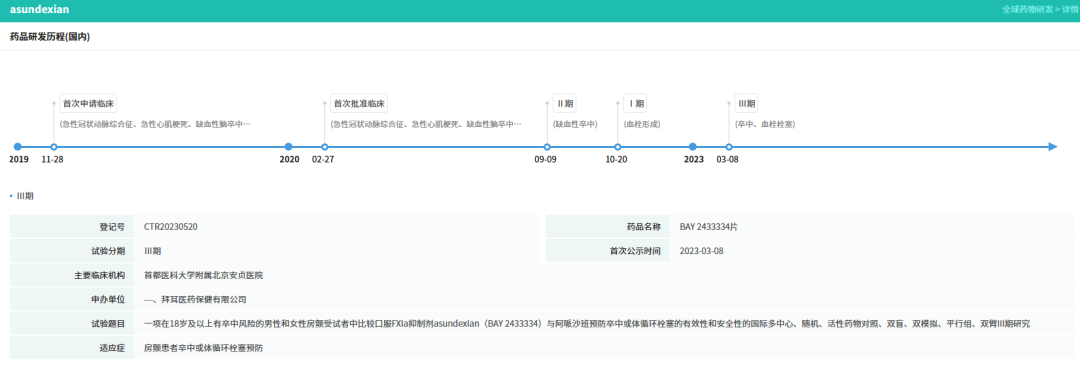
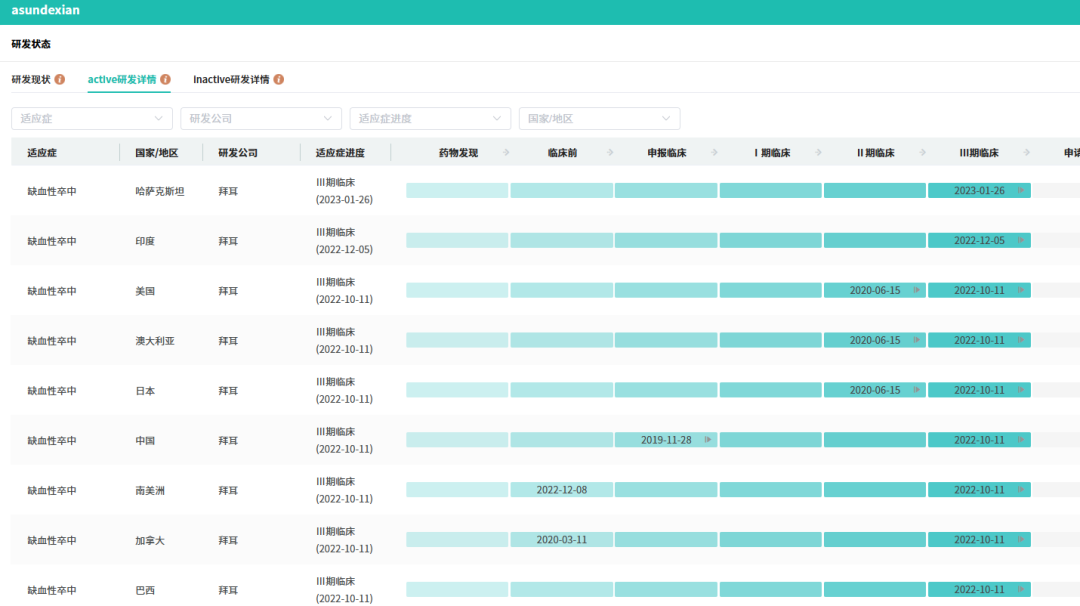
目前,全球范围内尚无FXI/FXIa抑制剂获批上市,口服小分子制剂因给药便利性,在卒中预防等需长期用药的场景中更具优势,成为研发竞争焦点。
拜耳的BAY 2433334是此赛道进展最快的候选药物之一,其III期成功是全球抗凝治疗领域的一个重要里程碑。此次在华获得优先审评资格,将大幅加速其在中国这个卒中高负担国家的上市进程,为临床提供潜在的全新治疗选择。
02
攻坚HER2突变肺癌,国产上市迎来第2款口服药
就在4月21日,NMPA官网显示,拜耳其口服靶向药塞伐艾替尼片已获批上市,用于治疗存在HER2激活突变且既往接受过至少一种系统治疗的不可切除局部晚期或转移性NSCLC成人患者。该药是一种口服、高选择性酪氨酸激酶抑制剂(TKI),可有效抑制EGFR及HER2突变。
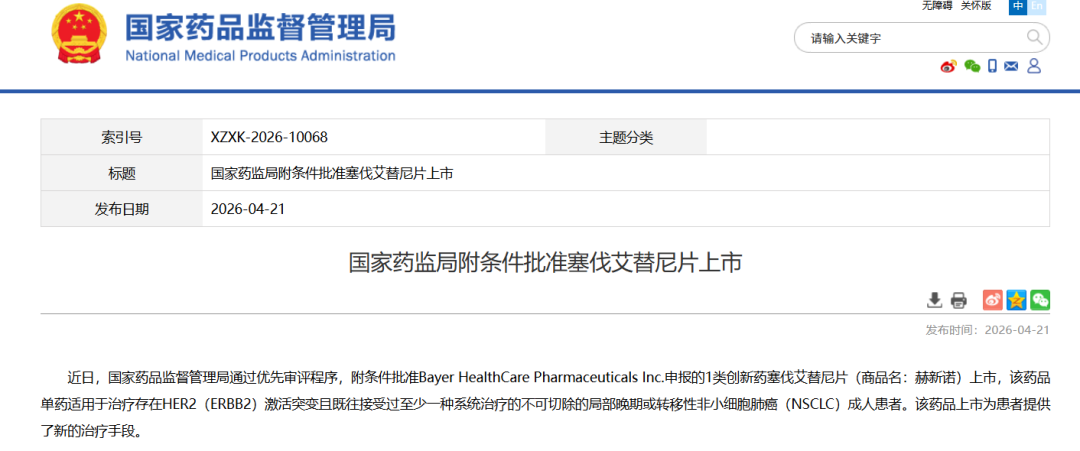
截图来源:NMPA官网
此次获批主要依托于开放标签、多中心的I/II期SOHO - 01研究所取得的积极数据。该研究聚焦于既往接受过治疗的HER2突变晚期非小细胞肺癌(NSCLC)患者群体。研究结果显示,在未接受过HER2靶向抗体药物偶联物(ADC)治疗的患者中,客观缓解率(ORR)高达64%,中位缓解持续时间(DoR)达9.2个月。即便对于既往接受过HER2 - ADC治疗的患者,ORR也达到了38%,充分彰显了其在后线治疗领域的良好潜力。该药已于2025年11月在美国率先获批,此次在华上市实现了快速接轨。

截图来源:全球药物研发数据库(查数据.找摩熵)
在塞伐艾替尼获批前,国内已有3款针对HER2突变NSCLC的靶向疗法上市,包括:恒瑞医药的瑞康曲妥珠单抗注射剂;第一三共/阿斯利康的德曲妥珠单抗注射剂;勃林格殷格翰/中国生物制药的宗艾替尼口服片剂。此次塞伐艾替尼获批,为国内第4款HER2突变NSCLC靶向疗法,同时也是第2款口服靶向药。该药的上市,为临床医生和患者,特别是需要长期口服治疗或对注射剂不耐受的患者,提供了新的重要选择,也使得该细分市场的竞争格局更为激烈。
拜耳在短时间内于中国市场接连传出审评与获批的重磅消息,凸显了其创新管线的厚度与中国市场的高度协同。BAY 2433334作为潜在的重磅抗凝新药,其审评进程提速,预示着我国卒中二级预防领域可能即将迎来全新机制的药物,有望重塑治疗标准。而塞伐艾替尼的快速获批,则直接丰富了HER2突变NSCLC的治疗版图,加剧了市场竞争,最终惠及患者。
随着这两款产品陆续进入商业化阶段,其未来的市场定位、医保准入策略以及真实世界表现,将决定它们能否在各自拥挤且快速发展的赛道中脱颖而出。
END
本文为原创文章,转载请留言获取授权
近期更多摩熵咨询最新报告
识别下方二维码领取

联系我们,体验摩熵医药更多专业服务 | ||||
会议 合作 | 报告 定制 | 数据库 咨询 | 数据 定制 | 媒体 合作 |