Cell重磅:双重CRISPR筛选,全面揭示HIV的“帮凶”与“克星”,发现全新抗艾滋病武器


撰文丨王聪
编辑丨王多鱼
排版丨水成文
艾滋病(AIDS)的元凶——人类免疫缺陷病毒(HIV),之所以难以根治,是因为它极其擅长“劫持”人体免疫细胞(主要是CD4+ T细胞)进行复制和传播。长久以来,科学家们一直在寻找细胞中哪些蛋白质是 HIV 的“帮凶”(促病毒因子),哪些又是“克星”(抗病毒因子)。找到它们,就可能找到阻断 HIV 感染的新靶点。
2026 年 4 月 20 日,Gladstone 研究所的研究人员在国际顶尖学术期刊 Cell 上发表了题为;Systematic discovery of pro- and anti-HIV host factors in primary human CD4+ T cells 的研究论文。
该研究首次在人类原代 CD4+ T 细胞中,利用全基因组 CRISPR 激活筛选和敲除筛选,绘制出了一幅前所未有的 HIV-宿主相互作用全景图,并发现了多个全新的强效抗病毒因子和促病毒因子,其中强效抗病毒因子 PPID 被证明通过 HIV 衣壳结合并减少其核输入。这些发现为开发艾滋病治疗新策略打开了大门。

告别大海捞针—— CRISPR 筛选的力量
过去的相关研究多依赖于永生化细胞系,与人体内真实的 T 细胞环境相差甚远。而原代 T 细胞难以进行大规模基因操作和高效 HIV 感染,这成为了研究的瓶颈。
在这项最新研就在,研究团队攻克了这些技术难题,建立了一个高效的筛选平台。他们运用了两种基于 CRISPR 的筛选技术——
CRISPR 敲除(CRISPRn):通过 CRISPR 基因敲除,让特定基因失活,进而观察 HIV 病毒感染是变容易了还是变难了。如果感染变难,说明这个基因可能是 HIV 的“帮凶”;反之,则可能是“克星”。
CRISPR 激活(CRISPRa):通过 CRISPR 转录激活,让特定基因过表达,进而观察其对 HIV 感染的影响。这尤其有助于发现那些在正常细胞中表达量不高、但一旦过量表达就能强力抑制 HIV 的“隐藏克星”。
研究团队用带有绿色荧光蛋白(GFP)标记的 HIV 病毒感染经过 CRISPR-Cas9(用于 CRISPRn 筛选)或 CRISPR-dCas9(用于 CRISPRa 筛选)转染的 T 细胞,然后通过流式细胞术将感染(发绿光)和未感染(不发光)的细胞分开。通过分析这细胞中 sgRNA 的丰度变化,就能精准定位出影响 HIV 感染的基因。
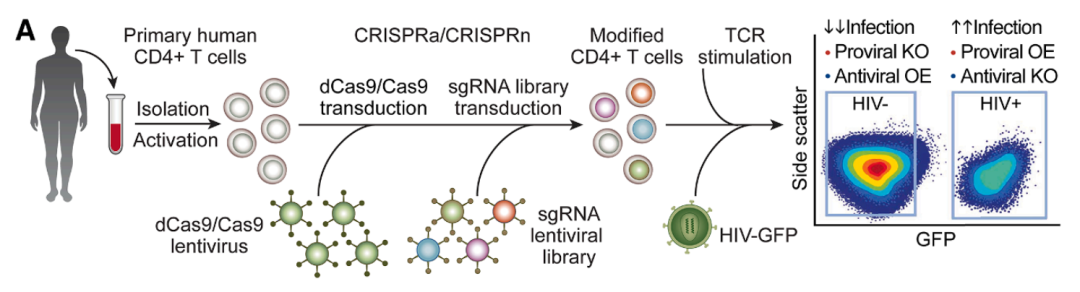
CRISPRa 和 CRISPRn 筛选
发现影响 HIV 感染的宿主因子名单
通过这项大规模的筛选,研究团队鉴定出了多个影响 HIV 感染的宿主因子。
促病毒因子(“帮凶”):当这些基因被敲除或抑制时,HIV 病毒的感染能力减弱。名单中包括许多转录因子(例如 TBX21)、肿瘤坏死因子超家族成员、细胞骨架相关蛋白以及整合素信号蛋白等。有趣的是,之前已知的辅助受体磺化修饰相关基因(SLC35B2、TPST2)也被确认为强效促病毒因子。
抗病毒因子(“克星”):当这些基因过表达时,HIV 感染被抑制。CRISPR 激活筛选比 CRISPR 敲除筛选发现了更多的抗病毒因子,凸显了该技术在挖掘“隐藏克星”方面的独特优势。名单中包括已知的抗病毒蛋白(例如 MX2、SPN),以及大量此前未知的全新因子。
值得注意的是,两个筛选结果高度互补且一致。只有一个基因 PPIA(编码 CypA 蛋白)表现特殊:无论是敲除还是过表达,都会降低 HIV 病毒的感染。这与其已知的复杂作用机制相符——适量的 CypA 是 HIV 的“帮凶”,因此,敲除会阻止感染,而过量则会导致病毒衣壳过于稳定,同样阻碍感染。
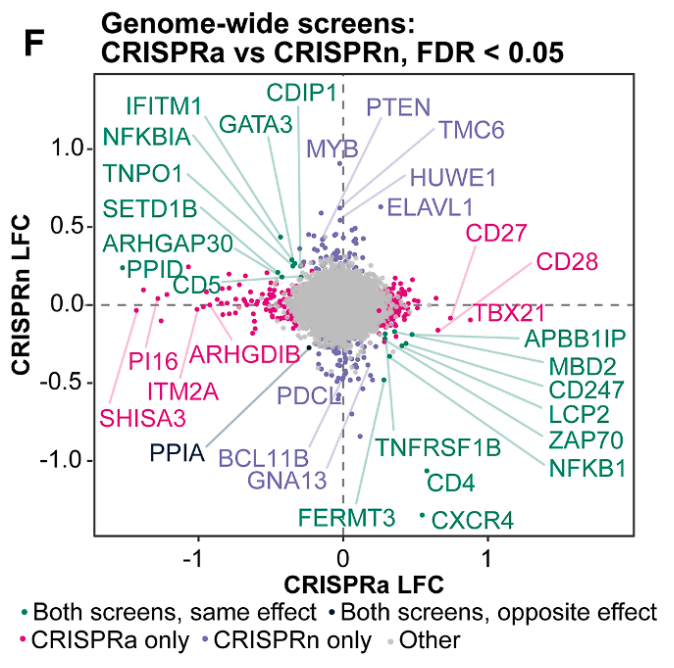
CRISPRa 和 CRISPRn 筛选结果比较,一致命中结果用绿色表示,不一致的命中结果用浅蓝色表示(只有一个,即 PPIA),仅 CRISPRa 命中结果用粉色表示,仅 CRISPRn 命中结果用紫色表示。
宿主因子如何影响 HIV 病毒的入侵?
这些宿主因子并非通过单一途径影响 HIV。通过后续的次级筛选和表型分析,研究团队发现,它们至少通过三种主要机制发挥作用:
1、调控 T 细胞活化状态:HIV 更易感染活化的 T 细胞。研究发现一部分宿主因子能影响 CD25、CD69 等活化标志物的表达,从而改变细胞对 HIV 的易感性。
2、调控 HIV入侵通道的数量:即改变病毒受体 CD4 和辅助受体 CXCR4 在细胞表面的水平。例如,直接过表达 CXCR4 能极大增强 HIV 的感染,而一些新发现的因子则通过调控这些受体的表达来影响感染效率。
3、干扰病毒生命周期的特定环节:使用 VSV-G 假病毒(绕过 CD4/CXCR4 进入细胞)进行的平行筛选,帮助区分了影响病毒进入环节和进入后环节的因子。
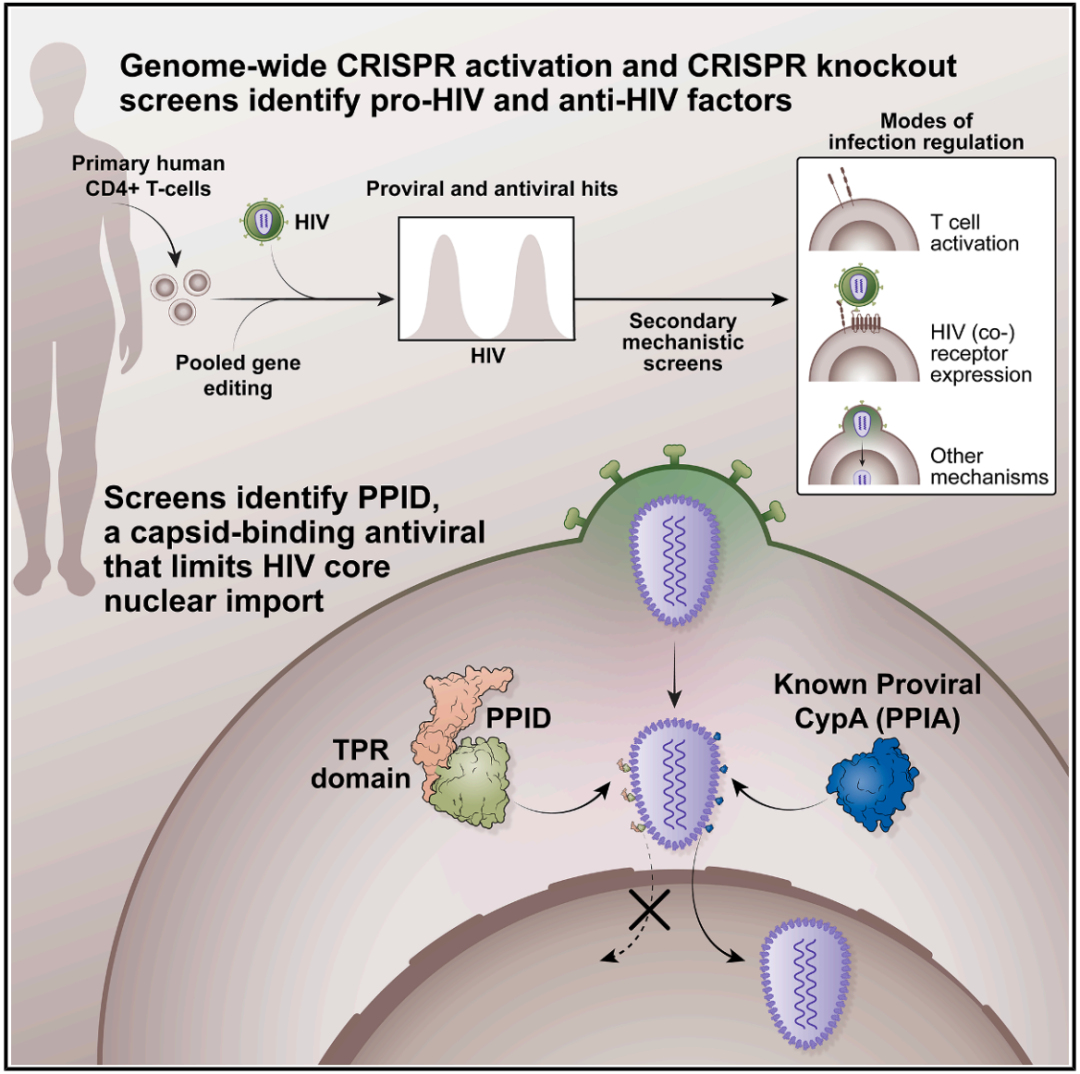
明星抗病毒因子:PI16 与 PPID
在所有新发现的抗病毒因子中,PI16 和 PPID 表现尤为突出,研究团队对它们进行了深入的机制探索。
PI16:守住病毒进入的“大门”,PI16 是一个功能未知的蛋白,该研究发现,过表达 PI16 能强力抑制 HIV 感染,但这种抑制作用在 VSV-G 假病毒实验中消失了。这表明 PI16 作用于病毒通过 HIV 包膜进入细胞的环节。进一步生化实验表明,PI16 能与参与 HIV 膜融合的宿主蛋白相互作用,从而抑制病毒与细胞的融合过程,把病毒挡在细胞门外。
PPID(Cyp40):在细胞核门口“设卡拦截”,PPID 是另一个明星因子,它是已知促病毒因子亲环蛋白 A(CypA)的旁系同源物。但有趣的是,PPID 发挥着截然相反的抗病毒作用。即使使用假病毒,PPID 的过表达依然能抑制感染,说明它作用于病毒进入细胞之后的步骤。研究团队发现,PPID 同样能够直接结合 HIV 的衣壳蛋白。然而,与 CypA 稳定衣壳、促进其进入细胞核不同,PPID 的结合会减少病毒核心向细胞核的输入,从而将病毒“困”在细胞质中,阻止其整合到人类基因组中。通过结构建模和定点突变,研究人员还鉴定出了 PPID 蛋白中负责抗病毒功能的关键结构域和氨基酸残基。
意义与展望:从图谱到新疗法
这项研究是首次在人类原代 CD4+ T 细胞中,无偏见、系统性地绘制出完整的 HIV-宿主因子相互作用图谱。它不仅验证了许多已知因子,更发现了大量全新因子,极大地扩展了我们对 HIV 与免疫细胞博弈复杂性的认知。
更重要的是,像 PI16 和 PPID 这样具有明确、强效抗病毒机制的新靶点的发现,为未来药物开发提供了全新方向。例如,可以设计小分子药物来模拟 PPID 的功能,干扰 HIV 衣壳的核输入;或者寻找能够上调 PI16 表达的药物,增强细胞对病毒入侵的天然防御。
总的来说,这项研究标志着我们对 HIV 的理解和对抗能力迈上了一个新台阶。从绘制“通缉名单”到解析“作案手法”,科学家们正一步步揭开 HIV 的弱点,为最终战胜艾滋病积累着关键的力量。
论文链接:
https://www.cell.com/cell/fulltext/S0092-8674(26)00382-X




点在看,传递你的品味




