In vivo CAR-T 最大并购案诞生!病毒递送 in vivo CAR-T/NK 获新进展

2026 年 4 月 26 日
医麦客新闻 eMedClub News
近日,礼来宣布以总金额高达 70 亿美元(含 32.5 亿美元首付款及里程碑付款)收购体内 CAR-T 公司 Kelonia Therapeutics,刷新体内 CAR-T 领域并购记录。这是继今年 2 月以 24 亿美元收购 Orna Therapeutics 后,礼来年内第二笔体内 CAR-T 重磅交易。
至此,礼来成为同时掌握环状 RNA+LNP 与慢病毒载体两种体内 CAR-T 技术平台的企业,覆盖自免与血液瘤两大领域,并有望将细胞疗法的应用拓展至更广泛的癌症和严重疾病。
Kelonia 的先导项目 KLN-1010 是一种在研体内 BCMA CAR-T,其治疗复发/难治性多发性骨髓瘤的 IND 申请已于今年 1 月获 FDA 批准。该批准使得 Kelonia 能够扩展其正在进行的 Ⅰ 期临床试验 inMMyCAR。
2025 年 12 月 ASH 年会公布的首次人体数据显示:前 4 例患者中,100% 患者达到微小残留病阴性缓解,持续缓解至少 5 个月,且安全性良好,为 Kelonia 的平台提供了概念验证。
Kelonia 的核心技术为体内基因放置系统(iGPS),采用经包膜修饰的慢病毒载体颗粒,通过趋向性分子实现组织特异性递送,并有望将体内 CAR-T 的应用拓展至更广泛的疾病领域。
凭借这一「主动靶向」机制及平台可拓展性,Kelonia 此前已吸引安斯泰来(2024 年 2 月,潜在总额超 8.75 亿美元)和强生(2025 年 11 月)达成合作。
MNC 重金押注体内 CAR 疗法
自 2024 年以来,阿斯利康、BMS、艾伯维、吉利德、强生等 MNC 通过并购与合作密集入局体内 CAR-T 赛道。LNP 递送(如,Orna、Capstan)与慢病毒载体递送(如,Kelonia、EsoBiotec、Interius)两条路线并驾齐驱。其中慢病毒载体因可实现稳定的基因组整合、支持长期 CAR 表达,对肿瘤治疗的持久性至关重要。
· 阿斯利康/EsoBiotec
2025 年 3 月,阿斯利康以最高 10 亿美元收购 EsoBiotec,获得其工程化纳米抗体慢病毒(ENaBL)平台及 4 条在研管线。该平台通过单次静脉注射即可实现细胞治疗,无需免疫细胞清除。
ESO-T01 是 ENaBL 平台的首发管线,通过纳米抗体靶向、免疫屏蔽的慢病毒递送载体,将人源化抗 BCMA CAR 序列直接递送至患者体内,实现 T 细胞的原位工程化改造。
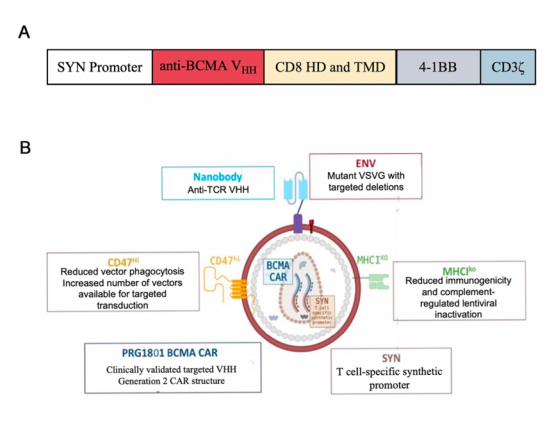
其治疗复发/难治性多发性骨髓瘤的 Ⅰ 期临床研究已发表于 Nature Medicine:单次静脉输注 0.2×10⁹ 转导单位后,5 例患者中 4 例达到客观缓解(含 3 例严格完全缓解),所有可评估缓解者(4/4)在第 60 天均达到微小残留病阴性(10⁻⁵)。
· 吉利德/Interius
2025 年 8 月,吉利德子公司 Kite Pharma 以 3.5 亿美元收购 Interius,获得后者核心 LENTIVECTOR 平台以及首发管线 INT2104。Interius 的慢病毒平台采用模块化设计,主要包括三个部分:
Binder:存在于慢病毒表面,用于识别体内的靶细胞,INT2104 采用 CD7 binder,用于识别 CD7+ 细胞;
fusogen:与靶细胞膜融合,实现慢病毒所携带基因的递送,INT2104 采用经过改造的去靶向化的 vsv-g;
Gargo:通常为转基因,可在靶细胞内进行表达并实现相应疗效,INT2104 采用自失活的 CAR 基因,可编码全人源的 CD20 分子。
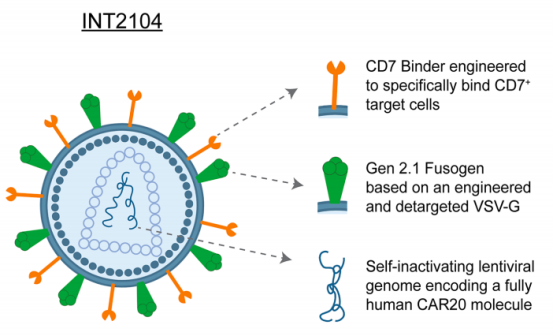
INT2104 正在开展针对复发/难治性 B 细胞恶性肿瘤的 Ⅰ 期临床。临床前数据发表于 Molecular Therapy:单次给药后可生成 CAR-T 和 CAR-NK 细胞,有效清除 CD20+ B 细胞,且未观察到 CRS 或神经毒性。
医麦客携手浚真生命科学于 2026 年 4 月 28 日(周二)19:00--20:00 带来主题为「生物工艺开发视角下的细胞计数结果评价方法」的直播课,邀请了药明生物助理主任苟超和浚真生命科学研发应用部经理王明翠进行线上演讲,将从细胞计数结果评价、数据桥接、细胞计数仪应用案例等方面带来干货分享,欢迎大家扫码预约直播课!

· 艾伯维/Umoja
Umoja 核心平台 VivoVec,采用慢病毒载体递送系统,具备四大独特优势:多结构域融合(MDF)表面工程技术增强 T 细胞结合与转导效率;Cocal 融合糖蛋白假型化抵抗人血清灭活,保障高药效;模块化设计支持多靶点 CAR 载荷递送;可与 RACR 平台联合提升免疫细胞存活与增殖能力。
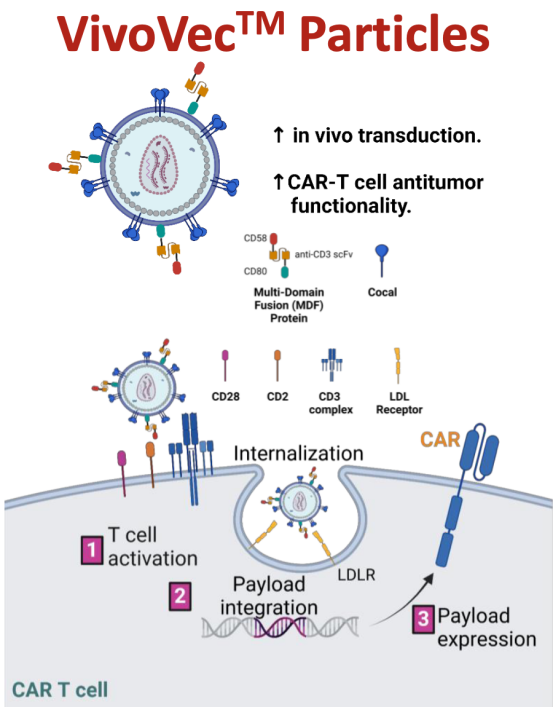
依托该平台,Umoja 已布局多款管线,其中靶向 CD19 的 UB-VV111 是首个获 FDA 批准临床的体内 CAR-T,正开展针对 CD19+ B 细胞恶性肿瘤的 Ⅰ 期研究(与艾伯维合作开发);CD22 靶向 UB-VV400/410 处于 Ⅰ 期临床,拟用于治疗 NHL 及自身免疫疾病,艾伯维拥有独家选择权。
国内企业加速突破
在国内,石药集团、易慕峰、驯鹿生物、博生吉、原启生物、传奇生物、济因生物、先博生物等多家企业已布局慢病毒载体递送的体内 CAR-T/NK,且已推进至临床阶段。今年来,多家企业获得进展:
4 月,易慕峰公布了基于自研 iMAGIC 平台(慢病毒载体体内 CAR-T 技术平台)开发的靶向 BCMA 体内 CAR-T 候选疗法 IMV102 的最新临床前研究成果。iMAGIC 平台载体表面覆盖突变型 MxV 糖蛋白(MxV-G-mut),通过突变消除受体结合能力但保留膜融合活性;同时整合新一代 T 细胞靶向模块 TCM3,高特异性识别并结合 T 细胞表面受体,实现对 T 细胞的高效转导。
体内研究中,IMV102 通过单次给药在两种多发性骨髓瘤异种移植小鼠模型(H929-Luc 和 MM.1S-Luc,人 PBMC 重建)中成功诱导靶向 BCMA CAR-T 细胞的体内生成,伴随 IFN-γ 分泌水平升高。研究期间,两个模型均实现显著且持续的肿瘤负荷降低,证实单次给药即可发挥抗肿瘤作用。同时,给药组小鼠状态未见异常,体重保持稳定,表明 IMV102 具有良好的安全性。
4 月,原启生物宣布完成 1.1 亿美元 Pre-IPO 轮融资,并表示公司的全平台技术体系正持续孵化多个下一代多靶点、多机制的 CAR-T 产品,包括分泌型、快速生产型和多款 in vivo CAR-T 项目。
3 月,传奇生物公布全年业绩时透露,已完成体内(in vivo)管线候选产品的首例患者给药。
3 月,博生吉杨林博士在接受采访时表示,公司自主研发的慢病毒体内 CAR 疗法 LV009 注射液已完成首例患者给药,战略定位为「以血液瘤为基石,向实体瘤和自身免疫病双向延伸」。
LV009 采用慢病毒载体系统,通过静脉注射,即可在体内精准武装患者自身的 T 细胞与 NK 细胞,使其同步表达靶向 CD19 的 CAR,实现适应性免疫和先天免疫协同攻击肿瘤细胞。
1 月,石药集团 SYS6055 注射液获 CDE 临床默示许可,拟开发治疗复发/难治侵袭性 B 细胞淋巴瘤,成为国内首款获批临床的体内 CAR-T。SYS6055 通过慢病毒载体在体内直接生成靶向 CD19 的 CAR-T 细胞,可特异性识别和清除靶细胞,从而达到治疗目的。
临床前研究显示,该疗法能够在体内高效生成 CAR-T 细胞,具备显著的抑瘤效果与良好的安全性,同时具有成本和时间优势。此外,该管线有望拓展至其他 CD19 阳性 B 细胞恶性肿瘤及自身免疫病的治疗。
责任编辑丨菊
校对丨菊
参考资料:
1.https://investor.lilly.com/news-releases/news-release-details/lilly-acquire-kelonia-therapeutics-advance-vivo-car-t-cell
2.https://www.nature.com/articles/s41591-026-04244-6
3.https://www.sciencedirect.com/science/article/pii/S1525001625004873
4. 各企业官方资料
精彩活动
长按识别二维码立即参与↓

点点“分享”、“点赞”和“在看”
给我充点儿电吧~