掘金下一个ADC新蓝海:B7-H3靶点ADC药物的疗效突破与未来挑战
发布时间:2026-04-27来源:药事纵横
抗体药物偶联物(ADC)在近几年的抗肿瘤药物研发中占据着极为核心的地位。随着靶向HER2和TROP2的ADC药物在临床实践中取得巨大成功,业界对新型靶点的探索步伐不断加快。B7-H3作为B7免疫共刺激分子家族的重要成员,因其独特的生物学表达特性正受到广泛关注。该靶点在多种实体瘤中呈现过度表达状态且与患者不良预后密切相关,但在正常组织中的表达却十分有限。这种巨大的表达差异使其成为构建精准靶向药物的理想选择。当前全球尚未有靶向B7-H3的ADC药物获批上市,但多条研发管线已在小细胞肺癌、妇科肿瘤等领域展现出令人瞩目的疗效数据。本文将从靶点机制、临床数据、安全性挑战以及未来发展方向等多个维度,对当前B7-H3靶点ADC药物的研发现状进行科学客观的深度分析。一、B7-H3靶点的生物学优势与成药潜力
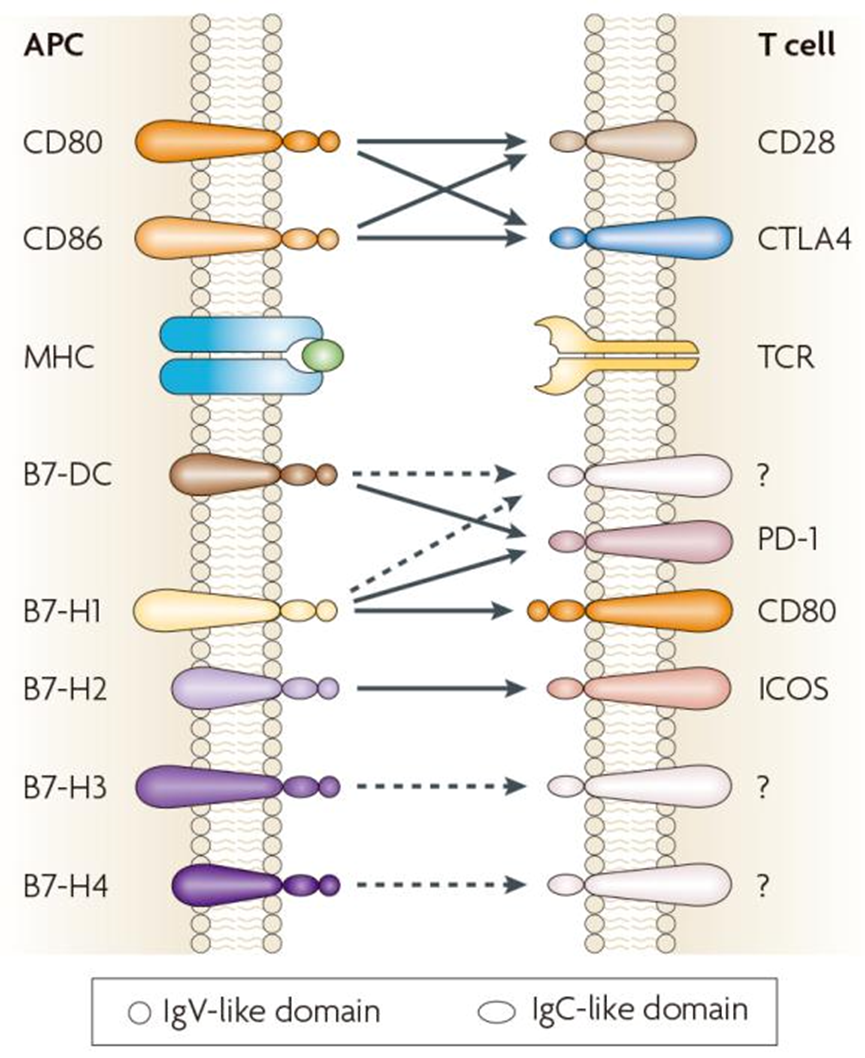
B7超家族分子是一类主要表达于抗原呈递细胞表面的跨膜蛋白,其典型成员包括CD80、CD86及B7-H1(即PD-L1)等。该超家族分子的表达受多重机制精密调控,在肿瘤细胞的增殖、迁移、免疫逃逸及耐药过程中发挥着关键作用。基于此,B7超家族成员被广泛视为肿瘤免疫治疗的重要潜力靶点,其中针对B7-H1(PD-L1)的靶向治疗已在临床中取得显著成效。其中,B7-H3在肿瘤微环境中扮演着双重促癌角色。一方面它参与构建免疫抑制屏障,帮助肿瘤细胞逃避免疫系统的监视与清除。另一方面它还能直接促进肿瘤细胞的增殖、转移以及血管生成。这种双重机制意味着靶向B7-H3不仅能解除免疫抑制,还能直接对肿瘤细胞实施打击。从表达谱来看,B7-H3具有极高的广谱性。研究数据显示70%-100%的卵巢癌、结直肠癌、前列腺癌、胰腺癌和乳腺癌样本中均显示B7-H3表达。此外,在小细胞肺癌领域,约65%的样本呈阳性表达。更为关键的是,相较于DLL3等其他小细胞肺癌潜力靶点,B7-H3在该癌种的四种主要分子亚型中均呈现高且一致的表达,肿瘤内部及个体间的异质性较低。这为ADC药物提供了极为广阔且稳定的潜在治疗人群基础。由于早期开发的B7-H3单克隆抗体或双特异性抗体受限于结构本身的抗肿瘤效力不足,临床疗效未达预期,直到ADC技术平台逐渐成熟,搭载高活性细胞毒素的B7-H3 ADC才真正释放了该靶点的治疗潜力。二、小细胞肺癌领域的重磅突破与管线情况
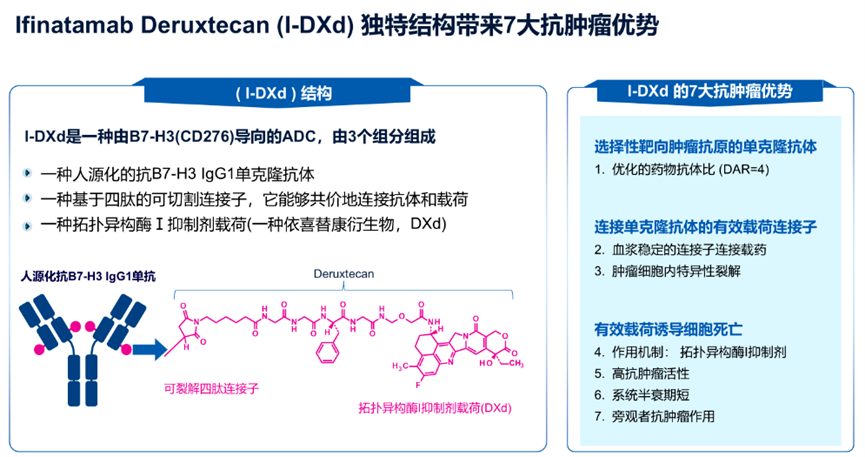
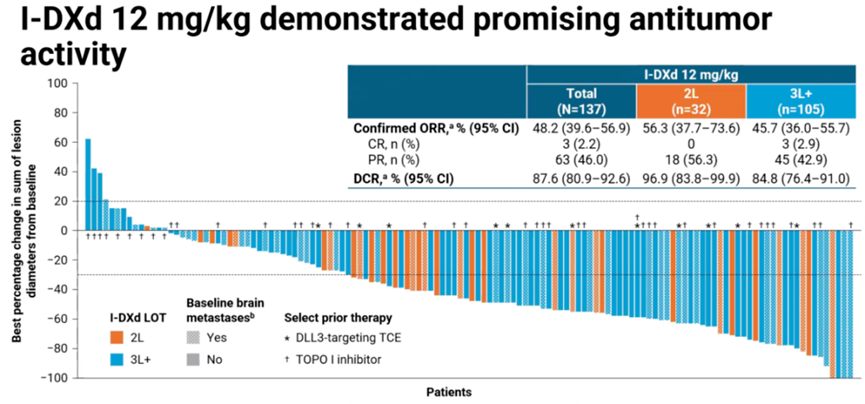
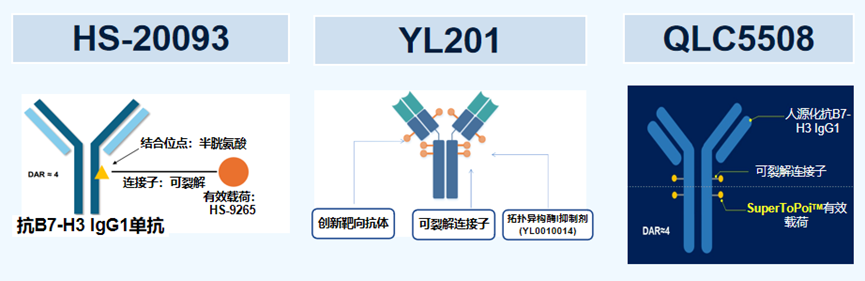
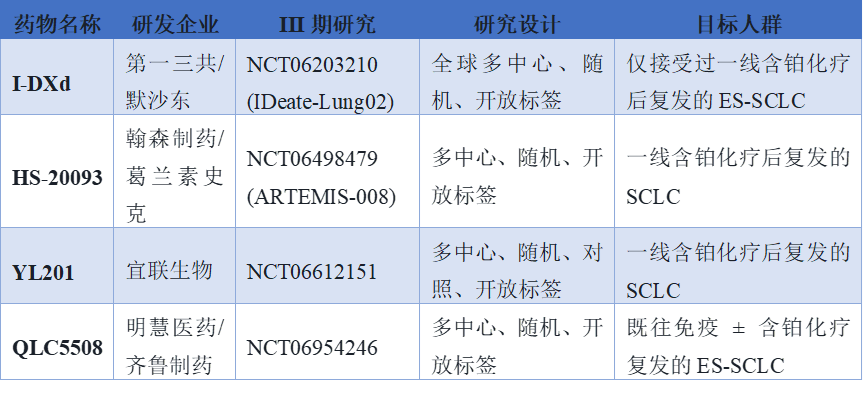
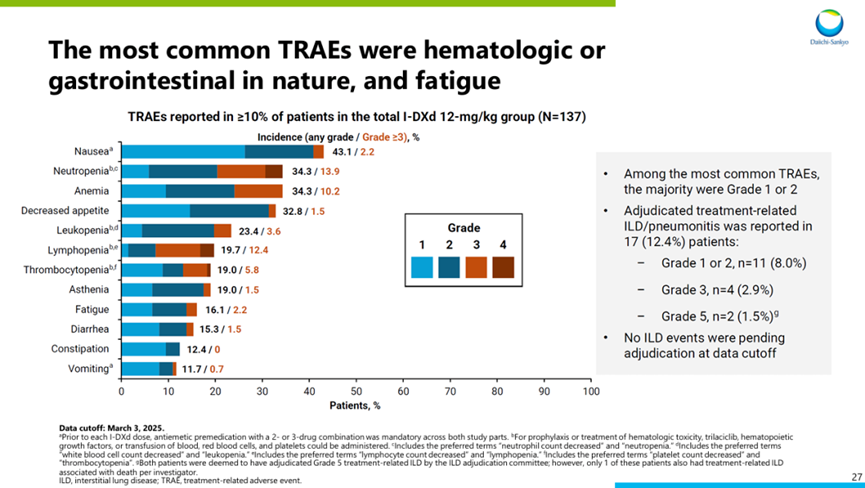
广泛期小细胞肺癌恶性程度极高,极易复发转移。尽管免疫检查点抑制剂联合化疗已成为一线标准治疗,绝大多数患者仍在短期内面临疾病进展。传统二线化疗药物如拓扑替康的客观缓解率十分有限,临床亟需更有效的后线方案。B7-H3 ADC的介入正在重塑这一格局。第一三共与默沙东联合开发的Ifinatamab Deruxtecan(I-DXd)在该领域处于领先地位。该药物采用第一三共经典的GGFG-Dxd构建,药物抗体比值为4。基于IDeate-Lung01二期临床试验结果,其已于近期向美国食品药品监督管理局(FDA)提交生物制品许可申请并获得优先审评资格。2025年世界肺癌大会(WCLC)公布的IDeate-Lung01研究主要分析结果显示,在137例接受12 mg/kg I-DXd治疗的患者中(中位随访12.8个月),经盲态独立中心审查确认的客观缓解率与疾病控制率分别达到48.2%和87.6%。该疗效在不同治疗线数人群中均得到维持,其中二线治疗亚组(n=32)的获益尤为显著,cORR与DCR分别高达56.3%和96.9%。在生存获益方面,整体人群的中位至缓解时间为1.4个月,中位缓解持续时间、无进展生存期(PFS)及总生存期(OS)分别为5.3、4.9和10.3个月;二线亚组的生存数据进一步改善,中位PFS和OS分别延长至5.6和12.0个月。安全性方面,最常见的不良反应为胃肠道反应及血液学毒性,且多以1~2级为主,≥3级治疗相关不良事件(TRAEs)发生率为36.5%,整体展现出可控的安全性与良好的耐受性。除第一三共外,国内多家药企的管线也已进入群雄逐鹿阶段。宜联生物的YL201基于其特有平台开发,药物抗体比值达到8。其在广泛期小细胞肺癌中的客观缓解率达到63.9%-73.7%,中位无进展生存期超过6个月,并已获得中美双突破性疗法认定,目前与罗氏达成巨额海外授权合作。翰森制药与葛兰素史克合作的HS-20093在8.0mg/kg剂量组的客观缓解率为61.3%,中位无进展生存期达5.9个月。明慧医药与齐鲁制药合作的QLC5508在2.0mg/kg剂量组也展现出中位无进展生存期5.95个月和中位总生存期11.73个月的稳健数据。这四款药物均已进入三期临床阶段,形成了多元并进的激烈竞争态势。三、向其他实体瘤拓展的显著疗效
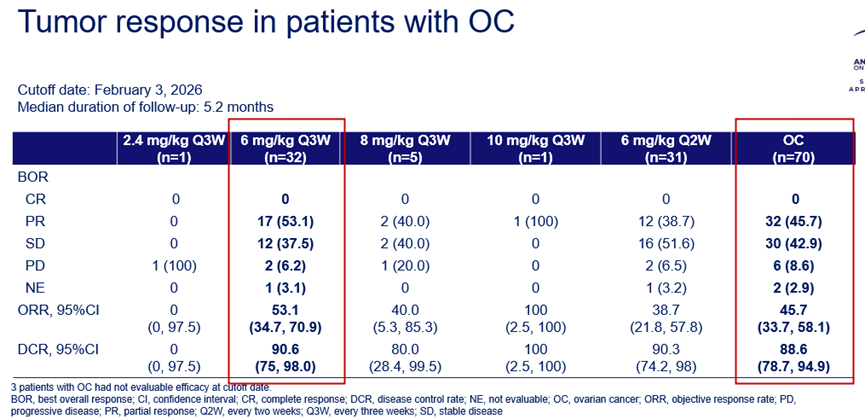
B7-H3的高表达特性不仅局限于肺癌,其在妇科肿瘤中的表现同样亮眼。在近期举行的美国妇科肿瘤学会(SGO)年会上,两款国产B7-H3 ADC更新了在铂耐药卵巢癌中的数据。石药集团开发的SYS6043在可评估的铂耐药高级别浆液性卵巢癌患者中,展现出了显著的抗肿瘤活性。在一项针对70例可评估疗效的卵巢癌患者的研究中,客观缓解率(ORR)为45.7%,疾病控制率(DCR)高达88.6%,中位无进展生存期(PFS)达到8.3个月,中位缓解持续时间(DoR)为6.9个月。该药物在高级别浆液性卵巢癌亚组中活性尤为突出,客观缓解率(ORR)高达51.8%。在6 mg/kg、每3周一次(Q3W)的给药方案下(n=32),患者的ORR和DCR分别提升至53.1%和90.6%。尤为重要的是,SYS6043在B7-H3阴性人群中仍能观察到36.4%的客观缓解率,与阳性人群的48.2%相比,体现了其“适度富集、广谱覆盖”的独特优势。此外,映恩生物与BioNTech合作的DB-1311在铂耐药卵巢癌患者中的客观缓解率(ORR)更是高达53.3%,疾病控制率(DCR)为83.3%,中位无进展生存期(mPFS)达9.5个月。这些数据充分证实了B7-H3 ADC在传统治疗手段捉襟见肘的妇科晚期肿瘤中具有极强的杀伤力。特别值得关注的是这些药物在临床应用中无需进行严格的生物标志物筛选。由于B7-H3在上述癌种中的高表达比例,泛瘤种用药的覆盖面极广,这大大降低了临床实施的门槛,提升了药物的可及性。四、脑转移病灶的穿透与控制能力
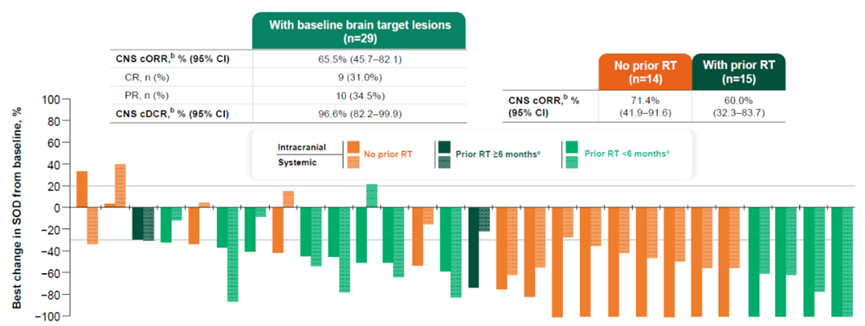
脑转移是晚期小细胞肺癌患者面临的重大临床挑战,血脑屏障的存在使得许多大分子药物难以在颅内达到有效浓度。B7-H3 ADC在临床研究中意外展现出了优异的中枢神经系统活性。第一三共的I-DXd在基线伴有脑转移的患者中,颅内客观缓解率达到46.2%,其中完全缓解率占30.8%。在具有可测量颅内靶病灶的患者亚组中,颅内客观缓解率达到65.5%,且这一疗效不受既往是否接受过脑部放疗的影响。在基线无脑转移的患者中,治疗后出现新发脑转移的比例仅为12.5%,提示其可能具有延缓脑转移发生的作用。宜联生物的YL201同样报告了积极的颅内疗效数据。在存在基线脑部靶病灶的肺癌患者中,确认的颅内客观缓解率为30.8%,颅内疾病控制率达100%。对于近期未接受过脑部放疗的患者,其颅内客观缓解率可达57.1%。这些数据强有力地证明了当前先进的ADC技术平台能够有效突破血脑屏障限制,解决实体瘤脑转移的临床痛点。五、间质性肺炎阴霾与安全性博弈
尽管疗效显著,但安全性问题,尤其是间质性肺炎,仍是B7-H3 ADC类药物研发与应用中亟待解决的关键挑战。第一三共基于Dxd的ADC创新平台虽然开创了新一代ADC研发热潮,但间质性肺炎始终是伴随其产品开发的阴霾。在I-DXd的二期临床中,间质性肺炎发生率为12.4%,三级及以上为4.4%。然而在其同步进行的三期临床Ideate-Lung02研究中,因出现了五级间质性肺炎致死事件,该研究一度在全球范围内暂停。尽管美国在短期内恢复了临床,但欧洲部分区域仍处于暂停状态。此前该平台的明星药物Enhertu已因间质性肺炎被加上黑框警告,且因该不良事件导致患者停药的比例占到一半以上。面对这一挑战,国内药企在连接子与载荷设计上采取了不同的规避策略。诺诚健华在近期公布的临床前数据中展示了其新型B7-H3 ADC药物ICP-B794。该药物采用不可逆接头搭配高亲水性连接子,搭载新型强效载荷。临床前毒理学研究显示其安全窗口高达两百多倍,且药物抗体比值在人体血浆中保持高度稳定,有效载荷不易提前释放,从结构底层逻辑上试图降低脱靶毒性。这种通过改善理化性质和药代动力学特征来拓宽治疗窗口的策略,代表了B7-H3 ADC下一步技术迭代的重点方向。六、未来面临的挑战与破局方向
随着多款B7-H3 ADC药物进入商业化阶段,未来的竞争格局将不再局限于单纯的有效性比拼,而是转向基于精准应用与差异化策略的深层次竞争。首先是生物标志物的探索。现有临床数据表明,B7-H3的蛋白表达水平与ADC疗效并未呈现明确的线性相关性,单一蛋白表达不足以筛选最佳获益人群。未来的转化医学研究需要向更深层次探索,例如将B7-H3表达与肿瘤分子亚型、微环境中CD8阳性T细胞浸润程度甚至肿瘤代谢状态进行整合建模,从而精准识别深度获益亚群。其次是耐药机制的破解。潜在的耐药机制包括靶点抗原下调或丢失、药物外排泵激活以及DNA损伤修复增强等。前瞻性的应对策略正在酝酿,例如开发搭载不同作用机制的双载荷B7-H3 ADC,通过细胞毒性药物与免疫调节剂的协同作用来克服单药耐药并逆转免疫抑制微环境。此外序贯使用不同技术平台的药物也可能成为延缓耐药的有效手段。第一三共I-DXd正在探索联合阿替利珠单抗加卡铂用于一线治疗的潜力,宜联生物的YL201也获得了联合斯鲁利单抗用于广泛期小细胞肺癌一线治疗的突破性疗法认定。从后线单药向前线联合治疗的挺进,将是该靶点药物放大队列价值的关键路径。七、结语
总的来说,B7-H3靶点ADC药物的研发正处于从临床验证走向商业化兑现的黄金时期。以第一三共I-DXd提交上市申请为标志,小细胞肺癌二线治疗缺乏高效药物的局面有望被彻底打破。同时国内药企如宜联生物、翰森制药、石药集团等展现出的强劲研发实力,使得该赛道形成了百花齐放的繁荣态势。尽管间质性肺炎等安全性挑战依然存在,且精准生物标志物的缺失在一定程度上制约了药物的极致应用,但随着新型连接子与毒素平台的不断迭代,以及联合治疗策略的深入推进,B7-H3 ADC有望在不久的将来跨越重重障碍,为包括小细胞肺癌和妇科恶性肿瘤在内的广大实体瘤患者提供更具生存获益的治疗新选择。[1] Zou W, Chen L. Inhibitory B7-family molecules in the tumour microenvironment. Nat Rev Immunol. 2008 Jun;8(6):467-77. doi: 10.1038/nri2326.[2] Ifinatamab Deruxtecan Granted Priority Review in the U.S. for Adult Patients with Previously Treated Extensive-Stage Small Cell Lung Cancer who Experienced Disease Progression on or After Platinum-Based Chemotherapy.[4] Carvajal-Hausdorf D, Altan M, Velcheti V, et al. Expression and clinical significance of PD-L1, B7-H3, B7-H4 and TILs in human small cell lung Cancer (SCLC)[J]. Journal for immunotherapy of cancer, 2019, 7(1): 65.[5] da Rocha P F S, Kim Y J, Han J Y, et al. 2760MO Intracranial activity of ifinatamab deruxtecan (I-DXd) in patients (pts) with extensive-stage (ES) small cell lung cancer (SCLC) and baseline (BL) brain metastases (BM): Primary analysis of IDeate-Lung01[J]. Annals of Oncology, 2025, 36: S1467-S1468.
转载说明:本文系转载内容,版权归原作者及原出处所有。转载目的在于传递更多行业信息,文章观点仅代表原作者本人,与本平台立场无关。若涉及作品版权问题,请原作者或相关权利人及时与本平台联系,我们将在第一时间核实后移除相关内容。