Angew | 脂质体重塑为盘:实现跨血脑屏障与深部肿瘤浸润
2026年4月11日,中国科学院上海药物研究所吴振永团队与烟台新药创制山东省实验室合作在
Angewandte Chemie International Edition
发表题为
“Amphiphilic Zwitterionic Polymers Induce Liposome Morphogenesis into Nanodiscs for Deep Glioblastoma Infiltration”
的研究论文。该研究设计并合成了一种新型两亲两性聚合物(zPMA),可高效诱导脂质体结构重塑形成纳米盘,并系统揭示了其形态转变机制。所构建的聚合物纳米盘(zNDs,粒径约15.5 nm)兼具高效跨血脑屏障、深部实体瘤浸润及药物递送三重功能,为脑部重大疾病治疗提供了全新策略。

胶质母细胞瘤(GBM)是恶性程度最高的原发性脑肿瘤之一,中位生存期不足15个月。其临床治疗长期受限于两大关键屏障:首先是血脑屏障(BBB),作为高度选择性的内皮界面,可阻断绝大多数小分子及几乎所有大分子药物进入脑组织;其次是GBM作为异质性肿瘤具有高间质压力、异常血管结构以及致密的细胞外基质,严重限制药物向肿瘤深部的有效扩散。尽管脂质体、聚合物纳米颗粒及胶束等多种纳米递送体系已被用于脑部给药研究,但仍普遍面临脱靶效应、非特异性分布及肿瘤浸润能力不足等问题,难以同时突破血管与基质构成的双重屏障。
针对上述挑战,吴振永团队围绕高效跨越血脑屏障并实现深部肿瘤递送这一科学问题开展了系统性研究:一方面,聚焦跨血脑屏障转运及肿瘤浸润的关键生物学机制解析;另一方面,发展能够实现主动跨屏障运输与深部递送的纳米递药策略
(
Journal of Nanobiotechnology
, 2025;
Journal of Controlled Release
, 2026)
。在此基础上,基于大脑对胆碱主要依赖血液循环供给的生理特性,研究团队从头设计并合成了一种胆碱仿生两亲性共聚物来模拟膜支架蛋白功能,由疏水性甲基丙烯酸己酯(HMA)与亲水性甲基丙烯酰氧乙基磷酰胆碱(MPC)构成。该聚合物可与磷脂分子协同自组装,形成无蛋白的纳米盘结构(zNDs)。相关技术已申请发明专利。
研究解析了脂质体向纳米盘重塑的三阶段机制:聚合物插入脂膜、膜结构破坏以及经膜重塑驱动的纳米盘重组。所得zNDs在生理条件下表现出优异的胶体稳定性,并可通过胆碱转运体(CHTs)介导的转胞吞作用高效穿越血脑屏障。在原位胶质瘤模型中,zNDs展现出显著的深层肿瘤穿透能力,并通过网格蛋白介导的内吞途径进入细胞,同时有效逃逸内溶酶体区室。最后团队与烟台新药创制山东省实验室管栋梁课题组合作,通过整合脂质-药物偶联策略,实现了和厚朴酚(HNK)的高效递送,构建HNK@zND复合体系。该体系不仅能够有效解构三维胶质瘤球体,还在原位肿瘤模型中显著抑制肿瘤生长,并在无明显全身毒性的前提下,将实验动物中位生存期延长近2.5倍。
本研究构建了一个模块化、无蛋白、低免疫原性的创新纳米递送平台,将理性聚合物设计与主动血脑屏障转运机制有机结合,为中枢神经系统恶性肿瘤的深部治疗提供了多功能解决方案,同时也为新一代血脑屏障穿透型纳米载体的设计提供了重要的机制依据。
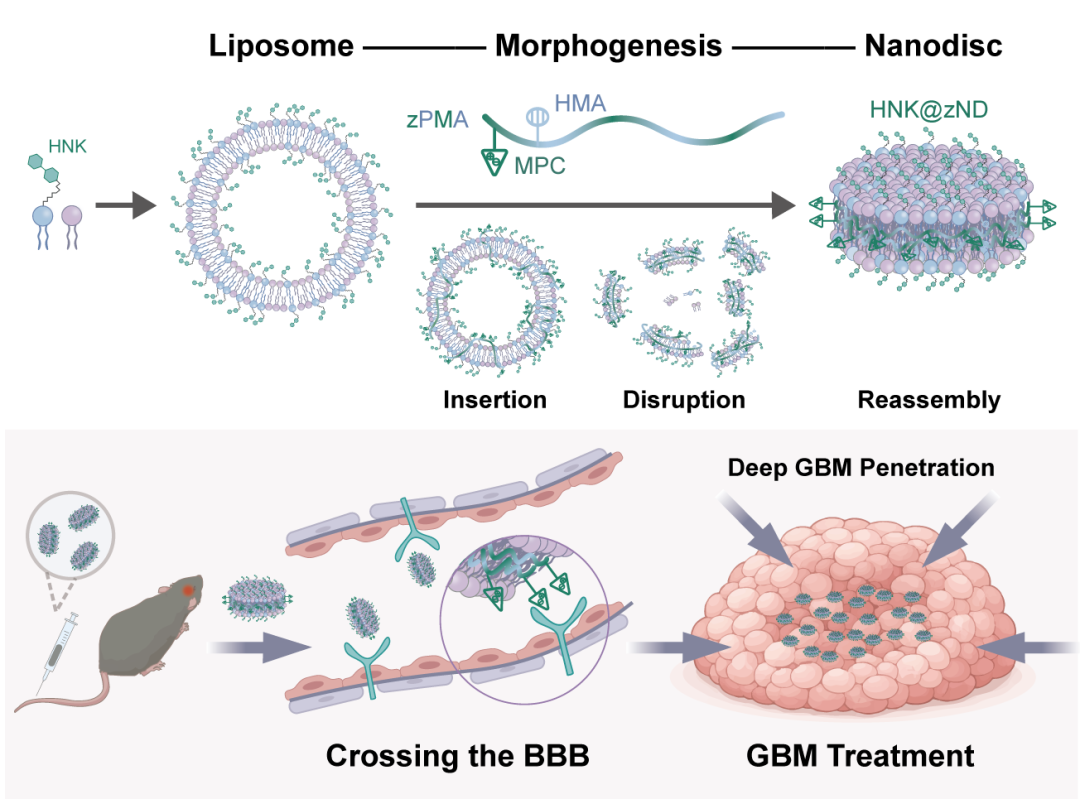
脂质体重塑为纳米盘的动态过程及功能表征
烟台新药创制山东省实验室联合培养硕士研究生黎烨莹、博士生徐小彭及郝腾为该本文共同第一作者,上海药物所吴振永研究员为本论文通讯作者。该研究获得国家自然科学基金、泰山学者计划、山东省重点研发计划、山东省青年科学基金及烟台市基础研究重点项目等多项资助。
吴振永课题组
以纳米技术为核心手段,解析神经生物学关键过程及重大脑疾病机制,在神经生物学与化学生物学交叉领域持续开展创新研究(
Journal of the American Chemical Society
, 2025)。并在此基础上推动基础理论向疾病干预策略的转化,致力于将机制认知转化为可用于脑疾病诊疗的新型技术与方法,服务于临床需求。课题组现诚邀神经生物学等相关方向博士后加入,共同开展面向临床应用的原创性探索。
全文链接
